Foram encontradas 50 questões.
A espectroscopia no infravermelho é uma poderosa ferramenta para identificação de compostos, especialmente orgânicos.
A atribuição da presença de tipos de cadeias carbônicas e grupos funcionais é possível a partir do modelo de modos
vibracionais de simetria, uma vez que esses modos apresentam frequências e formatos de bandas típicos no espectro. A
seguir, é mostrado um espectro de infravermelho por transformada de Fourier (FTIR) de um composto orgânico.
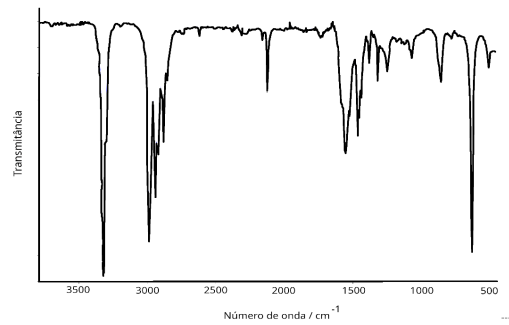
O espectro FTIR apresentado é atribuído a qual molécula orgânica?

O espectro FTIR apresentado é atribuído a qual molécula orgânica?
Provas
Questão presente nas seguintes provas
Na cromatografia gasosa, uma amostra de uma mistura que se quer analisar é injetada no instrumento e entra em uma
corrente de gás, chamada de fase móvel, que transporta essa amostra para a coluna de separação. Os componentes
são separados dentro dessa coluna, e o detector mede a quantidade dos componentes que saem da coluna. A
separação dentro da coluna se dá por dois parâmetros: (i) efeito da volatilidade dos compostos, em que os mais
voláteis tendem a passar mais tempo na fase móvel e têm um menor tempo de retenção; (ii) efeito da polaridade, em
que os compostos de maior polaridade tendem a interagir mais fortemente quando utilizada coluna constituída de
material cuja superfície possui natureza polar e têm maior tempo de retenção. Considere uma amostra constituída de
uma mistura dos compostos I a V, cujas estruturas são mostradas na figura a seguir. Essa amostra foi injetada num
instrumento que possui uma coluna de sílica.
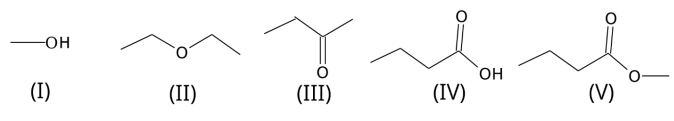
A sequência da saída dos compostos, do menor ao maior tempo de retenção, é:

A sequência da saída dos compostos, do menor ao maior tempo de retenção, é:
Provas
Questão presente nas seguintes provas
Quando o oxigênio líquido é derramado entre dois polos de um ímã, ele fica aprisionado, evidenciando o seu
paramagnetismo. A Teoria do Orbital Molecular (TOM) ganhou grande aceitação na ciência por explicar justamente
essa propriedade, o que a Teoria da Ligação de Valência (TLV) é incapaz de fazer, uma vez que, ao considerar a
estrutura de Lewis, coloca os elétrons emparelhados numa dupla ligação entre os dois átomos de oxigênio. Na TOM,
cada estado é descrito por um termo espectroscópico, que simplificadamente é um símbolo dado pela notação 2S+1Λ,
em que S é spin total e Λ é o momento angular orbital, atribuindo-se Σ, Π e Δ para momentos iguais a 0, 1 e 2,
respectivamente. O momento angular orbital de um elétron em um orbital molecular é dado por λ = |ml|, em que ml é o
número quântico magnético. Para o orbital σ, λ = 0 e para orbital π, λ = 1.
A molécula de oxigênio molecular no seu estado fundamental possuirá os elétrons de valência e termo espectroscópico, respectivamente, iguais a:
A molécula de oxigênio molecular no seu estado fundamental possuirá os elétrons de valência e termo espectroscópico, respectivamente, iguais a:
Provas
Questão presente nas seguintes provas
Compostos inter-halogênios são formados por dois ou mais átomos diferentes de elementos pertencentes ao
grupo XVII. Em sua maioria, esses compostos são binários, e suas fórmulas são geralmente XYn, em que n varia
de 1 a 7. O átomo Y é o mais eletronegativo e assume NOX −1. A ligação química pode ser descrita pela Teoria de
Ligação de Valência, e as geometrias podem ser previstas pelo modelo de Repulsão de Pares de Elétrons da Camada
de Valência (conhecida pela sigla em inglês VSEPR). O trifluoreto de cloro apresenta-se como um gás incolor com odor
irritante. Bastante reativo, é suscetível a hidrólise e, em contato com materiais orgânicos, pode resultar em ignição
espontânea. É corrosivo para metais e tecidos e, sob calor intenso, o recipiente pode romper-se violentamente e ser
projetado como um foguete.
Com base nas informações do texto, quais são a geometria molecular e a hibridação de orbitais atômicos do átomo central da molécula inter-halogênio mencionada?
Com base nas informações do texto, quais são a geometria molecular e a hibridação de orbitais atômicos do átomo central da molécula inter-halogênio mencionada?
Provas
Questão presente nas seguintes provas
O prêmio Nobel de Química de 2025 foi destinado a três pesquisadores pelas suas contribuições à área de redes
metalorgânicas (Metal-Organic Framework – MOF). Esses materiais são promissores em diversas aplicações, como
captura de CO2 e água da atmosfera, catálise e armazenamento de hidrogênio verde. A síntese desses materiais é
relativamente simples; por exemplo, um MOF pode ser preparado ao misturar AlCl3.6H2O com
ácido 3,5-pirazoldicarboxílico (H2DPC, estrutura mostrada na figura) na proporção 1:2 em água e colocado em
autoclave a 180 °C por 12 horas. A reação é determinada por controle termodinâmico, isto é, as interações ácido-base
de Lewis direcionam o produto. Ao término, são obtidas as redes estendidas, cristalinas, porosas, bastante estáveis e
insolúveis do MOF.
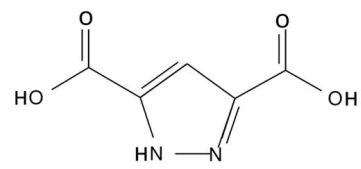
O material mencionado no texto é produzido graças às interações entre:

O material mencionado no texto é produzido graças às interações entre:
Provas
Questão presente nas seguintes provas
A crioterapia é largamente utilizada por atletas para recuperação muscular. Atualmente, existem no mercado
compressas de gelo instantâneas que se baseiam no processo endotérmico da dissolução de nitrato de amônio
(NH4NO3, M = 80 g mol–1) em água (capacidade térmica específica c = 4,2 J g–1 K–1). Essas compressas são bolsas
descartáveis, normalmente de tecido de polipropileno, que contêm inicialmente, em compartimentos separados, água
e o sal de amônio, que, quando misturados, atingem a temperatura de até 0 ºC. A entalpia de dissolução do nitrato de
amônio é um processo que está relacionado à entalpia de rede cristalina (ΔlatH = −646 kJ mol–1) e a entalpias de
hidratação do cátion (ΔhidH = −307 kJ mol–1) e do ânion (ΔhidH = −313 kJ mol–1). Uma compressa possui uma certa massa
de sal de amônio e 200 g de água e está inicialmente a 20 ºC.
Para que a temperatura da compressa atinja 0 ºC (considerando que não há trocas de calor com o tecido nem com o exterior), a massa, em gramas, de sal de amônio no compartimento deve ser mais próxima de:
Para que a temperatura da compressa atinja 0 ºC (considerando que não há trocas de calor com o tecido nem com o exterior), a massa, em gramas, de sal de amônio no compartimento deve ser mais próxima de:
Provas
Questão presente nas seguintes provas
Soluções-tampão são muito empregadas em laboratório, uma vez que são capazes de resistir a mudanças
de pH quando ácidos ou bases são adicionados, permitindo maior controle sobre variáveis experimentais. O tampão
ácido acético (CH3CO2H, M = 60 g mol–1, Ka = 1,8 x 10–5, pKa = 4,74) / acetato (NaCH3CO2, M = 82 g mol–1) é bastante
utilizado quando se deseja fixar o pH do meio em faixa ácida.
Deseja-se preparar 250 mL de uma solução com pH = 5,74. Para tanto, foram adicionados 10,3 g de acetato de sódio no balão de 250 mL. Para se ter a solução de pH desejado, qual é o volume mais próximo de ácido acético glacial que deve ser adicionado no balão antes de preenchê-lo com água?
Dados: Ácido acético glacial: densidade = 1 g mL–1, pureza = 97%.
Deseja-se preparar 250 mL de uma solução com pH = 5,74. Para tanto, foram adicionados 10,3 g de acetato de sódio no balão de 250 mL. Para se ter a solução de pH desejado, qual é o volume mais próximo de ácido acético glacial que deve ser adicionado no balão antes de preenchê-lo com água?
Dados: Ácido acético glacial: densidade = 1 g mL–1, pureza = 97%.
Provas
Questão presente nas seguintes provas
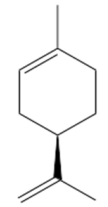
O limoneno, estrutura ilustrada a seguir, é o principal componente do óleo essencial das cascas de frutas cítricas e é utilizado como
fragrância na indústria alimentícia, solvente e precursor de outras moléculas. Ele possui um isômero, que tem propriedades
físicas – como temperatura de ebulição, densidade e índice de refração – idênticas à molécula ilustrada e que é comumente
associada em livros didáticos ao aroma de limão, enquanto a molécula desenhada seria responsável pelo aroma de tangerina. No
entanto, um artigo no Journal of Chemical Education de 2021 afirma que essa informação deriva da repetida citação de uma
publicação de 1971, que não se comprova experimentalmente.
Kvittingen, L. Sjursnes, B.J., Schmid, R. Limonene in Citrus: A String of Unchecked Literature Citings? J. Chem. Educ. 2021, 98, 11, 3600–3607. Disponível
em https://doi.org/10.1021/acs.jchemed.1c00363.
Provas
Questão presente nas seguintes provas
O limoneno, estrutura ilustrada a seguir, é o principal componente do óleo essencial das cascas de frutas cítricas e é utilizado como
fragrância na indústria alimentícia, solvente e precursor de outras moléculas. Ele possui um isômero, que tem propriedades
físicas – como temperatura de ebulição, densidade e índice de refração – idênticas à molécula ilustrada e que é comumente
associada em livros didáticos ao aroma de limão, enquanto a molécula desenhada seria responsável pelo aroma de tangerina. No
entanto, um artigo no Journal of Chemical Education de 2021 afirma que essa informação deriva da repetida citação de uma
publicação de 1971, que não se comprova experimentalmente.

Kvittingen, L. Sjursnes, B.J., Schmid, R. Limonene in Citrus: A String of Unchecked Literature Citings? J. Chem. Educ. 2021, 98, 11, 3600–3607. Disponível
em https://doi.org/10.1021/acs.jchemed.1c00363.
Provas
Questão presente nas seguintes provas
A alta demanda por cobre, impulsionada pela eletrificação de carros e intensa produção de componentes eletrônicos,
tem criado escassez do material e alta de preços. A obtenção de cobre metálico a partir de seu minério não requer
grande quantidade de energia e pode ser alcançada pela redução do seu óxido por monóxido de carbono. A redução
de óxido de cobre (II) passa pelo intermediário óxido de cobre (I) até chegar a cobre metálico. Considere as seguintes
equações químicas e correspondentes entalpias de reação:
2 Cu + ½ O2 → Cu2O ΔH = −170 kJ Cu2O + ½ O2 → 2 CuO ΔH = 16 kJ CO + ½ O2 → CO2 ΔH = −283 kJ
Utilizando monóxido de carbono como redutor, qual é o valor de entalpia mais próximo para a redução de 1 mol de óxido de cobre (II) a cobre?
2 Cu + ½ O2 → Cu2O ΔH = −170 kJ Cu2O + ½ O2 → 2 CuO ΔH = 16 kJ CO + ½ O2 → CO2 ΔH = −283 kJ
Utilizando monóxido de carbono como redutor, qual é o valor de entalpia mais próximo para a redução de 1 mol de óxido de cobre (II) a cobre?
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container