Foram encontradas 405 questões.
A Organização das Nações Unidas para a Educação, a Ciência e a Cultura − UNESCO − e a União Internacional de Química Pura e Aplicada − IUPAC − decidiram celebrar 2011 como o Ano Internacional da Química, com objetivo de "destacar as conquistas e avanços da Química e o papel das mulheres nesta ciência". A Escolha deste ano é também uma homenagem à cientista Marie Curie, agraciada com o Prêmio Nobel de Física em 1903, pela descoberta da radioatividade, e agraciada com o Prêmio Nobel de Química de 1911, pela descoberta dos elementos químicos rádio e polônio. Sobre a radioatividade e seu amplo uso em nossa sociedade moderna, indique a opção incorreta.
Provas
C(s) + CO2(g)É(São) correta(s) apenas a(s) assertativa(s)2CO(g) ΔH = + 174 KJ/mol
I. A constante de equilíbrio dessa reação expressa em termos de concentração é Kc = [CO]2 /[CO2].[C]
II. Segundo o princípio de Le Chatelier, se for adicionado mais C(s) no meio reacional, o equilíbrio irá se deslocar no sentido da formação de CO.
III. O aumento da temperatura favorece a formação de CO.
IV. A adição de um catalisador não influencia no estado de equilíbrio dessa reação, pois o catalisador aumenta simultaneamente as velocidades das reações direta e inversa, diminuindo as energias de ativação de ambas as reações.
Provas
Cl2 (g) + CO (g) → COCl2 (g)Considere, para isto, os seguintes dados experimentais coletados a uma dada temperatura:
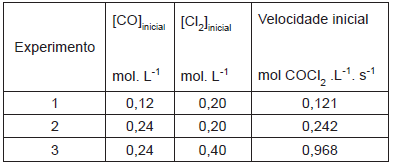
Provas
Cl- + O3 → ClO- + O2 (Etapa 1)Em relação à atuação do catalisador e o mecanismo acima, julgue os itens a seguir.
ClO- + O- → Cl- + O2 (Etapa 2)
I. O radical Cl- é o catalisador da reação, portanto ele altera a cinética da reação, deslocando o equilíbrio no sentido da formação dos produtos.É(São) correta(s) a(s) assertiva(s)
II. O radical ClO- é o intermediário da reação.
III. A lei da velocidade da reação de decomposição do ozônio é v = k[O3][ O-][ ClO-].
Provas
Fe3O4(s) + 2 C(s) → 3 Fe(s) + 2 CO2(g)Dados:
ΔHfº (Fe3O4) = - 1118KJ.mol-1 ΔHfº (CO2) = - 394KJ.mol-1
Sº (Fe3O4) = 146J.mol-1.K-1 Sº(C) = 6 J.mol-1.K-1
Sº (Fe) = 27 J.mol-1.K-1 Sº (CO2) = 214 J.mol-1.K-1
Provas
O gás metano (CH4) é um gás incolor e, quando adicionado ao ar, transforma-se em mistura de alto teor inflamável. É também chamado de biogás, pois pode ser produzido pela digestão anaeróbica de matéria orgânica, como lixo e esgoto, através de microrganismos. Portanto, o gás metano pode representar um perigo à segurança pública, como no caso informado há alguns meses sobre acumulação desse gás no subsolo de um shopping em São Paulo, construído sob um depósito de lixo. A partir das reações (A), (B) e (C), indique qual o valor da variação de entalpia da reação de combustão parcial do metano.
CH4(g) + 3/2 O2(g) → CO(g) + 2 H2O(g)(A) CH4(g) + 2 O2(g) → CO2(g) + 2 H2O(g) ΔHº = - 802,0 KJ
(B) CH4(g) + CO2(g) → 2 CO(g) + 2 H2(g) ΔHº = + 247,0 KJ
(C) CH4(g) + H2O(g) → CO(g) + 3 H2(g) ΔHº = + 206,0 KJ
Provas
I. Entalpia (H) é uma função de estado que mede a quantidade de calor absorvido ou liberado em qualquer transformação.É(São) correta(s) apenas a(s) assertiva(s)
II. Entropia (S) é uma função de estado que mede o grau de desordem dos diferentes estados da matéria em uma transformação espontânea.
III. A variação de energia livre de Gibbs (ΔG) é uma medida da entropia total de um sistema, quando a temperatura e a pressão são constantes. As transformações espontâneas, nessas condições, são acompanhadas pelo aumento da energia livre.
IV. Sabendo que a variação de energia livre de Gibbs (ΔG) é dada pela expressão ΔG= ΔH − TΔS, uma transformação exotérmica (ΔH<0) acompanhada pela diminuição da entropia (ΔS<0) não pode ser espontânea.
Provas
Provas
Tabela 1. Resultados da análise de amostras de água do rio Quilombo coletadas em 13 de outubro de 2005. NMP = número máximo permissível.
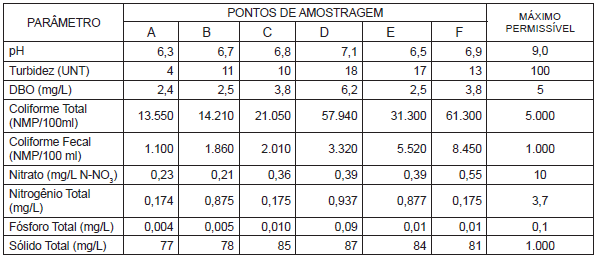
Provas
KAlSi3O8 (feldspato-K) + 8H2O = Al(OH)3 (gibbsita) + 3H4SiO4 + K+ + OH-
Essa reação é conhecida como
Provas
Caderno Container