Foram encontradas 376 questões.
Julgue o item subsequente, acerca da operação de sedimentação.
De acordo com a lei de Kynch, que rege a operação de sedimentação, a velocidade de sedimentação de uma partícula isolada é função de sua viscosidade e de seu diâmetro.
De acordo com a lei de Kynch, que rege a operação de sedimentação, a velocidade de sedimentação de uma partícula isolada é função de sua viscosidade e de seu diâmetro.
Provas
Questão presente nas seguintes provas
Julgue o item seguinte, a respeito dos medidores de vazão.
O tubo de Venturi clássico de seção circular apresenta três partes importantes: o cone de entrada, destinado a aumentar progressivamente a velocidade do fluido; a parte intermediária cilíndrica, onde se faz a medição de alta pressão; e o cone de saída, que aumenta progressivamente a velocidade do fluido.
O tubo de Venturi clássico de seção circular apresenta três partes importantes: o cone de entrada, destinado a aumentar progressivamente a velocidade do fluido; a parte intermediária cilíndrica, onde se faz a medição de alta pressão; e o cone de saída, que aumenta progressivamente a velocidade do fluido.
Provas
Questão presente nas seguintes provas
O cloro, o ácido nítrico e o ácido sulfúrico são compostos inorgânicos bastante utilizados na indústria química para a preparação de outros compostos inorgânicos e orgânicos comercialmente importantes, como PVC (policloreto de vinila) e fertilizantes, e no refino do petróleo, para remover impurezas da gasolina e de outros óleos. Com referência aos processos de produção dos compostos inorgânicos cloro, ácido nítrico e ácido sulfúrico, julgue o item que se segue.
No processo de produção de ácido sulfúrico, utiliza-se como matéria-prima para a obtenção do o enxofre, que sofre um processo de combustão no qual são utilizados como agentes comburentes o oxigênio puro ou o ar seco. A utilização de ar seco proporciona ao meio reacional uma temperatura maior que a obtida ao se utilizar oxigênio puro.
o enxofre, que sofre um processo de combustão no qual são utilizados como agentes comburentes o oxigênio puro ou o ar seco. A utilização de ar seco proporciona ao meio reacional uma temperatura maior que a obtida ao se utilizar oxigênio puro.
No processo de produção de ácido sulfúrico, utiliza-se como matéria-prima para a obtenção do
 o enxofre, que sofre um processo de combustão no qual são utilizados como agentes comburentes o oxigênio puro ou o ar seco. A utilização de ar seco proporciona ao meio reacional uma temperatura maior que a obtida ao se utilizar oxigênio puro.
o enxofre, que sofre um processo de combustão no qual são utilizados como agentes comburentes o oxigênio puro ou o ar seco. A utilização de ar seco proporciona ao meio reacional uma temperatura maior que a obtida ao se utilizar oxigênio puro.Provas
Questão presente nas seguintes provas
No que se refere a mecanismos de troca de calor, julgue o item a seguir.
Os valores típicos para o coeficiente de troca de calor por convecção forçada, em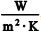 , estão na faixa de dezenas a centenas para gases e de centenas a milhares para líquidos.
, estão na faixa de dezenas a centenas para gases e de centenas a milhares para líquidos.
Os valores típicos para o coeficiente de troca de calor por convecção forçada, em
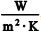 , estão na faixa de dezenas a centenas para gases e de centenas a milhares para líquidos.
, estão na faixa de dezenas a centenas para gases e de centenas a milhares para líquidos.Provas
Questão presente nas seguintes provas
O 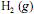 , obtido como subproduto da eletrólise do
, obtido como subproduto da eletrólise do 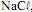 , é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno
, é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno 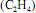 , representada pela seguinte
, representada pela seguinte
equação:
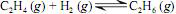
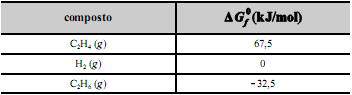
A tabela seguinte contém as energias livres de Gibbs padrão de formação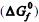 a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.
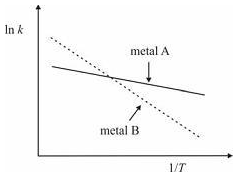
O gráfico a seguir mostra o ln da constante de velocidade da referida reação (k) em função do inverso da temperatura (1/T) para a reação catalisada por dois diferentes metais.
Considerando que as reações de hidrogenação sejam exotérmicas, que todos os gases envolvidos apresentem comportamento ideal e que o produto da constante universal dos gases pela temperatura absoluta (R×T) seja igual a 2.500 J/mol, julgue o item que se segue.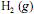 , obtido como subproduto da eletrólise do
, obtido como subproduto da eletrólise do 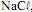 , é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno
, é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno 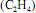 , representada pela seguinte
, representada pela seguinteequação:
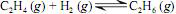
A tabela seguinte contém as energias livres de Gibbs padrão de formação
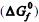 a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.
O gráfico a seguir mostra o ln da constante de velocidade da referida reação (k) em função do inverso da temperatura (1/T) para a reação catalisada por dois diferentes metais.

Considere que a reação de hidrogenação em apreço seja de ordem um com relação ao
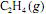 e de ordem um com relação ao
e de ordem um com relação ao 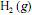 , e que as concentrações iniciais de cada um dos dois reagentes sejam iguais a
, e que as concentrações iniciais de cada um dos dois reagentes sejam iguais a  . Nessas condições, a concentração de
. Nessas condições, a concentração de  em um instante t da reação é dada por
em um instante t da reação é dada por 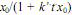 , em que k' é a constante de velocidade na temperatura da reação.
, em que k' é a constante de velocidade na temperatura da reação.Provas
Questão presente nas seguintes provas
O 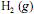 , obtido como subproduto da eletrólise do
, obtido como subproduto da eletrólise do 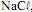 , é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno
, é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno 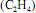 , representada pela seguinte
, representada pela seguinte
equação:
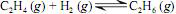
A tabela seguinte contém as energias livres de Gibbs padrão de formação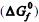 a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.

O gráfico a seguir mostra o ln da constante de velocidade da referida reação (k) em função do inverso da temperatura (1/T) para a reação catalisada por dois diferentes metais.

Considerando que as reações de hidrogenação sejam exotérmicas, que todos os gases envolvidos apresentem comportamento ideal e que o produto da constante universal dos gases pela temperatura absoluta (R×T) seja igual a 2.500 J/mol, julgue o item que se segue.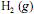 , obtido como subproduto da eletrólise do
, obtido como subproduto da eletrólise do 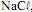 , é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno
, é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno 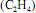 , representada pela seguinte
, representada pela seguinteequação:
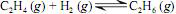
A tabela seguinte contém as energias livres de Gibbs padrão de formação
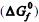 a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.
O gráfico a seguir mostra o ln da constante de velocidade da referida reação (k) em função do inverso da temperatura (1/T) para a reação catalisada por dois diferentes metais.

A energia de ativação da reação de hidrogenação catalisada pelo metal B é superior à da reação catalisada pelo metal A.
Provas
Questão presente nas seguintes provas
O 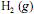 , obtido como subproduto da eletrólise do
, obtido como subproduto da eletrólise do 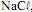 , é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno
, é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno 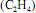 , representada pela seguinte
, representada pela seguinte
equação:
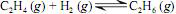
A tabela seguinte contém as energias livres de Gibbs padrão de formação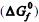 a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.

O gráfico a seguir mostra o ln da constante de velocidade da referida reação (k) em função do inverso da temperatura (1/T) para a reação catalisada por dois diferentes metais.

Considerando que as reações de hidrogenação sejam exotérmicas, que todos os gases envolvidos apresentem comportamento ideal e que o produto da constante universal dos gases pela temperatura absoluta (R×T) seja igual a 2.500 J/mol, julgue o item que se segue.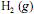 , obtido como subproduto da eletrólise do
, obtido como subproduto da eletrólise do 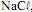 , é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno
, é largamente empregado na indústria em reações de hidrogenação, como a que ocorre com o eteno 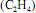 , representada pela seguinte
, representada pela seguinteequação:
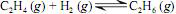
A tabela seguinte contém as energias livres de Gibbs padrão de formação
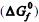 a 25 ºC de cada composto envolvido.
a 25 ºC de cada composto envolvido.
O gráfico a seguir mostra o ln da constante de velocidade da referida reação (k) em função do inverso da temperatura (1/T) para a reação catalisada por dois diferentes metais.

A constante de equilíbrio para a reação de hidrogenação do
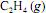 a 100 ºC é maior que a 25 ºC.
a 100 ºC é maior que a 25 ºC.Provas
Questão presente nas seguintes provas
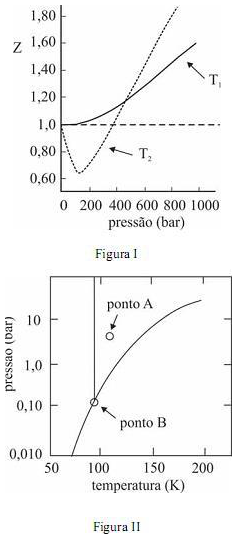
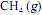 em função da pressão para duas temperaturas distintas (T1 eT2 ) e a figura II representa o diagrama de fases desse mesmo composto. A partir das figuras apresentadas, julgue o item que se segue.
em função da pressão para duas temperaturas distintas (T1 eT2 ) e a figura II representa o diagrama de fases desse mesmo composto. A partir das figuras apresentadas, julgue o item que se segue.Na temperatura e pressão correspondentes ao ponto A da figura II, o potencial químico do metano gasoso é superior ao do metano líquido.
Provas
Questão presente nas seguintes provas

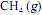 em função da pressão para duas temperaturas distintas (T1 eT2 ) e a figura II representa o diagrama de fases desse mesmo composto. A partir das figuras apresentadas, julgue o item que se segue.
em função da pressão para duas temperaturas distintas (T1 eT2 ) e a figura II representa o diagrama de fases desse mesmo composto. A partir das figuras apresentadas, julgue o item que se segue.O CH4 não pode ser liquefeito por simples compressão à temperatura de 150 K, uma vez que o ponto B, na figura II, corresponde à temperatura crítica desse gás.
Provas
Questão presente nas seguintes provas

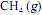 em função da pressão para duas temperaturas distintas (T1 eT2 ) e a figura II representa o diagrama de fases desse mesmo composto. A partir das figuras apresentadas, julgue o item que se segue.
em função da pressão para duas temperaturas distintas (T1 eT2 ) e a figura II representa o diagrama de fases desse mesmo composto. A partir das figuras apresentadas, julgue o item que se segue.Infere-se da situação mostrada na figura I que T1 é maior que T2.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container