Foram encontradas 120 questões.
Uma das propriedades fundamentais da matéria é a carga elétrica. A carga elétrica pode ser transferida de um corpo a outro e é sempre conservada. A respeito das propriedades relacionadas às cargas elétricas, julgue os itens seguintes.
Em um sistema de cargas eletricamente neutro, não existem linhas de força.
Provas
Aproximadamente 140 milhões de toneladas de gás amoníaco são produzidos anualmente pelo processo de Haber, que combina nitrogênio retirado do ar com gás hidrogênio, conforme representa a equação não-balanceada a seguir. O gás amoníaco é matéria-prima para a produção de ácido nítrico e NH4NO3, este último empregado como fertilizante e explosivo.
!$ N_2(g) + H_2(g) \rightleftharpoons NH_3(g) !$
Considerando as informações acima e sabendo que M(H) = 1 g/mol e M(N) = 14 g/mol, julgue o item a seguir.
Borbulhando-se NH3 em água, a solução resultante forma um ácido de Arrhenius.
Provas
A sequência de equações parciais de I a V, a seguir, indicam a formação da salmoura — equação I e II —, a eletrólise da solução e a obtenção de hidróxido de sódio como subproduto.
I !$ Na C \ell(s) \overset{água} { \rightarrow} Na^+(aq) + C \ell^- (aq) !$
II !$ H_2 O ( \ell) \rightarrow H^+(aq) + OH^- (aq) !$
III reação anódica: !$ 2 C \ell^- (aq) - 2e^- \rightarrow 2[C \ell] \rightarrow C \ell_2(g) !$
IV reação catódica: !$ 2 H^+ (aq) + 2e^- \rightarrow 2[H] \rightarrow H_2(g) !$
V !$ Na^+(aq) + OH^- \overset{evaporação} {(aq) \rightarrow} Na OH(s) !$
Considerando as informações acima, julgue o item a seguir.
As equações I e II representam, respectivamente, a ionização do cloreto de sódio e a dissociação da água.
Provas
A sequência de equações parciais de I a V, a seguir, indicam a formação da salmoura — equação I e II —, a eletrólise da solução e a obtenção de hidróxido de sódio como subproduto.
I !$ Na C \ell(s) \overset{água} { \rightarrow} Na^+(aq) + C \ell^- (aq) !$
II !$ H_2 O ( \ell) \rightarrow H^+(aq) + OH^- (aq) !$
III reação anódica: !$ 2 C \ell^- (aq) - 2e^- \rightarrow 2[C \ell] \rightarrow C \ell_2(g) !$
IV reação catódica: !$ 2 H^+ (aq) + 2e^- \rightarrow 2[H] \rightarrow H_2(g) !$
V !$ Na^+(aq) + OH^- \overset{evaporação} {(aq) \rightarrow} Na OH(s) !$
Considerando as informações acima, julgue o item a seguir.
A reação anódica é de redução.
Provas
Até meados do século XIX, as cirurgias eram realizadas sem anestesia, às vezes com a administração de quantidades apreciáveis de álcool, justificada pela crença de que o paciente ficaria entorpecido. Em 1846, William Morton conseguiu demonstrar que o éter dietílico podia ser usado para produzir inconsciência temporária durante os procedimentos cirúrgicos. Um problema dessa prática era o fato de o éter formar com o oxigênio do ar uma mistura explosiva, e qualquer choque entre os instrumentos metálicos cirúrgicos podia resultar em uma centelha e consequentemente em ignição. Outra substância usada como anestésico, o clorofórmio !$ H CC \ell_3 !$ 3 foi considerado melhor que o éter, pois a recuperação era mais rápida e menos desagradável. No entanto, alguns pacientes morriam; apesar disso, os riscos associados eram considerados pequenos. A partir de 1857, o clorofórmio tornou-se o anestésico preferido para os partos sem dor, na Europa e nos Estados Unidos. Atualmente, o clorofórmio não é mais usado para tal fim.
Acerca das substâncias citadas no texto, julgue o item a seguir.
O clorofórmio pertence à classe dos haletos de alquila.
Provas
A sequência de equações parciais de I a V, a seguir, indicam a formação da salmoura — equação I e II —, a eletrólise da solução e a obtenção de hidróxido de sódio como subproduto.
I !$ Na C \ell(s) \overset{água} { \rightarrow} Na^+(aq) + C \ell^- (aq) !$
II !$ H_2 O ( \ell) \rightarrow H^+(aq) + OH^- (aq) !$
III reação anódica: !$ 2 C \ell^- (aq) - 2e^- \rightarrow 2[C \ell] \rightarrow C \ell_2(g) !$
IV reação catódica: !$ 2 H^+ (aq) + 2e^- \rightarrow 2[H] \rightarrow H_2(g) !$
V !$ Na^+(aq) + OH^- \overset{evaporação} {(aq) \rightarrow} Na OH(s) !$
Considerando as informações acima, julgue o item a seguir.
As etapas III e IV do processo são não espontâneas e, por isso, é necessário utilizar uma fonte externa de corrente elétrica para que as reações ocorram.
Provas
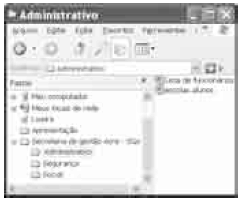
A figura acima mostra uma janela do Windows Explorer, executada em um computador cujo sistema operacional é o Windows XP. Com relação a essa figura, julgue o item a seguir.
A pasta ![]() é uma subpasta da pasta
é uma subpasta da pasta ![]() .
.
Provas
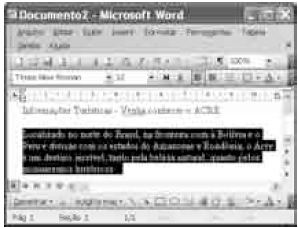
Com base na figura acima, julgue o item que se segue com relação ao Word 2003.
Considerando-se que a impressora padrão esteja configurada corretamente, para se imprimir o texto é suficiente clicar a ferramenta ![]() .
.
Provas

Com base na figura acima, julgue o item que se segue com relação ao Word 2003.
O parágrafo selecionado está formatado com alinhamento justificado.
Provas

Com base na figura acima, julgue o item que se segue com relação ao Word 2003.
O título do texto pode ser formatado com borda utilizando-se a ferramenta ![]()
Provas
Caderno Container