Foram encontradas 100 questões.
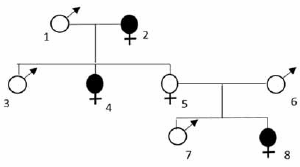
O heredograma anterior refere-se a uma característica controlada por um par de genes com dominância. Os símbolos escuros representam indivíduos que exibem o distúrbio ligado à característica recessiva. Em relação a esse heredograma e ao par de genes mostrado, assinale a opção correta.
Provas
Na interfase, que é definida como o espaço de tempo em que a célula não está se dividindo,
Provas
Considerando-se as características de uma hemácia, de uma célula do pâncreas de um ser humano e de uma célula do parênquima foliar de um arbusto, julgue os itens que se seguem.
I A hemácia não possui retículo endoplasmático e mitocôndria.
II As mitocôndrias não estão presentes na célula do parênquima foliar.
III Todas possuem membrana plasmática, DNA e mitocôndria.
IV Todas possuem membrana plasmática, DNA e ribossomo.
Assinale a opção correta.
Provas
No que se refere ao desenvolvimento embrionário humano, assinale a opção correta.
Provas
Em um ser humano adulto saudável, estima-se que a água seja responsável por 60% do total de sua massa corporal, e a maior parte dessa água localiza-se
Provas
Em algumas regiões brasileiras, o café faz parte de todas as refeições e uma das maneiras de prepará-lo é colocar a água no fogo juntamente com açúcar e o pó, até que seja formada a mistura desses componentes. Para que seja ingerido, basta passála pelo coador.
Considerando o preparo do café conforme essa descrição, assinale a opção correta.
Provas
Recentemente, um britânico de 23 anos de idade morreu por overdose de cafeína (C8H10N4O2). Na necropsia, foi constatado que havia o equivalente a 70 latas de energético em seu organismo, sendo a dose de cafeína em cada lata equivalente a 30 mg.
Com base nessa situação e considerando-se \( M_{C_{8}H_{10} N_{4} O_{2}} = 194,19 g/mol \) a massa molar da cafeína e \( N_A = 6 \times 10^{23} mol^{-1} \), a constante de Avogadro, é correto concluir que o número de moléculas de cafeína ingeridas pelo britânico é
Provas
Considerando-se que, para titular completamente 10 mL de uma solução de ácido sulfúrico (H2SO4), tenham sido utilizados 15 mL de uma solução 1,2 mol/L de hidróxido de sódio (NaOH), conclui-se que a concentração em quantidade de matéria do ácido sulfúrico na solução analisada seria igual a
Provas
A reação de decomposição da amônia (NH3) pode produzir hidrazina (N2H4) e gás hidrogênio (H2), conforme a equação química que se segue.
\( 2\,\,NH_{3(g)} \rightarrow N_2 H_{4(I)} + H_{2(g)} \)
Essa reação ocorreu a partir de 0,07 m3 de uma mistura gasosa que possui 70% em massa de amônia e cuja densidade é 0,9 g/L. A eficiência do processo foi de 65% e foram observadas as seguintes reações químicas e respectivas variações de entalpia (ΔHn, em que n = 1 ou 2):
\( N_{2(g)} + 2\,H_{2(g)} \rightarrow N_2 H_{4(I)}\,\,\,\,\,\triangle H_1 + 51 KJ/mol\\N_{2(g)} + 3\,\,H_{2(g)}\rightarrow 2\,,\,NH_{3(g)}\,\,\,\triangle\,H_2 = -92 KJ /mol \)
Nessa situação hipotética, considerando-se que \( M_{N_{2H_4}} = 32\,g/mol \) e \( M_{NH_{3}} = 17\,g/mol \) sejam as massas molares da hidrazina e da amônia, respectivamente, a variação de entalpia envolvida na quebra da amônia, caso o rendimento da reação tivesse sido de 100%, seria
Provas
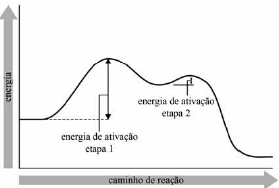
A partir das informações do gráfico precedente, que representa uma reação química genérica do tipo A + 2 B → AB2, processando-se com velocidade global constante, conclui-se que
Provas
Caderno Container