Foram encontradas 2.005 questões.
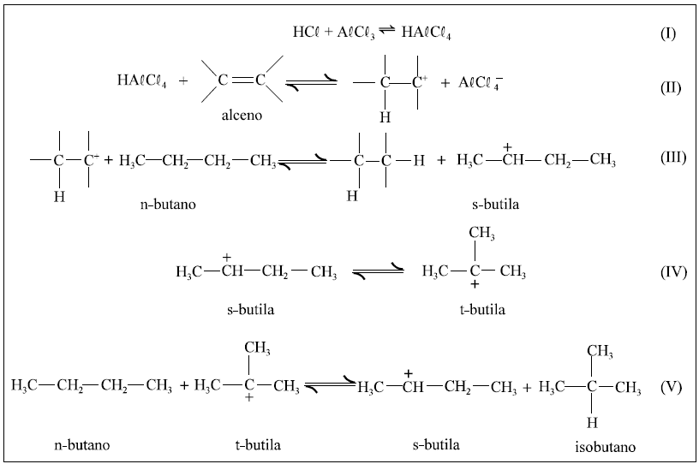
É bem conhecido o fato de que hidrocarbonetos mais ramificados resistem melhor à compressão, sem sofrer ignição espontânea, que hidrocarbonetos menos ramificados.Oíndice de octanagem de uma gasolina, por exemplo, reflete o teor de hidrocarbonetos ramificados presentes nessa gasolina. Gasolinas com alto índice de octanagem permitem à indústria automobilística construir pistões mais eficientes, capazes de trabalhar a compressões maiores. Por isso, a isomerização de alcanos é um processo importante na indústria do petróleo. Por intermédio dela, se produz alcanos ramificados a partir de alcanos nãoramificados. Para que essa reação ocorra, é necessário adicionar pequenas quantidades de HCR, ARCR3 e um alceno. As várias reações envolvidas na isomerização de n-butano em isobutano são mostradas no quadro ao lado.
Julgue o item a seguir, relativos às reações e intermediários mostrados no referido quadro.
O alceno é adicionado apenas para iniciar a reação. Uma vez iniciada, apenas as reações (IV) e (V) passam a ser importantes.
Provas
Uma semicélula A, consistindo em uma tira de manganês mergulhada em uma solução de Mn2+ (1 mol/L), e uma semicélula B, consistindo em uma tira de zinco mergulhada em uma solução de Zn2+ (1 mol/L), foram ligadas sucessivamente, eletricamente e por meio de ponte salina, a uma semicélula-padrão de hidrogênio a 25º C. As diferenças de potencial (ddp) medidas entre esta última e as semicélulas A e B foram de 1,18 V para a semicélula A e 0,76 V para a semicélula B. Emambos os casos, o eletrodo metálico—Mn e Zn— apresentou-se como pólo negativo.
Diante dessa situação hipotética e considerando que o produto 2,303RT/F —em que R é a constante universal dos gases, T é a temperatura de 298 K (25º C) e F é a constante de Faraday — seja igual a 0,06, julgue o item que se segue.
A constante de equilíbrio para a reação
Zn2+ (aq) + Mn (s) º Zn (s) + Mn2+ (aq)
é igual a 1,00 × 1014.
Provas
Uma semicélula A, consistindo em uma tira de manganês mergulhada em uma solução de Mn2+ (1 mol/L), e uma semicélula B, consistindo em uma tira de zinco mergulhada em uma solução de Zn2+ (1 mol/L), foram ligadas sucessivamente, eletricamente e por meio de ponte salina, a uma semicélula-padrão de hidrogênio a 25º C. As diferenças de potencial (ddp) medidas entre esta última e as semicélulas A e B foram de 1,18 V para a semicélula A e 0,76 V para a semicélula B. Emambos os casos, o eletrodo metálico—Mn e Zn— apresentou-se como pólo negativo.
Diante dessa situação hipotética e considerando que o produto 2,303RT/F —em que R é a constante universal dos gases, T é a temperatura de 298 K (25º C) e F é a constante de Faraday — seja igual a 0,06, julgue o item que se segue.
Sabendo que o Zn2+ (aq) forma um íon complexo na presença de hidróxido, Zn(OH)4 2!, caso houvesse a adição de hidróxido de sódio à semicélula B, a ddp entre ela e a semicélula-padrão de hidrogênio tornar-se-ia maior.
Provas
Uma semicélula A, consistindo em uma tira de manganês mergulhada em uma solução de Mn2+ (1 mol/L), e uma semicélula B, consistindo em uma tira de zinco mergulhada em uma solução de Zn2+ (1 mol/L), foram ligadas sucessivamente, eletricamente e por meio de ponte salina, a uma semicélula-padrão de hidrogênio a 25º C. As diferenças de potencial (ddp) medidas entre esta última e as semicélulas A e B foram de 1,18 V para a semicélula A e 0,76 V para a semicélula B. Emambos os casos, o eletrodo metálico—Mn e Zn— apresentou-se como pólo negativo.
Diante dessa situação hipotética e considerando que o produto 2,303RT/F —em que R é a constante universal dos gases, T é a temperatura de 298 K (25º C) e F é a constante de Faraday — seja igual a 0,06, julgue o item que se segue.
Ocorrerá uma reação perceptível quando o manganês metálico for mergulhado em uma solução de 1 mol/L de Zn2+.
Provas
Uma semicélula A, consistindo em uma tira de manganês mergulhada em uma solução de Mn2+ (1 mol/L), e uma semicélula B, consistindo em uma tira de zinco mergulhada em uma solução de Zn2+ (1 mol/L), foram ligadas sucessivamente, eletricamente e por meio de ponte salina, a uma semicélula-padrão de hidrogênio a 25º C. As diferenças de potencial (ddp) medidas entre esta última e as semicélulas A e B foram de 1,18 V para a semicélula A e 0,76 V para a semicélula B. Emambos os casos, o eletrodo metálico—Mn e Zn— apresentou-se como pólo negativo.
Diante dessa situação hipotética e considerando que o produto 2,303RT/F —em que R é a constante universal dos gases, T é a temperatura de 298 K (25º C) e F é a constante de Faraday — seja igual a 0,06, julgue o item que se segue.
Caso as semicélulas A e B sejam ligadas entre si, eletricamente e por meio de ponte salina, a tira de manganês será o catodo, a tira de zinco será o anodo e a diferença de potencial entre as duas será de +0,42 V.
Provas
Uma semicélula A, consistindo em uma tira de manganês mergulhada em uma solução de Mn2+ (1 mol/L), e uma semicélula B, consistindo em uma tira de zinco mergulhada em uma solução de Zn2+ (1 mol/L), foram ligadas sucessivamente, eletricamente e por meio de ponte salina, a uma semicélula-padrão de hidrogênio a 25º C. As diferenças de potencial (ddp) medidas entre esta última e as semicélulas A e B foram de 1,18 V para a semicélula A e 0,76 V para a semicélula B. Emambos os casos, o eletrodo metálico—Mn e Zn— apresentou-se como pólo negativo.
Diante dessa situação hipotética e considerando que o produto 2,303RT/F —em que R é a constante universal dos gases, T é a temperatura de 298 K (25º C) e F é a constante de Faraday — seja igual a 0,06, julgue o item que se segue.
Entre as espécies químicas Mn (s), Mn2+ (aq), Zn (s) e Zn2+ (aq), esta última é o redutor mais forte e Mn (s) é o oxidante mais forte.
Provas
O planeta Aragonose é formado basicamente pelo mineral aragonita (CaCO3). Sua atmosfera possui 1010 L de volume e contém metano e dióxido de carbono, cada qual exercendo uma pressão parcial de 0,10 atm. Seus oceanos são formados de água líquida saturada com aragonita, em que o íon H3O+ está presente em uma concentração de 1,8 × 10-7 mol/L. A temperatura média do planeta é de +5º C (278 K).
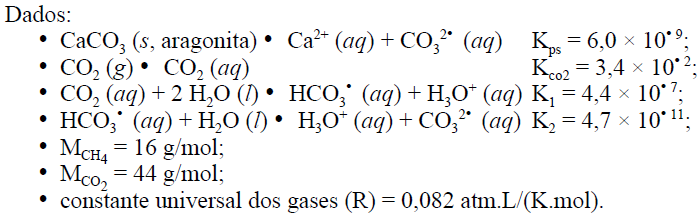
Considerando a situação hipotética e os dados apresentados acima, em que K denota a constante de equilíbrio da reação mostrada, julgue o item a seguir.
Umlitro da água do mar de Aragonose contém menos de 0,1 g de Ca2+.
Provas
O planeta Aragonose é formado basicamente pelo mineral aragonita (CaCO3). Sua atmosfera possui 1010 L de volume e contém metano e dióxido de carbono, cada qual exercendo uma pressão parcial de 0,10 atm. Seus oceanos são formados de água líquida saturada com aragonita, em que o íon H3O+ está presente em uma concentração de 1,8 × 10-7 mol/L. A temperatura média do planeta é de +5º C (278 K).
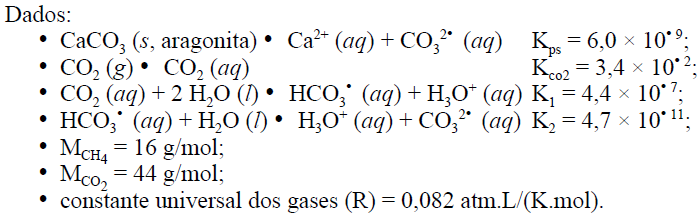
Considerando a situação hipotética e os dados apresentados acima, em que K denota a constante de equilíbrio da reação mostrada, julgue o item a seguir.
Se houvesse uma bactéria nos oceanos de Aragonose que produzisse CO2, o pH da água desses oceanos aumentaria.
Provas
O planeta Aragonose é formado basicamente pelo mineral aragonita (CaCO3). Sua atmosfera possui 1010 L de volume e contém metano e dióxido de carbono, cada qual exercendo uma pressão parcial de 0,10 atm. Seus oceanos são formados de água líquida saturada com aragonita, em que o íon H3O+ está presente em uma concentração de 1,8 × 10-7 mol/L. A temperatura média do planeta é de +5º C (278 K).
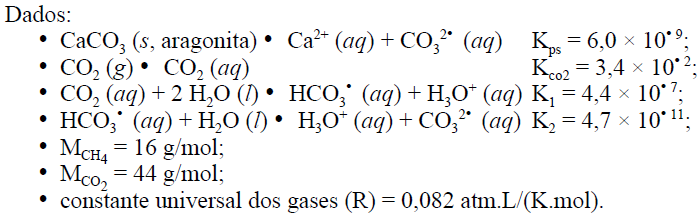
Considerando a situação hipotética e os dados apresentados acima, em que K denota a constante de equilíbrio da reação mostrada, julgue o item a seguir.
A molaridade do gás metano na atmosfera de Aragonose é superior a 0,005 mol/L.
Provas
O planeta Aragonose é formado basicamente pelo mineral aragonita (CaCO3). Sua atmosfera possui 1010 L de volume e contém metano e dióxido de carbono, cada qual exercendo uma pressão parcial de 0,10 atm. Seus oceanos são formados de água líquida saturada com aragonita, em que o íon H3O+ está presente em uma concentração de 1,8 × 10-7 mol/L. A temperatura média do planeta é de +5º C (278 K).
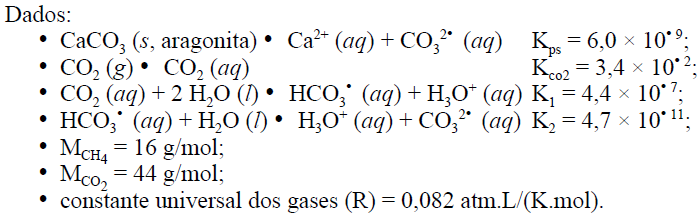
Considerando a situação hipotética e os dados apresentados acima, em que K denota a constante de equilíbrio da reação mostrada, julgue o item a seguir.
A massa de gás metano na atmosfera de Aragonose é superior a 1.000 ton.
Provas
Caderno Container