Foram encontradas 280 questões.
Um perito criminal encontrou em uma cena de crime duas amostras desconhecidas. Essas amostras foram analisadas e as substâncias identificadas foram descritas como cocaína e morfina, apresentadas a seguir.
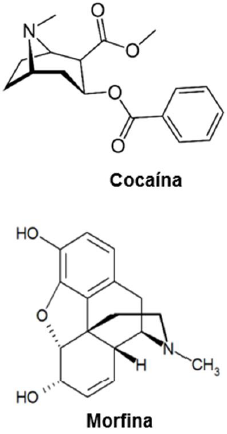
A partir das estruturas da cocaína e da morfina, assinale a alternativa que apresenta corretamente os grupos funcionais presentes em cada uma delas, respectivamente.
Provas
A síntese de amônia é realizada pelo processo conhecido como “Síntese de Haber-Bosch”, desenvolvido por Fritz Haber e Carl Bosch no início do século XX. O equilíbrio químico da síntese de amônia é representado a seguir:
3H2(g) + N2(g)\( \rightleftharpoons \) 2NH3(g) ΔH < 0
Sabendo que ΔH corresponde à variação de entalpia e com base nos conhecimentos sobre deslocamento de equilíbrio químico, assinale a alternativa que NÃO descreve uma mudança na condição desse equilíbrio para aumentar a produção de amônia.
Provas
A respeito do modelo atômico de Rutherford e seus experimentos, assinale a alternativa correta.
Provas
Na literatura são descritos principalmente três tipos de etilômetro que se baseiam em princípios diferentes para detectar a quantidade de álcool no ar alveolar exalado, a saber, bafômetros descartáveis (colorimétricos), detector eletroquímico (células eletroquímicas) e semicondutores (modelo Taguchi). Independentemente do princípio de funcionamento de cada dispositivo, todos se baseiam no princípio de que o álcool contido no sangue está em equilíbrio com o álcool contido no ar dos pulmões. O princípio de funcionamento dos bafômetros descartáveis é baseado em uma reação de oxirredução de acordo com a seguinte reação química:
2 K2Cr2O7 + 3 CH3CH2OH + 8 H2SO4 →
2 Cr2(SO4)3 + 2 K2SO4 + 3 CH3COOH + 11 H2O
Diante da reação apresentada e com base nos conhecimentos de nomenclatura de compostos e de reações de oxirredução, assinale a alternativa correta.
Provas
Acerca do caráter ácido e básico das substâncias orgânicas, analise as assertivas e assinale a alternativa que aponta a(s) correta(s).
I. Os ácidos carboxílicos apresentam caráter ácido e a força do ácido diminui com o aumento da cadeia carbônica, sendo assim, o ácido acético é um ácido mais forte que o ácido fórmico.
II. O ácido cloroacético é um ácido mais forte do que o ácido acético.
III. A ordem decrescente do caráter ácido para a classe de compostos orgânicos a seguir é: ácidos carboxílicos > fenóis > álcoois > alcanos.
IV. A amônia apresenta maior basicidade do que a fenilamina (anilina).
Provas
Considere a reação genérica descrita a seguir:
X + Y \( \rightarrow \) XY
Essa reação apresenta os seguintes dados experimentais de velocidade:
| Experimentos |
[X] (mol/L) |
[Y] (mol/L) |
Velocidade inicial (mol/L s-1) |
| 1 | 1,0 | 0,5 | 6,0 x 10-3 |
| 2 | 0,5 | 0,5 | 1,5 x 10 -3 |
| 3 | 0,5 | 1,0 | 3,0 x 10 -3 |
Assinale a alternativa que descreve corretamente a lei de velocidade e o valor da constante de velocidade para essa reação, respectivamente.
Provas
A talidomida é um fármaco que já foi muito utilizado como sedativo e como medicamento contra enjoos em mulheres no período de gestação. A estrutura da talidomida é representada a seguir.
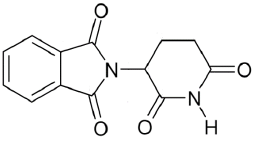
Com base nessa estrutura e acerca do conhecimento sobre estereoisomeria, assinale a alternativa que apresenta o número de enantiômeros possíveis para a talidomida.
Provas
As reações mais características de alcenos e alcinos são as reações de adição, nas quais um reagente é adicionado aos dois átomos que formam a ligação múltipla. Considere as diferentes reações de adição, para a molécula de etileno, descritas a seguir:
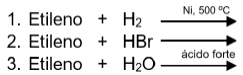
Considerando essas reações de adição, assinale a alternativa que apresenta, respectivamente, as substâncias formadas a partir das reações descritas em 1, 2 e 3.
Provas
A teoria da repulsão de pares de elétrons na camada de valência (VSEPR, do inglês "valence shell electron-pair repulsion") permite prever a geometria de moléculas. Acerca desse assunto, assinale a alternativa que apresenta a correta descrição da geometria molecular das seguintes moléculas: CH4, NH3 e SeCl4, respectivamente.
Provas
Dentre os combustíveis mais utilizados nos automóveis está a gasolina, cujo componente majoritário é o octano (C8H18). A equação química de combustão completa do octano (não balanceada) é representada a seguir:
C8H18(l) + O2(g) → CO2(g) + H2O(g)
Considerando a reação de combustão completa de 5,0 g de C8H18, assinale a alternativa que apresenta todos os coeficientes estequiométricos (na ordem da reação apresentada), como números inteiros, e a massa (gramas) de O2, respectivamente.
Provas
Caderno Container