Foram encontradas 372 questões.
Disciplina: Engenharia Ambiental e Sanitária
Banca: IOBV
Orgão: Pref. Araquari-SC
Provas
Provas
Disciplina: Legislação Estadual e Distrital
Banca: IOBV
Orgão: Pref. Araquari-SC
Provas
A obtenção de água doce de boa qualidade está cada vez mais difícil devido ao adensamento populacional, às mudanças climáticas, à expansão da atividade industrial e à poluição. A água, uma vez captada, precisa ser purificada, o que é feito nas estações de tratamento. Um esquema de tratamento de purificação é:
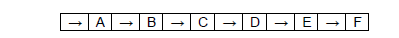
Onde as etapas B, D, e F são:
B – adição de sulfato de alumínio e óxido de cálcio;
D – filtração em areia;
F – fluoretação.
Assim sendo, assinale a alternativa correta em que as etapas A, C e E correspondem respectivamente.
Provas
A água potável proveniente de estações de tratamento resulta de um conjunto de procedimentos físicos e químicos que são aplicados na água para que esta fique em condições adequadas para o consumo. Esta separação é necessária uma vez que a água de rios ou lagoas apresenta muitos resíduos sólidos, por isso tem que passar por uma série de etapas para que esses resíduos sejam removidos. Neste processo de tratamento a água fica livre também de qualquer tipo de contaminação, evitando a transmissão de doenças. Em uma ETA (estação de tratamento de água) típica, a água passa pelas seguintes etapas: coagulação, floculação, decantação, filtração, desinfecção, fluoretação e correção de pH. Com relação às informações acima, analise as seguintes proposições:
I. Fluoretação: é quando se adiciona flúor na água, cuja finalidade é prevenir a formação de cárie dentária em crianças.
II. Floculação: ocorre em tanques de concreto, logo após a coagulação. Com a água em movimento, as partículas sólidas se aglutinam em flocos maiores.
III. Decantação: nesta etapa, que é posterior â coagulação e à floculação, por ação da gravidade, os flocos com as impurezas e partículas ficam depositados no fundo de outros tanques, separando-se da água. A etapa da decantação pode ser considerada um fenômeno físico.
IV. Filtração: é a etapa em que a água passa por filtros formados por carvão, areia e pedras de diversos tamanhos. Nesta etapa, as impurezas de tamanho pequeno ficam retidas no filtro. A etapa da filtração pode ser considerada um fenômeno químico.
V. Coagulação: é a etapa em que a água, na sua forma bruta, entra na ETA. Ela recebe, nos tanques, uma determinada quantidade de cloreto de sódio. Esta substância serve para aglomerar partículas sólidas que se encontram na água como, por exemplo, a argila.
VI. Desinfecção: é a etapa que cloro ou ozônio é aplicado na água para eliminar microorganismos causadores de doenças.
VII. Correção de pH: esse procedimento serve para corrigir o pH da água e preservar a rede de encanamentos de distribuição. Se a água está básica, é aplicada certa quantidade de cal hidratada ou carbonato de sódio.
Assinale a alternativa que contém somente proposições corretas:
Provas
Provas
Considerando as etapas de tratamento de água para consumo humano: coagulação, floculação, decantação, filtração, desinfecção, fluoretação e correção de pH. Na etapa de coagulação, a adição da cal, nome vulgar do óxido de cálcio, tem o objetivo de corrigir o pH para aumentar a eficiência no processo de floculação das partículas suspensas.
Sobre o fenômeno que ocorre nessa etapa, é correto afirmar que a cal reage com:
Provas
Provas
O cloreto de carbonilo gasoso decompõe-se, à temperatura T, em monóxido de carbono e cloro molecular. Este sistema gasoso atinge um estado de equilíbrio, para o qual as espécies têm as seguintes concentrações:
[COCl2] = 1,60 mol/dm3
[CO] = 0,40 mol/dm3
[Cl2] = 0,40 mol/dm3
O valor da constante de equilíbrio é:
Provas
Provas
Caderno Container