Foram encontradas 40 questões.
A reação química abaixo, não balanceada, representa a transformação da glicose em energia:
x C6H12O6 (s) + y O2 (g) ⟶ z CO2 (g) + w H2O(l) + energia
Considerar que x, y z e w sejam os menores números inteiros que fazem o correto balanceamento da reação. Considerar, também, a tabela abaixo que apresenta a entalpia padrão de formação, a 25°C, de alguns compostos.
| Entalpia padrão de formação a 25ºC | |
| Composto | ΔH (kJ/mol) |
| CO2 (g) | -394 |
| H2O(l) | - 286 |
| C6H12O6 (s) | -1.271 |
Dados: H = 1; C = 12; O = 16.
Qual é o valor da entalpia padrão de combustão da glicose, em kJ, a 25°C?
Provas
A reação química abaixo, não balanceada, representa a transformação da glicose em energia:
x C6H12O6 (s) + y O2 (g) ⟶ z CO2 (g) + w H2O(l) + energia
Considerar que x, y z e w sejam os menores números inteiros que fazem o correto balanceamento da reação. Considerar, também, a tabela abaixo que apresenta a entalpia padrão de formação, a 25°C, de alguns compostos.
| Entalpia padrão de formação a 25ºC | |
| Composto | ΔH (kJ/mol) |
| CO2 (g) | -394 |
| H2O(l) | - 286 |
| C6H12O6 (s) | -1.271 |
Dados: H = 1; C = 12; O = 16.
É CORRETO afirmar que:
Provas
Sobre o estudo cinético das reações químicas e assuntos correlatos, marcar C para as afirmativas Certas, E para as Erradas e, após, assinalar a alternativa que apresenta a sequência CORRETA:
(---) A lei de velocidade de uma reação química catalisada, que se processa na temperatura T e pressão P, mantidas constantes as concentrações dos demais reagentes, é igual àquela da mesma reação não catalisada.
(---) Os catalisadores são substâncias que diminuem a energia de ativação do complexo ativado. Desta forma, aumentam a velocidade da reação química.
(---) Em uma reação química, um dos produtos dessa reação pode ser o catalisador.
Provas
A tabela periódica dos elementos foi desenvolvida a partir da segunda metade do século XIX e é uma disposição sistemática dos elementos químicos em função de suas propriedades. Acerca da tabela periódica dos elementos, assinalar a alternativa INCORRETA:
Provas
Uma solução de ácido nítrico foi preparada a partir de 1,575g de ácido nítrico, com pureza de 100%, acrescentando-se água destilada até completar a marca do menisco de um balão volumétrico. Determinar o volume, em mL, do balão volumétrico, sabendo-se que ao final o pH da solução era igual a 2,0:
Dados: H = 1; N = 14; O = 16.
Provas
Deseja-se preparar 2.000mL de uma solução de NaNO3 em uma concentração igual a 5mol/L. Qual é, em gramas, a massa aproximada de NaNO3 necessária para o preparo dessa solução?
Dados: H = 1; N = 14; O = 16; Na = 23.
Provas
Uma das razões pelas quais as propriedades dos sistemas em equilíbrio são muito importantes é que todas as reações químicas tendem a alcançar um equilíbrio. A uma dada temperatura o valor da expressão da lei da ação das massas (Q) para uma certa reação em equilíbrio é uma constante.
Para o equilíbrio 2SO3(g) ↔ 2SO2(g) + O2(g), o valor da constante de equilíbrio (K) é 4,8 x 10-3 a 700°C. Se, em um recipiente, as concentrações das três substâncias forem: [SO3] = 0,5mol/litro, [SO2] = 0,2mol/litro e [O2] = 0,01mol/litro e mantendo-se a temperatura constante, fazem-se as seguintes afirmações:
I - Como o valor de Q é maior que K, a reação procede no sentido de aumentar a concentração dos produtos SO2 e O2.
II - Como o valor de Q é menor que K, a reação procede no sentido de aumentar a concentração dos produtos SO2 e O2.
III - Se a concentração inicial de O2 for 0,1mol/litro, a reação procede no sentido da direita para a esquerda.
Está(ão) CORRETO(S):
Provas
Um sistema com volume de 30 litros absorve 1,5kJ de calor. Calcular a variação de energia ΔU para o sistema se:
I) O calor for absorvido a volume constante.
II) O sistema expande para um volume de 35 litros, contra uma pressão constante de 1,5atm.
Observação: Considerar 1 atm.litro = 101,3J.
Assinalar a alternativa que apresenta os valores CORRETOS para as situações I e II, respectivamente:
Provas
O processo pelo qual uma solução-padrão é introduzida em meio reagente é conhecido por titulação, em que, sabendo-se a quantidade da solução-padrão necessária para reagir totalmente com a amostra e a reação química que ocorre entre as duas espécies, têm-se condições para se calcular a concentração da substância analisada. Sobre os procedimentos volumétricos para determinação da concentração de substâncias, marcar C para as afirmativas Certas, E para as Erradas e, após, assinalar a alternativa que apresenta a sequência CORRETA:
(---) Uma vez que o hidróxido de sódio não é um padrão primário, o biftalato de potássio é comumente utilizado para padronização desta solução.
(---) Segundo o método de Mohr para a determinação de cloretos, o haleto é titulado com uma solução-padrão de nitrato de prata usando-se cromato de potássio como indicador. Uma vez que a solução a ser titulada deve ser neutra e deve-se evitar pH muito alto, este é um bom processo para se determinar cloretos em soluções neutras ou não tamponadas.
(---) A figura abaixo pode representar a curva de titulação de um ácido fraco com uma base forte, uma vez que o pH no ponto de equivalência é maior que 7.
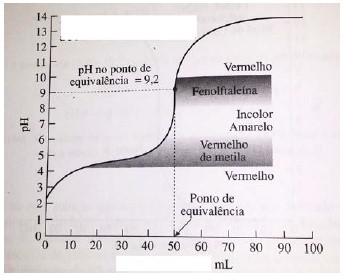
Provas
Para compreender o comportamento das moléculas e dos sólidos, necessita-se compreender os átomos. Sobre as estruturas atômicas, analisar os itens abaixo:
I - A alta abundância de ferro e de níquel no universo é consistente com o fato de eles serem os núcleos mais estáveis, ou seja, com maior energia de ligação.
II - Elétrons podem se comportar como partículas ou ondas. Uma consequência imediata da dualidade é a impossibilidade de se saber o momento linear e a localização de um elétron simultaneamente. Essa restrição é conteúdo do Princípio da Incerteza de Schrödinger, o qual formulou uma equação que levou em conta a dualidade onda-partícula e considerou o movimento dos elétrons nos átomos.
III - Para um conjunto de orbitais definido por n (número quântico principal) = 4 e l (número quântico momento angular orbital) = 1 existem três orbitais 4p.
Está(ão) CORRETO(S):
Provas
Caderno Container