Foram encontradas 1.037 questões.
Rubinho percorreu 40km a uma velocidade média de 20km/h e, a seguir, percorreu D km a uma velocidade média de 40km/h. Se, no total do percurso, Rubinho fez uma velocidade média de 25km/h, então o valor de D, em km, é aproximadamente
Provas
Seja !$ N !$ a solução da equação
!$ \log_9(\log_4N)=\log_{16}(\log_216) !$.
A soma dos algarismos de !$ N !$ é
Provas
Dois dados comuns, um azul e outro vermelho, são lançados. Sejam:
x, o número de maneiras diferentes de se obter soma 3.
y, o número de maneiras diferentes de se obter soma 6.
z, o número de maneiras diferentes de se obter soma 9.
É correto afirmar que
Provas
Uma função quadrática !$ f(x)=x^2+bx+c !$ tem um valor mínimo no ponto em que !$ x=-2 !$ e o seu gráfico passa pelo ponto !$ (−1, 3) !$. O valor de !$ f(1) !$ é:
Provas
Quatro irmãs têm idades diferentes, mas todas têm idades que são números de dois dígitos. O produto das idades de duas delas é 216 e o produto das idades das outras duas é 224. A soma das idades das quatro irmãs é:
Provas
A diferença de potencial (ddp) de uma célula galvânica é uma medida da habilidade da reação da célula de empurrar e puxar elétrons através de um circuito. Dessa forma, cada eletrodo contribui para esse valor através de seu potencial padrão (E0). Analise a tabela de potenciais padrão apresentada a seguir.
| Semi-Reação | E0 (V) |
| Fe+2(aq) + 2e → Fe0(s) | – 0,44 |
| Zn+2(aq) + 2e → Zn0(s) | – 0,76 |
| Pb+2(aq) + 2e → Pb0(s) | – 0,13 |
| Cu+2(aq) + 2e → Cu0(s) | + 0,34 |
| Ag+1(aq) + 1e → Ag0(s) | + 0,80 |
A célula com maior ddp será formada por
Provas
Um técnico de laboratório preparou uma solução aquosa de hidróxido de potássio, dissolvendo 2,80 g da base para 500 mL de solução. Uma alíquota de 10,0 mL dessa solução foi, então, diluída a um litro com água, formando uma nova solução.
O pH da solução diluída será igual a
Provas
A espontaneidade de uma transformação química pode ser predita a partir de seus parâmetros termodinâmicos.
Analise a tabela a seguir que contém os valores das variações de entalpia (ΔH) e entropia (ΔS) para três reações distintas (I, II e III).
| REAÇÃO | ΔH (kJ) | ΔS (J.K-1) |
| I. N2(g) + 3F2(g) → 2NF3(g) | – 249 | – 278 |
| II. N2(g) + 3C!$ \ell !$2(g) → 2NC!$ \ell !$3(g) | 460 | – 275 |
| III. N2F4(g) → 2NF2(g) | 85 | 198 |
A partir das informações, analise as afirmativas a seguir e assinale (V) para a verdadeira e (F) para a falsa.
( ) A reação I torna-se não espontânea a baixas temperaturas.
( ) A reação II é não espontânea a qualquer temperatura.
( ) A reação III torna-se espontânea a altas temperaturas.
As afirmativas são, na ordem apresentada, respectivamente,
Provas
O gengibre é uma planta herbácea muito apreciada na culinária por seu sabor e pungência. Diversos compostos químicos são responsáveis por essas características. Na forma desidratada (em pó) prevalece o 6-shogaol, cuja estrutura está representada a seguir.
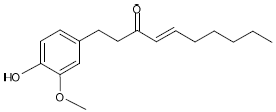
Assinale a opção que apresenta as funções orgânicas presentes na estrutura.
Provas
Anticongelantes são substâncias químicas capazes de fazer com que a temperatura de congelamento de um líquido diminua.
Ao se preparar uma solução aquosa contendo 25% em massa de um anticongelante X, verificou-se o abaixamento de 10ºC na temperatura de congelamento da água.
(Dado: constante de ponto de congelamento (Kc) da água = 1,86 ºC.mol.kg-1).
A fórmula química que melhor representa X é
Provas
Caderno Container