Foram encontradas 50 questões.
O gesso é um material aglomerante, obtido a partir da Gipsita, mineral abundante em terrenos cretáceos no Brasil, como o polo gesseiro do Araripe, estado de Pernambuco. Seu principal componente é o Sulfato de Cálcio di-hidratado. Por meio de calcinação, parte da água de hidratação é retirada e o mineral é moído para formar um pó, usado na construção civil e na medicina, entre muitas outras aplicações.
Quando se reidrata o Sulfato de Cálcio hemi-hidratado, com cerca de um terço de seu peso em água, ele volta ao seu estado di-hidratado.
Nesse processo, o gesso endurece em alguns minutos, em uma reação perceptivelmente exotérmica, vista abaixo:
CaSO4 . !$ ^1/_2 !$ H2O (s) + 3/2 H2O (liq) !$ \rightarrow !$ CaSO4 . 2 H2O (s) + Energia (Calor)
Analisando a variação de entalpia dessa reação:
!$ \Delta Hº_{Reação} \, = \, \Sigma \Delta Hº_{Produtos} \, - \, \Sigma \Delta Hº_{Reagentes} !$
!$ \Delta Hº_{Reação} \, = \, \Delta Hº_{CaSO4 \cdot 2H2O \, (s)} \, - \, \Delta Hº_{CaSO4 \cdot 1/2H2O \, (s)} \, - \, 3/2 \, \Delta Hº_{H2O \, (liq)} !$
!$ \Delta Hº_{Reação} \, = \, -2021,1 \, kJ.mol^{-1} \, - \, (-1575,2b \, kJ.mol^{-1}) \, - \, 3/2 \, (-285,83 \, kJ.mol^{-1}) !$
!$ \Delta Hº_{Reação} \, = \, -17,2 \, kJ.mol^{-1} !$
Um paciente, que teve a perna engessada para imobilização ortopédica, se queixou que o gesso esquentou muito enquanto endurecia. Pode-se estimar a temperatura máxima da peça de gesso assim que se endurece, com base nos dados de entalpia da reação acima, fazendo as seguintes considerações:
- A temperatura ambiente na sala ortopédica ficou estável em 21 °C, não se alterando enquanto o gesso foi aplicado e endureceu;
- A pressão não variou ao longo do processo de endurecimento do gesso e os valores de entalpia de cada substância não são dependentes da temperatura;
- Todo o calor liberado pela reação seria expresso no aumento de temperatura da peça de gesso !$ ([\Delta Hº_{Reação}] \, = \, \Delta Hº_{Aquecimento \,\, do \,\, Gesso).} !$
Assim, calculando com base na equação de Kirchhoff:
!$ n \, . \, [\Delta Hº_{Reação}] \, = \, n \, . \, Cp \, . \, \Delta T !$
Onde:
n = Número de moles
Cp = Capacidade Calorífica do Gesso = 186,2 Joules.K-1.mol-1
!$ \Delta !$T = Variação da Temperatura da peça de Gesso (Temperatura final ºK – Temperatura Inicial do Gesso ºK)
Dada a equação de conversão entre °K (kelvin) em °C (celsius):
°C = °K - 273,15
Depois de aplicar o cálculo, considerando que toda a energia térmica da reação fosse acumulada no gesso, com relação à temperatura do gesso, é correto afirmar que
Provas
Analise, abaixo, o diagrama simplificado dos vários tipos de fluxos de energia que entram e saem do planeta para responder à questão.
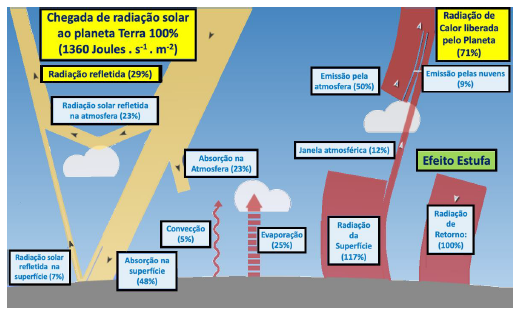
Ao analisar o diagrama, pode-se perceber que o efeito estufa, causado pelos gases da atmosfera, é fundamental para manter a temperatura dentro de valores capazes de sustentar as inúmeras formas de vida que se encontram em nosso planeta. Sem o efeito estufa, a temperatura média da Terra poderia ser 20 °C ou 30 °C mais baixa. Tal efeito acontece porque existe uma janela de transparência no espectro de absorção da mistura de gases da atmosfera que, por sua vez, permite a passagem da radiação eletromagnética UV/Visível. Uma vez incidindo sobre a superfície do planeta, essa energia será absorvida, usada em processos ligados à vida e retornada ao meio na forma de calor (radiação eletromagnética infravermelha). Acontece que essa radiação é reabsorvida pela própria atmosfera terrestre e só uma parte dela é devolvida ao espaço. O processo guarda parte do calor pela diferença de tempo entre a absorção e a liberação do calor, apesar de que o fluxo de energia eletromagnética vinda do Sol e devolvida ao espaço está em relativo equilíbrio. Esse equilíbrio nos mantém nessa média de temperaturas, adequadas à vida na Terra, por milênios sem grandes variações.
Sobre o assunto, é correto afirmar que o efeito estufa
Provas
Analise, abaixo, o diagrama simplificado dos vários tipos de fluxos de energia que entram e saem do planeta para responder à questão.

De acordo com medidas e cálculos desenvolvidos pela NASA em 2009, com base nos dados de satélites do projeto CERES, cerca de 1360 J s-1m-2 de energia solar chegam à alta atmosfera do planeta Terra. Esse é o mesmo valor de energia que o planeta retorna ao espaço, somando-se a reflexão de parte dessa radiação eletromagnética com o calor emitido pelo planeta de volta ao espaço. A radiação que chega é composta principalmente de frequências das bandas UV / Visível / Infravermelho Próximo e o calor irradiado desde a própria atmosfera e da superfície terrestre é composto maiormente pelos comprimentos de onda eletromagnéticos das bandas Infravermelho próximo e distante.
Pode-se dizer, então, que o fluxo de energia eletromagnética que chega na Terra vindo do Sol, é completamente balanceado pelo fluxo de energia eletromagnética que deixa o planeta na forma de calor. Em outras palavras, a Terra está em equilíbrio radiante, o que torna a temperatura relativamente estável ao longo de milênios.
Assim, é correto afirmar que o sol fornece
Provas
A queima de combustíveis à base de Carbono, na presença de Oxigênio atmosférico, foi talvez a primeira tecnologia da engenharia química desenvolvida pelo ser humano.
Quando dominamos o fogo, milênios antes de entendermos os princípios científicos envolvidos, aprendemos a reproduzir comportamentos empíricos e a contornar as dificuldades que apareciam, nos forçando a ser uma espécie cada vez mais criativa. Seguramente não foram poucos os dias de vento e chuva, onde os ancestrais humanos tiveram de usar musgo, cera das cascas de frutas e óleo de folhas de coníferas para aproveitar as chispas do novo conhecimento. Muito tempo se passou, a chama do conhecimento cresceu ainda mais e a humanidade decidiu explorar o espaço. Novamente, se deparou com dificuldades impensadas até então. Agora precisamos queimar metais (para obter maiores quantidades de energia) e levantar foguetes até superar a atmosfera terrestre. Exatamente lá onde não temos o oxigênio nos esperando com nossa fagulha de atrevimento. Mas encontramos soluções, como sempre fazemos.
Os poderosos combustíveis sólidos foram adotados inicialmente pela NASA em seus lançamentos e agora também sendo usados pelas agências privadas que prestam serviços aos governos, levando carga e passageiros para suas missões fora do planeta. As reações a seguir, representam as duas principais reações de oxirredução envolvidas na queima dos combustíveis sólidos dos foguetes:
2 NH4ClO4 (s) + 2 Al (s) !$ \rightarrow !$ Al2O3 (s) + 2 HCl (g) + 2 NO (s) + 3 H2O (g)
Reação 1
6 NH4ClO4 (s) + 10 Al (s) !$ \rightarrow !$ 5 Al2O3 (s) + 6 HCl (g) + 3 N2 (g) + 9 H2O (g)
Reação 2
Analisando ambas as reações combinadas, fica evidente que o alumínio passa do estado de oxidação (zero) para (3+), enquanto o cloro passa de (+7) para (-1). Assim, pode-se concluir nessa análise que o estado de oxidação de nitrogênio vai de
Provas
A reação de queima do alumínio na oxirredução que envolve o poderoso oxidante perclorato de amônio e forma tri-óxido-de-di-alumínio (responsável pelo interminável rastro branco deixado nos céus durante os lançamentos), ácido clorídrico, gás nitrogênio, óxido nitroso, e água. Em seu balanço de massa, vemos que 69,6% do peso é referente ao oxidante, enquanto o combustível (alumínio metálico) corresponde a 16%. Imagina-se que para atingir o ponto de queima de metais, temos de superar uma importante energia de ativação. Por conta disso, temos a participação de um catalizador à base de óxido de ferro (0,4% do peso da mistura). Fundamental nesse sistema, temos ainda 12,04% de um polímero aglutinante (para manter os ingredientes posicionados e garantir a continuidade da combustão). Afinal temos uma força explosiva tentando separar toda a mistura e não contamos com a convergente força da gravidade, que temos sempre quando estamos com os pés na terra. O complemento é dado por 1,96% do peso total em um agente à base de resina epóxi para assegurar a cura do polímero aglutinante.
Sem contar que esse tipo de combustível, depois de aceso no foguete, não pode ser parado.
Realmente, avançamos muito nos processos, ingredientes e tecnologias da combustão desde que começamos a queimar galhos secos de árvores, incendiados com uma faísca vinda de duas pedras se chocando. Apesar dessa incrível jornada tecnológica, os processos de combustão seguem todos os princípios simples e semelhantes.
Sobre o assunto, assinale a alternativa mais adequada para resumir a combustão.
Provas
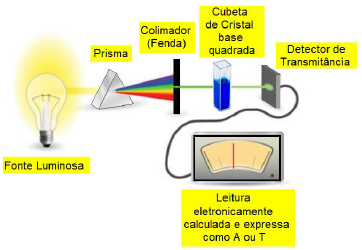
A absorbância de uma amostra foi medida em condições padronizadas a partir de uma fonte de luz conhecida e colimada em determinado comprimento de onda, caminho ótico conhecido em uma cubeta de dimensões padronizadas e um indicador eletrônico da intensidade da luz absorvida pela amostra. Sabendo que o valor da absorbância medida é proporcional à concentração da substância amostrada na cubeta de acordo com a equação de Lambert–Beer:
A = !$ \varepsilon !$bc
Onde:
A é a absorbância da amostra;
!$ \varepsilon !$ é a absortividade molar da substância analisada;
b é o comprimento do caminho seguido pela luz, convencionado em medida unitária (cubeta quadrada de 1 cm por 1 cm);
c é a concentração da espécie absorvente.
Comparando-se 3 amostras da mesma substância entre si, chega-se a 3 leituras diferentes de Absorbância, medidas sempre no mesmo comprimento de onda de 540 nm:
Amostra 1 ………… A1 = 2,0
Amostra 2 ………… A2 = 4,0
Amostra 3 ..……….. A3 = 1,0
A partir desses resultados, é correto afirmar que a amostra
Provas
O uso de cromatografia para separar e identificar substâncias em uma mistura, é uma das técnicas experimentais mais versáteis da Química. Diversas são as técnicas: cromatografia gasosa, cromatografia de fase líquida, cromatografia de troca iônica, cromatografia por afinidade etc. Se hoje se usam colunas de cromatografia líquida super sofisticadas e de longos comprimentos, toda essa técnica nasceu da cromatografia de fase delgada e da cromatografia em papel. Mas os princípios básicos são sempre os mesmos. Trata-se de uma corrida entre moléculas que se deseja separar, identificar ou medir a concentração na mistura. Existe uma fase móvel, formada pelas moléculas sendo comparadas e um fluido carreador, que viaja através da fase estática. Essa fase estática, por sua vez, representa desafios diferenciados por afinidade ou por diferença com cada uma das moléculas que competem entre si. A medida que cada molécula termina o percurso estacionário, nessa corrida com obstáculos, seu tempo de prova pode ser registrado, que passará a identificá-la nas condições utilizadas. Instrumentos analíticos como espectrofotômetros de chama ou espectrômetros de massa etc. podem ser usados para corroborar as identificações dessas moléculas.
Ao final da corrida, plota-se um gráfico característico.
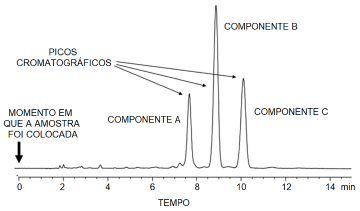
Considerando as informações do gráfico de HPLC (sigla em inglês de uma técnica cromatográfica, que se traduz como Cromatografia Líquida de Alta Performance), é correto afirmar que
Provas
A Cidade do México, Capital Federal do México, foi construída em solos formados por misturas de argila, fragmentos vulcânicos, areia e água, onde antes existia um lago profundo.
Sua consistência é pouco compactada e reage com liquefação/fluidificação momentânea na sua superfície, quando submetida a abalos sísmicos de grande magnitude, o que se repete a intervalos de algumas décadas entre si. Segundo o Professor James Jackson, Geofísico da Universidade de Cambridge, na Inglaterra, o solo macio da Cidade do México aumenta os efeitos dos sismos que lá acontecem, pois durante os abalos, o solo responde assumindo aspectos pseudoplásticos em seu comportamento, instabilizando as estruturas de sustentação das edificações. É como se suas fundações deixassem de se ancorar em terra firma durante os terremotos e se apoiassem por instantes em gelatina. Isso explica as enormes perdas em edificações e vidas humanas durante grandes terremotos, como o ocorrido em 1985.
O comportamento não newtoniano desse tipo de solos, mesmo na ausência de grandes abalos, responde também ao excesso de concentração de cargas em edifícios e permite o recalque das edificações, causando a sua inclinação ao longo do tempo. Fenômenos dessa natureza acontecem em várias partes do mundo onde areia, argila e água de origem sedimentar se acumulam por longos períodos. No Brasil, vemos o fenômeno do recalque em cerca de 65 prédios construídos na orla santista, que se inclinam um para o outro (apelidados de “edifícios amantes”).
Nesses projetos, foram utilizadas fundações de sapatas rasas, de 4 a 5 metros de profundidade, já que a investigação de solo realizada nos anos 1950s e 1960s apontou que o solo, até 12 metros de profundidade, se mostrava compacto. Porém, não sabiam que abaixo desse solo existia uma camada de solo mole e outras camadas de solos arenosos. Hoje, por segurança, as fundações de edifícios da orla santista, em especial entre os canais três e seis, são estruturas de estacas profundas, que se estendem cerca de 50 m abaixo da superfície, até atingirem rocha mãe, garantindo a estabilidade do prumo das construções mais recentes.
Alguns dos edifícios que sofreram recalques, chegaram a graus de inclinação maiores do que manda a norma e tiveram de sofrer intervenções de engenharia para solucionar seu problema.
Os casos de melhor sucesso no reajuste do prumo e estancamento das inclinações envolveram substituir as sapatas de baixa profundidade por uma elevação das estruturas rasas com macacos hidráulicos, drenagem de parte do solo inadequado, preenchimento com concreto formando um piso de sustentação, ancorado por um conjunto de estacas volumosas com profundidades ao redor de 50 m.
Com base no texto, sabe-se que os solos pseudoplásticos diminuem sua viscosidade conforme se deformam. Entretanto, a sua viscosidade também diminui com o passar do tempo em que estão sobre uma tensão (efeito tixotrópico). Quando deixados em repouso, tais solos fluidos retornam à viscosidade normal (voltam do estado liquidificado para o sólido). Também são exemplos desse mesmo tipo de comportamentos não-newtonianos a areia movediça, as tintas de paredes, as pastas de dentes e o ketchup. Apesar das semelhanças entre os problemáticos solos de comportamento não-newtonianos da Cidade do México – MX e de Santos – BR, ao longo das 5 últimas décadas, não se registraram casos de desabamento de prédios na orla santista, apesar das inclinações relatadas.
Assim, essa diferença de comportamento se deve
Provas
Ao medir alcalinidade, os resultados são normalmente expressos como ppm (ou mg/L) de Carbonato de Cálcio (CaCO3). Íons de hidróxido (OH–), íons de Bicarbonato (HCO3–) e íons de Carbonato (CO32-) também contribuem para a alcalinidade da água. A mesma unidade de medida pode ser indicadora da concentração dos íons de Ca2+.
Cátions como Ca2+ e Mg2+ devem ser controlados em águas recebidas para processos industriais, pois são fonte de sais de “dureza”. Sua presença em sistemas geradores de vapor pode ser danosa, já que sais desses cátions tendem a formar incrustrações e pontos de aderência em caldeiras e linhas de condução de vapor, prejudicando sua eficiência de troca térmica, gerando pontos de superaquecimento na tubulação e gastando mais combustível no processo. Isso se deve aos precipitados de carbonatos e sulfatos de Cálcio e Magnésio, insolúveis em água.
A melhor solução para esse problema está na prevenção, retirando tais cátions no processo de tratamento de água.
Os 2 principais tratamentos usados para garantir a qualidade da água a ser usada nas caldeiras são:
- Tratamento com fosfatos, que precipitam os sais de cálcio e magnésio, formando um lodo no fundo da caldeira que pode ser facilmente purgado;
- Tratamento com quelatos (como EDTA, por exemplo). Formam-se complexos solúveis com cálcio e magnésio, permitindo a indisponibilização dos mesmos para atacar as paredes das tubulações e da caldeira.
Em escala de laboratório, é comum se trabalhar com água deionizada por passagem em resinas de troca iônica ou até mesmo com água destilada, quando se precisa remover a dureza da água de trabalho.
Sobre essa mudança de procedimentos de trabalho entre a escala de laboratório e a escala industrial, é correto afirmar que
Provas
Alcalinidade total e pH são conceitos inter-relacionados, mas diferentes. O pH mede a concentração de íons H+ ou de OH- indicando o quanto uma solução é ácida ou básica, em uma escala absoluta e de crescimento exponencial. Por sua vez, a alcalinidade total indica quanto ácido ou base a solução pode absorver sem alterar de forma impactante seu pH. Em outras palavras, a alcalinidade total mede a capacidade de tamponamento de uma solução, uma certa elasticidade em absorver ácidos sem impactar os valores de pH. Essa capacidade de tamponamento é extremamente importante para a manutenção da vida, e é comum encontrarmos muitos exemplos de soluções tamponadas nos sistemas biológicos. Em fontes naturais de água, a alcalinidade varia de acordo com a geologia do local. Os minerais das rochas mais próximas e a permeação do solo influenciam dramaticamente a alcalinidade das águas adjacentes. Por exemplo, áreas com predominância de rochas de calcário terão uma alcalinidade maior em suas águas do que áreas com predominância de rochas graníticas. Ao medir alcalinidade, os resultados são normalmente expressos como ppm (ou mg/L) de Carbonato de Cálcio (CaCO3). Íons de hidróxido (OH–), íons de Bicarbonato (HCO3–) e íons de Carbonato (CO32-) também contribuem para a alcalinidade da água.
Diante do exposto, pode-se afirmar que o(a)
Provas
Caderno Container