Foram encontradas 533 questões.
Alcalinidade total e pH são conceitos inter-relacionados, mas diferentes. O pH mede a concentração de íons H+ ou de OH- indicando o quanto uma solução é ácida ou básica, em uma escala absoluta e de crescimento exponencial. Por sua vez, a alcalinidade total indica quanto ácido ou base a solução pode absorver sem alterar de forma impactante seu pH. Em outras palavras, a alcalinidade total mede a capacidade de tamponamento de uma solução, uma certa elasticidade em absorver ácidos sem impactar os valores de pH. Essa capacidade de tamponamento é extremamente importante para a manutenção da vida, e é comum encontrarmos muitos exemplos de soluções tamponadas nos sistemas biológicos. Em fontes naturais de água, a alcalinidade varia de acordo com a geologia do local. Os minerais das rochas mais próximas e a permeação do solo influenciam dramaticamente a alcalinidade das águas adjacentes. Por exemplo, áreas com predominância de rochas de calcário terão uma alcalinidade maior em suas águas do que áreas com predominância de rochas graníticas. Ao medir alcalinidade, os resultados são normalmente expressos como ppm (ou mg/L) de Carbonato de Cálcio (CaCO3). Íons de hidróxido (OH–), íons de Bicarbonato (HCO3–) e íons de Carbonato (CO32-) também contribuem para a alcalinidade da água.
Diante do exposto, pode-se afirmar que o(a)
Provas
Quando se observam os catalizadores automobilísticos, vê-se que ajudam a promover a queima completa de vários gases que deixam o motor em reações de oxidação incompletas. Eles são fundamentais para a melhoria da qualidade do ar em grandes cidades, pois podem reduzir as emissões de gases altamente poluentes em até 80%.
Exemplo: Óxido de Nitrogênio, Monóxido de Carbono, Hidrocarbonetos diversos. Sua temperatura ideal de atuação catalítica gira ao redor de 400 °C até 800 °C. Os catalizadores são estruturas complexas, compostas por uma base cerâmica, com área cheia de microvilosidades, recobertos por diferentes materiais ativos, capazes de gerar sinergias entre eles. Por exemplo, a Platina é um metal nobre que atua melhor em ambientes com abundância de O2, oxidando os gases poluente de forma sequencial. Já em ambientes ou momentos com menor disponibilidade de oxigênio, o Ródio entra em ação, catalisando outros mecanismos de reação para formar gases menos poluentes.
A presença desses metais encarece o acessório dos veículos, mas a durabilidade pode se estender a toda a vida útil do automóvel, já que o catalisador nunca é consumido na reação.
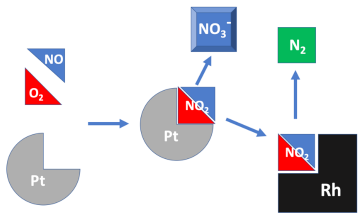
O mecanismo típico de catálise heterogênea envolve os seguintes passos:
Provas
O tratamento de água para linhas de vapor pode ser dividido em 3 partes: desaeração em “flasheamento”, tratamento químico e purgas.
Sobre o processo de purga, assinale a alternativa correta.
Provas
Considere os dados de massas atômicas e as massas molares abaixo para responder à questão.
Cl - 35,45 uma
I - 126,90 uma
Ag - 107,87 uma
Hg - 200,59 uma
Pb - 207,20 uma
AgCl - 143,32 g.mol-1
PbCl2 - 278,10 g.mol-1
Hg2Cl2 - 472,09 g.mol-1
AgI - 234,77 g.mol-1
PbI2 - 461,01 g.mol-1
Hg2I2 - 654,99 g.mol-1
O cloreto branco da questão anterior, que havia sido totalmente precipitado por solução HCl diluído, foi depois redissolvido em solução aquosa por aquecimento em banho-maria. O íon foi novamente precipitado, agora pela ação de uma solução de Iodeto de Potássio (KI), gerando um sal amarelo. Esse novo sal, foi filtrado, separado, seco e pesado em balança analítica, totalizando 9,22 g do sal de Iodeto para cada litro da amostra original.
Assinale a alternativa que apresenta a concentração molar desse íon encontrado na solução amostra original.
Provas
O precipitado branco da questão anterior (que havia sido completamente precipitado com HCl diluído), foi recolhido após filtração, recebeu mais 10 ml de água destilada e foi aquecido em banho-maria até a temperatura de ebulição da água, mantido assim por cerca de 5 minutos. Esse processo de aquecimento dissolveu todo material que estava precipitado. Isso indicou que apenas um dos 3 cloretos estava presente no sal branco que havia precipitado, já que dois deles são tão insolúveis que não se redissolveriam com o aquecimento na solução aquosa, sem que ocorressem mudanças no pH da solução.
Com base nas informações fornecidas, assinale a alternativa que apresenta qual dos 3 cátions estava presente na solução amostra: Ag+, Pb2+ ou Hg22+.
Provas
Analise as informações abaixo para responder à questão.
Os cloretos dos íons Prata (Ag+), Chumbo (Pb+2) e Mercuroso (Hg2+2) são insolúveis à temperatura ambiente em meio neutro ou ácido, e seus respectivos Kps e reações de precipitação são descritos a seguir.
Ag+ + Cl- !$ \rightarrow !$ AgCl (s) Kps = 1,82 . 10-10
Pb2+ + 2Cl- !$ \rightarrow !$ PbCl2 (s) Kps = 1,71 . 10-5
Hg22+ + 2Cl- !$ \rightarrow !$ Hg2Cl2 (s) Kps = 1,22 . 10-18
Em uma solução amostra, dentro de um tubo de ensaio, gotejou-se uma solução diluída de HCl em quantidade suficiente para causar a precipitação completa de sais brancos no fundo do tubo. A partir desse teste, sobre a composição da solução amostra antes da precipitação, pode-se concluir que
Provas
A pilha de Zinco/Óxido de Manganês pode ser representada pelas reações abaixo. A reação no ânodo será de formação de cloreto de zinco e liberação de um elétron:
Zn + 2 Cl− !$ \rightarrow !$ ZnCl2 + 2 e−
A reação no cátodo produz hidróxido de zinco e óxido de manganês (3+):
2 MnO2 + ZnCl2 + H2O + 2 e− !$ \rightarrow !$ Mn2O3 + Zn(OH)2 + 2 Cl−
A reação geral simplificada da pilha vai ser:
Zn + 2 MnO2 + H2O !$ \rightarrow !$ Mn2O3 + Zn(OH)2
Essas pilhas alcalinas fornecem um ddp de cerca de 1,5 volts, e como todas as pilhas, tendem a sofrer com a autodescarga e com reações de deterioração. Mesmo ficando sem uso, sua capacidade vai se degradando aos poucos, pois a placa de zinco na pilha vai sendo corroída com o tempo e ocorrem vazamentos que colocam os eletrólitos em contato. Esses processos de auto degradação são acelerados quando as pilhas são submetidas a temperaturas mais altas. Nesse tipo de pilha, cerca de 0,08% de sua capacidade é perdida a cada dia sob uma temperatura de 20 °C (ou seja, em 2 meses, sem usar a pilha, sua capacidade terá chegado a cerca de 94,5% do valor original). Essa degradação é fortemente acelerada, podendo chegar a 0,6% quando a temperatura ambiente é de 45 °C (em 2 meses, sem usar a pilha, sua capacidade terá chegado a cerca de 69,7% do valor original) reduzindo importantemente a vida útil da pilha.
Assim, mesmo sem estarem em uso, pilhas AAA alcalinas têm uma capacidade de armazenamento inicial que vai caindo mais ou menos rapidamente, a partir dos valores iniciais de 1250 miliamp.hora ou 1.87 watts.hora. Por conta disso, os fabricantes de pilhas recomendavam guardá-las sob refrigeração enquanto não estivessem em uso, (sempre protegidas em sacos plásticos para não entrarem em contato com alimentos). O barateamento desse tipo de pilha no mundo fez mudar tais recomendações, mas seus princípios seguem válidos. Dessa maneira, a refrigeração faria as pilhas serem melhor preservadas em sua capacidade, até o momento do uso. Segundo a equação de Arrhenius:
K = A.e -Ea /RT
Onde:
K é a constante de velocidade de uma reação química;
A é o chamado fator pré-exponencial;
Ea é a Energia de ativação da reação;
T é a Temperatura em °K .
Com base na equação acima, é correto afirmar que
Provas
Sabe-se que os aparelhos de espectrofotometria leem sempre uma diferença entre a fonte de luz sem a amostra e a luz que a atravessa. Nesse comparativo, a grandeza física realmente mediada é a transmitância, não a absorbância. Na prática, utiliza-se mais os valores de absorbância.
Felizmente, a conversão entre as duas grandezas exige apenas o seguinte cálculo matemático:
Absorbância = log (1/Transmitância)
Foram feitas duas leituras de Transmitância (T1 e T2), de amostras distintas. As absorbâncias, nesse caso, indicam a presença de um contaminante (chumbo) na solução.
Quanto mais concentrada em íons chumbo (2+) na solução, mais intensa é sua absorbância.
Os valores encontrados para as leituras de transmitâncias, foram os listados abaixo.
T1 = 0,1
T2 = 1,0
Para expressar esses valores nas suas respectivas Absorbâncias (A1 e A2), assinale a alternativa que apresenta, respectivamente, os valores equivalentes e quais seriam as amostras contaminadas com sal de chumbo.
Provas
A medida do pH é um controle importante para garantir a qualidade da água e permitir o funcionamento adequado das caldeiras e seus sistemas e tubulações. Portanto, se faz necessária a instalação de um sensor de pH no conjunto gerador de vapor.
Com esse objetivo, é correto afirmar que o sensor de pH deve ser instalado
Provas
Os gases fluorocarbonetos e seus derivados (onde pode haver também outros átomos, como hidrogênio ou cloro) foram sintetizados a partir da década de 1930 pelo cientista Thomas Midgely Jr. e logo surpreenderam por sua baixa reatividade química. As ligações entre carbono e flúor são tão fortes, que esses compostos ignoram quase que completamente o ataque químico da maioria das moléculas, só reagindo com aquelas extremamente oxidantes. Essa inércia química, mesmo à quente, associada ao fato de serem inodoros e incolores, fez com que fossem usados como expansores na fabricação de polímeros orgânicos e, também, como gases propulsores de aerossóis. Outra propriedade dos fluorocarbonetos nasce da baixa interação entre as suas próprias moléculas, o que diminui seus pontos de fusão e ebulição quando comparados a moléculas de hidrocarbonetos com estruturas similares. Isso confere a elas excelentes propriedades criogênicas, o que tornou os fluorocarbonetos ideais para serem usados nos motores de refrigeração (nos ciclos de compressão, expansão, evaporação e condensação). Observando a condutividade térmica do gás Tetra-Flúor-Metano (CF4, nome comercial FREON 14), ele apresenta um valor de 4,06 (Kgás / cal / cm . K . s), tendo sido usado como gás de refrigeradores, material de isolamento térmico em janelas de vidro, propulsor de aerossóis e outras aplicações por décadas. Atualmente ele quase não é mais usado nessas aplicações, tendo sido paulatinamente substituído inicialmente por moléculas de Cloro-Fluor-Carboneto e mais recentemente essas também foram substituídas por algumas moléculas menos eficientes nas características de isolamento e refrigeração, além do que, os novos refrigerantes são muitas vezes inflamáveis, como o Isobutano.
Sobre o assunto, é correto afirmar que o CF4 perdeu seu lugar de destaque tanto na refrigeração como no isolamento térmico porque
Provas
Caderno Container