Foram encontradas 160 questões.
Texto para a questão.
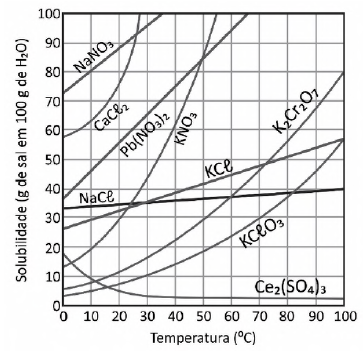
Curvas de solubilidade em água em função da temperatura para algumas substâncias
Provas
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química CinéticaTransformações Químicas
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
Texto para a questão.
Entre os elementos conhecidos, alguns são familiares a todos e outros são bastante raros. Algumas das substâncias elementares são metais e outras, não. temperatura ambiente, alguns são gases, alguns, líquidos e outros, sólidos. Variam eles extremamente nas propriedades químicas e na natureza dos compostos que formam. Como consequência, estudar química não é simples nem fácil. Para se adquirir conhecimento razoável de química geral, é necessário aprender um grande número de fatos. Não existe uma teoria que unifique todos esses fatos completamente. Contudo, várias teorias foram desenvolvidas suficientemente para servir de ajuda ao estudante na tarefa de aprender algo sobre as propriedades e reações das substâncias, correlacionando informações empíricas com teorias, como, por exemplo, a lei periódica.
L. Pauling. Química Geral. Rio de Janeiro: Ao Livro
Técnico e Edusp, 1966 (com adaptações).
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Texto para a questão.
Curvas de solubilidade em água em função da temperatura para algumas substâncias

Deseja-se preparar duas soluções saturadas na temperatura de 20 °C, uma contendo o sal menos solúvel e outra contendo o sal mais solúvel nessa temperatura. Para cada uma das soluções, será empregado o mínimo possível dos sais e será utilizado 1 L de água, mantida a 20 °C durante todo o processo de dissolução. A massa específica da água é igual a 1.000 kg m-3.
Com base nesse caso hipotético e no gráfico, assinale a alternativa que apresenta, correta e respectivamente, as massas aproximadas dos dois sais necessárias para o preparo dessas soluções.
Provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
Provas
Texto para a questão.
Desde o início dos tempos, vem o homem executando trabalhos de engenharia progressivamente mais complexos, com a finalidade de suprir abrigo e propiciar conforto para si e seus dependentes, protegendo-os dos perigos e das intempéries. O primeiro elemento estrutural, isto é, o primeiro material de engenharia usado pelo homem, foi a madeira, seguindo-se a pedra, depois os metais, a cerâmica, o vidro e, finalmente, os polímeros.
E. B. Mano. Polímeros como materiais de engenharia. São Paulo: Edgard Blücher, 1991.
Provas
Texto para a questão.
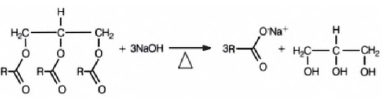
A exploração, em sala de aula, do tema sabões e detergentes permite diferentes enfoques e técnicas de ensino, que promovem o pensamento crítico dos alunos por se tratar de um tema organizador relacionado a seu cotidiano. Tal proposta valoriza o aluno como indivíduo pensante, promovendo o papel do professor a mediador e orientador do processo educacional. Isso valoriza o papel desempenhado pela escola e contribui com o processo de aprendizagem da química, favorecendo, encorajando e sustentando a autoconstrução e o desenvolvimento do conhecimento por parte dos alunos. Nesse contexto, a equação genérica seguinte descreve o processo de saponificação, em que R corresponde a cadeias iguais ou diferentes, contendo entre 12 e 18 átomos de carbono.
Provas
Considerando o texto acima, assinale a alternativa que apresenta, correta e respectivamente, essas transformações.
Provas
CH4 (g) + 2 O2 (g) → CO2 (g) + 2 H2O (g) ΔH1 CH4 (g) + 2 O2 (g) → CO2 (g) + 2 H2O (l) ΔH2
Assinale a alternativa que apresenta a relação entre essas variações de entalpia.
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Texto para a questão.
Surfactantes ou agentes tensoativos são moléculas que se associam espontaneamente, em solução aquosa, a partir de uma determinada concentração. Apresentam uma região apolar e outra polar, ou iônica, e podem ser divididos em neutros ou iônicos. Os tensoativos iônicos podem ser catiônicos ou aniônicos ou, ainda, anfóteros, quando ambas as cargas estão presentes no surfactante. Em soluções diluídas, as moléculas dos surfactantes apresentam-se dispersas e, em soluções mais concentradas, organizam-se em agregados moleculares, que geralmente contêm de 50 a 100 moléculas, denominadas de micelas.
I. M. Rizzatti, D. R. Zanette e L. C. Mello. Determinação
potenciométrica da concentração micelar crítica de
surfactantes: uma nova aplicação metodológica
no ensino de química. In: Química Nova, v. 32,
n.° 2, 2009, p. 518-521 (com adaptações).
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Texto para a questão.
Curvas de solubilidade em água em função da temperatura para algumas substâncias

Provas
Caderno Container