Foram encontradas 40 questões.
A testosterona é um hormônio esteroide fundamental, principalmente conhecido como o principal
hormônio masculino, embora também esteja presente em mulheres em níveis mais baixos. É crucial para
o desenvolvimento das características sexuais secundárias masculinas, como aumento da massa
muscular, pelos faciais e corporais e profundidade da voz. Contribui para a densidade óssea, distribuição
de gordura, produção de glóbulos vermelhos e libido. A progesterona é um hormônio esteroide
importante, especialmente relacionado à reprodução e à saúde feminina. Em mulheres é produzida
principalmente pelos ovários, especialmente após a ovulação, e pela placenta durante a gravidez. Abaixo
são representadas as respectivas estruturas, figura 4.
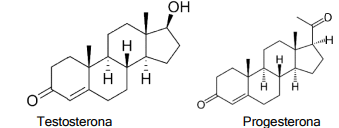
Figura 4. Hormônios esteroides masculino e feminino. Disponível em: https://pt.wikipedia.org/wiki/Testosterona/Progesterona. Acessado em: setembro.2024
Nas alternativas descritas, assinale corretamente qual delas indica as funções orgânicas presentes nas duas substâncias.

Figura 4. Hormônios esteroides masculino e feminino. Disponível em: https://pt.wikipedia.org/wiki/Testosterona/Progesterona. Acessado em: setembro.2024
Nas alternativas descritas, assinale corretamente qual delas indica as funções orgânicas presentes nas duas substâncias.
Provas
Questão presente nas seguintes provas
No grupo de funções orgânicas oxigenadas, o manitol é um tipo de açúcar que é utilizado em várias
aplicações na indústria alimentícia, farmacêutica e médica. Dente elas, o manitol é frequentemente
utilizado como um adoçante em produtos dietéticos e sem açúcar, devido ao seu baixo índice glicêmico,
também atua como um agente de textura e conservante. Na medicina, o manitol é utilizado como um
diurético osmótico, ajudando a reduzir a pressão intracraniana e a pressão ocular. É frequentemente
utilizado em emergências, como em pacientes com edema cerebral ou glaucoma. Pode ser encontrado
naturalmente em algumas plantas, como em frutas (por exemplo, maçãs e peras) e em algas. Sua
fórmula estrutura é apresentada na figura 3 a seguir.

Figura 3. Fórmula estrutural do manitol. Disponível em https://pt.dreamstime.com/manitol-mannite-ou-f%C3%B3rmula-qu%C3%ADmica-do-a%C3%A7%C3%BAcar-manna-e-estruturaesquel%C3%A9tica-de-manga-is%C3%B4mero-sorbitol-utilizado-como-image209330436. Acesso em: setembro.2024.
Qual o nome oficial segundo o International Union of Pure and Applied Chemistry (IUPAC) desse açúcar?

Figura 3. Fórmula estrutural do manitol. Disponível em https://pt.dreamstime.com/manitol-mannite-ou-f%C3%B3rmula-qu%C3%ADmica-do-a%C3%A7%C3%BAcar-manna-e-estruturaesquel%C3%A9tica-de-manga-is%C3%B4mero-sorbitol-utilizado-como-image209330436. Acesso em: setembro.2024.
Qual o nome oficial segundo o International Union of Pure and Applied Chemistry (IUPAC) desse açúcar?
Provas
Questão presente nas seguintes provas
O elemento Tório (Th) é um metal prateado e macio, que se torna mais duro e quebradiço quando
oxidado. Seu isótopo mais abundante é o tório-232 (²³²Th), que é radioativo e possui uma meia-vida de
aproximadamente 14 bilhões de anos. Mas sua radioatividade é relativamente baixa em comparação com
outros elementos como o urânio ou o plutônio. Dentre seus usos cita-se: como combustível em reatores
nucleares, e produzem menos resíduos que reatores de urânio, em lâmpadas de gás de alta intensidade,
é usado também na produção de cerâmicas especiais, devido à sua alta resistência ao calor.
MAHAN, Bruce M. Química: um curso universitário. 4ª ed. Editora Blücher, São Paulo: 1995. p. 582.
Suponha que este elemento, 90Th232 , de número atômico 90 e número de massa igual a 232, emita sucessivamente uma partícula α seguida de duas emissões β e novamente uma emissão α. Ao final, o átomo que encerra essa série de emissões terá em seu núcleo:
MAHAN, Bruce M. Química: um curso universitário. 4ª ed. Editora Blücher, São Paulo: 1995. p. 582.
Suponha que este elemento, 90Th232 , de número atômico 90 e número de massa igual a 232, emita sucessivamente uma partícula α seguida de duas emissões β e novamente uma emissão α. Ao final, o átomo que encerra essa série de emissões terá em seu núcleo:
Provas
Questão presente nas seguintes provas
No estudo da interação de radiação com a matéria, as partículas alfa (α), beta (β) e gama (ϒ) emitidas
em processos de decaimento nuclear são altamente energéticas e provocam alterações químicas
substanciais, à medida que interagem com a matéria. A excitação eletrônica de uma molécula pode levar
a sua dissociação em átomos ou outras moléculas. Os íons atômicos e moleculares produzidos pela
radiação são também muito reativos, e isso pode ter importantes consequências químicas.
MAHAN, Bruce M. Química: um curso universitário. 4ª ed. Editora Blücher, São Paulo: 1995. p. 582.
Neste contexto, o Ferro (Ferro – 59, 26Fe59) é um isótopo radioativo, bastante usado em análises clínicas no diagnóstico de anemia.
A equação nuclear para o decaimento do 26Fe59 , como um emissor beta é:
MAHAN, Bruce M. Química: um curso universitário. 4ª ed. Editora Blücher, São Paulo: 1995. p. 582.
Neste contexto, o Ferro (Ferro – 59, 26Fe59) é um isótopo radioativo, bastante usado em análises clínicas no diagnóstico de anemia.
A equação nuclear para o decaimento do 26Fe59 , como um emissor beta é:
Provas
Questão presente nas seguintes provas
Quando a água cai espontaneamente, em uma cachoeira, a Física explica o fato afirmando que a água
caiu de um nível de maior energia para outro, de menor energia (no caso, energia potencial). Quanto
maior for a quantidade de água e maior a altura da queda, maior será a energia liberada pela água (que
pode ser transformada, por exemplo, em energia elétrica, em uma usina hidroelétrica). Fato idêntico
ocorre com as pilhas, dependendo dos materiais (metais e eletrólitos) que formam a pilha, ela irá
“despejar” uma quantidade maior ou menor de elétrons, com mais ou menos energia, através do circuito
externo. A altura da queda de água corresponde, na eletricidade, ao que se chama de diferença de
potencial (ddp) ou, mais especificamente, de força eletromotriz (fem) da pilha, representa a “pressão” que
move os elétrons através do condutor externo, ela é medida em Volts (V), com o uso de voltímetros.
Com base nas explicações presentes no texto, observe a célula eletroquímica representada na figura 2 a seguir:
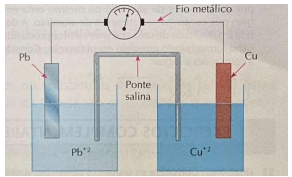
Figura 2. Célula Eletroquímica Fonte: Brady. J.E; Humiston, G. E. Química Geral. Vol. 2. 2ª ed. Livros Técnicos e Científicos Editora. 1996.
Considere os Potenciais:
Pb+2 + 2e ⟶ Pb (Eº = - 0,13 V) Cu+2 + 2e ⟶ Pb (Eº = + 0,34 V)
Pode-se afirmar corretamente sobre a célula que:
Com base nas explicações presentes no texto, observe a célula eletroquímica representada na figura 2 a seguir:

Figura 2. Célula Eletroquímica Fonte: Brady. J.E; Humiston, G. E. Química Geral. Vol. 2. 2ª ed. Livros Técnicos e Científicos Editora. 1996.
Considere os Potenciais:
Pb+2 + 2e ⟶ Pb (Eº = - 0,13 V) Cu+2 + 2e ⟶ Pb (Eº = + 0,34 V)
Pode-se afirmar corretamente sobre a célula que:
Provas
Questão presente nas seguintes provas
Algumas pilhas galvânicas comuns têm papel importante em nossas vidas, fornecendo-nos energia
elétrica, dentre elas têm a pilha seca de zinco-carbono. Este tipo de pilha é usado em lanternas, rádios
portáteis, brinquedos etc. Na figura 1, a seguir, mostra-se um diagrama em corte de uma pilha seca de
zinco-carbono típica.
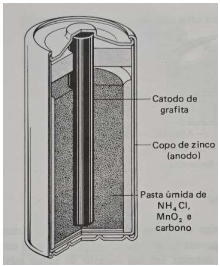
Figura 1. Pilha Galvânica, pilha seca de Zinco-Carbono. Fonte: Brady. J.E; Humiston, G. E. Química Geral. Vol. 2. 2ª ed. Livros Técnicos e Científicos Editora. 1996.
Considere as assertivas a seguir:
I. As pilhas secas têm uma camada externa de papelão ou metal, que serve apenas para isolá-la da atmosfera, e, interiormente a este revestimento, há um copo de zinco que serve como ânodo.
II. O copo de zinco é cheio de uma massa úmida, consistindo de cloreto de amônio, dióxido de manganês e carbono finamente dividido, e imerso nesta pasta há um bastão de grafita, que serve como cátodo.
III. A amônia produzida no cátodo reage com parte do Zn 2+, formado no ânodo, para dar o íon complexo Zn(NH3)4 2+ . Devido a natureza da pilha não se pode escrever uma única reação global.
IV. As pilhas secas não podem ser recarregadas e, portanto, têm um tempo de vida relativamente longo, como, por exemplo, quando comparadas com a bateria de chumbo e a pilha de níquel-cádmo que são recarregáveis.
V. No ânodo, o zinco é reduzido, enquanto que, no cátodo, a mistura de MnO2/NH4Cl sofre oxidação, para dar uma mistura complexa de produtos.
Assinale a alternativa que contenha APENAS as afirmações corretas.

Figura 1. Pilha Galvânica, pilha seca de Zinco-Carbono. Fonte: Brady. J.E; Humiston, G. E. Química Geral. Vol. 2. 2ª ed. Livros Técnicos e Científicos Editora. 1996.
Considere as assertivas a seguir:
I. As pilhas secas têm uma camada externa de papelão ou metal, que serve apenas para isolá-la da atmosfera, e, interiormente a este revestimento, há um copo de zinco que serve como ânodo.
II. O copo de zinco é cheio de uma massa úmida, consistindo de cloreto de amônio, dióxido de manganês e carbono finamente dividido, e imerso nesta pasta há um bastão de grafita, que serve como cátodo.
III. A amônia produzida no cátodo reage com parte do Zn 2+, formado no ânodo, para dar o íon complexo Zn(NH3)4 2+ . Devido a natureza da pilha não se pode escrever uma única reação global.
IV. As pilhas secas não podem ser recarregadas e, portanto, têm um tempo de vida relativamente longo, como, por exemplo, quando comparadas com a bateria de chumbo e a pilha de níquel-cádmo que são recarregáveis.
V. No ânodo, o zinco é reduzido, enquanto que, no cátodo, a mistura de MnO2/NH4Cl sofre oxidação, para dar uma mistura complexa de produtos.
Assinale a alternativa que contenha APENAS as afirmações corretas.
Provas
Questão presente nas seguintes provas
O cromo é um elemento químico com várias características importantes, dentre elas pode-se citar no
setor industrial, sendo amplamente utilizado na fabricação de ligas (como o aço inoxidável), na produção
de pigmentos (como o óxido de cromo) e em tratamentos de superfícies para proteção contra corrosão. É
um elemento relativamente resistente à corrosão e à oxidação, especialmente em sua forma metálica.
Contudo, sua toxicidade e impacto ambiental são preocupantes. Os compostos de cromo, especialmente
o cromo hexavalente, são tóxicos e carcinogênico, podendo causar sérios problemas de saúde e
ambientais.
Sobre o átomo de cromo sabemos que ele apresenta múltiplos estados de oxidação, sendo +3 e +6 os mais comuns, com base nesta informação em qual das espécies a seguir o átomo de cromo apresenta número de oxidação +3?
Sobre o átomo de cromo sabemos que ele apresenta múltiplos estados de oxidação, sendo +3 e +6 os mais comuns, com base nesta informação em qual das espécies a seguir o átomo de cromo apresenta número de oxidação +3?
Provas
Questão presente nas seguintes provas
“A amônia, apesar do seu tempo de vida relativamente curto, de aproximadamente 10 dias, é o terceiro
composto de nitrogênio mais abundante na atmosfera, ficando atrás apenas do N2e N2O. A sua
concentração é variável no espaço e no tempo, sendo os valores característicos na faixa de 0,1-10
mL/m3
. As principais fontes incluem a decomposição enzimática da ureia proveniente de urina e
excremento animais, emissão pelo solo, queima de biomassa e perdas durante a produção e aplicação
de fertilizantes, que representam a emissão global de cerca de 104,5 MtN (Megatonelada de Nitrogênio
106 ano como amônia”.
MARTINS, C. R. et al.; Ciclos Globais de Carbono, Nitrogênio e Enxofre: a importância na Química da Atmosfera. Cadernos Temáticos de Química Nova na Escola. Nº 5, Novembro, 2003, p.35.
Observando a fixação do Nitrogênio para a produção de amônia como indica a reação a seguir:
3H2(g) + N2 (g) ⇆ 2NH3(g)
Considere que na reação de fixação do nitrogênio para a produção de amônia, a uma temperatura de 500º C, a constante de equilíbrio (Kc) tem valor igual a 6,0 x10 -2 , imagine se, em um simulador de reator industrial a esta temperatura, há 0,250 mol dm-3 de H2 e 0,0500 mol dm-3 de NH3 presentes no equilíbrio, qual é a concentração de N2?
MARTINS, C. R. et al.; Ciclos Globais de Carbono, Nitrogênio e Enxofre: a importância na Química da Atmosfera. Cadernos Temáticos de Química Nova na Escola. Nº 5, Novembro, 2003, p.35.
Observando a fixação do Nitrogênio para a produção de amônia como indica a reação a seguir:
3H2(g) + N2 (g) ⇆ 2NH3(g)
Considere que na reação de fixação do nitrogênio para a produção de amônia, a uma temperatura de 500º C, a constante de equilíbrio (Kc) tem valor igual a 6,0 x10 -2 , imagine se, em um simulador de reator industrial a esta temperatura, há 0,250 mol dm-3 de H2 e 0,0500 mol dm-3 de NH3 presentes no equilíbrio, qual é a concentração de N2?
Provas
Questão presente nas seguintes provas
Muitos compostos contendo nitrogênio são encontrados na natureza, pois este elemento químico possui
grande capacidade de fazer ligações químicas, com números de oxidação variando de (–3) a (+5). É o
mais abundante elemento químico na atmosfera terrestre, contribuindo com aproximadamente 78% de
sua composição. A molécula de N2 é extremamente estável e quase não desempenha papel químico
importante, exceto na termosfera (altitude maior que 90 km) onde pode ser fotolizada ou ionizada. Os
constituintes minoritários, tais como óxido nitroso (N2O), óxido nítrico (NO), dióxido de nitrogênio (NO2),
ácido nítrico (HNO3) e amônia (NH3) são quimicamente reativos e têm importantes papéis nos problemas
ambientais contemporâneos, incluindo a formação e precipitação ácida (chuva ácida), poluição
atmosférica (smog fotoquímico), aerossóis atmosféricos e a depleção da camada de ozônio. Os óxidos de
nitrogênio, NO e NO2, são rapidamente interconversíveis e existem em equilíbrio dinâmico.
Assim, em experimento no laboratório, observando a reação do gás castanho NO2, um poluente do ar, e o gás incolor N2O4 que se encontram em equilíbrio, como indica a equação a seguir, foram adicionados em um reator de 5dm³, 0,625 mol de N2O4 e deixou-se decompor até atingir o equilibro com o NO2.
A concentração de equilíbrio do N2O4 obtida foi de 0,0750 M. Qual a constante de equilíbrio, kc, para esta reação?
2NO2 ⇄ N2O4
Assim, em experimento no laboratório, observando a reação do gás castanho NO2, um poluente do ar, e o gás incolor N2O4 que se encontram em equilíbrio, como indica a equação a seguir, foram adicionados em um reator de 5dm³, 0,625 mol de N2O4 e deixou-se decompor até atingir o equilibro com o NO2.
A concentração de equilíbrio do N2O4 obtida foi de 0,0750 M. Qual a constante de equilíbrio, kc, para esta reação?
2NO2 ⇄ N2O4
Provas
Questão presente nas seguintes provas
O amoníaco e seus sais são fertilizantes valiosos, a fabricação do amoníaco pela combinação direta do
N2 com o H2 constitui um dos principais equilíbrios químicos mais importantes para a civilização. E
através do estudo de equilíbrio químico podemos observar os fatores que afetam um equilíbrio químico e
como lidar com um equilíbrio quantitativamente. Assim, segundo o princípio de Le Chatelier: Quando uma
perturbação é aplicada em um sistema em equilíbrio dinâmico, ele tende a se ajustar para reduzir ao
mínimo o efeito da perturbação.
ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de química: questionando a vida moderna e o meio ambiente. 7. ed. Porto Alegre: Bookman, 2018.
Considerando a equação abaixo:
CO(g) + H₂O(g) ⇌ CO₂(g) + H₂(g) ΔH < 0
Qual das seguintes alternativas representa uma ação que levará ao aumento da produção de CO₂?
ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de química: questionando a vida moderna e o meio ambiente. 7. ed. Porto Alegre: Bookman, 2018.
Considerando a equação abaixo:
CO(g) + H₂O(g) ⇌ CO₂(g) + H₂(g) ΔH < 0
Qual das seguintes alternativas representa uma ação que levará ao aumento da produção de CO₂?
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container