Foram encontradas 1.768 questões.
Sabendo-se que, em soluções aquosas diluídas, 1 ppm equivale a 1 mg de soluto por litro de solução, que cálcio (Ca), estrôncio (Sr) e bário (Ba) são elementos que pertencem ao grupo 2A da tabela periódica, que o número atômico (Z) do carbono seja 6, que ZCa = 20, ZSr = 38 e ZBa = 56 e considerando que M CaCO3 = 100,1 g·mol-1 seja a massa molar do carbonato de cálcio, julgue o item a seguir.
Suponha-se que, na reação de formação de Ca(HCO3)2, 10,01 g de CaCO3 tenham reagido com 0,88 g de CO2 e 0,72 g de H2O. Nessa situação, é correto afirmar que a massa de bicarbonato de cálcio formada é superior a 3,4 g.
Provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
Sabendo-se que, em soluções aquosas diluídas, 1 ppm equivale a 1 mg de soluto por litro de solução, que cálcio (Ca), estrôncio (Sr) e bário (Ba) são elementos que pertencem ao grupo 2A da tabela periódica, que o número atômico (Z) do carbono seja 6, que ZCa = 20, ZSr = 38 e ZBa = 56 e considerando que M CaCO3 = 100,1 g·mol-1 seja a massa molar do carbonato de cálcio, julgue o item a seguir.
Segundo a teoria da repulsão dos pares de elétrons da camada de valência, o íon carbonato (CO32-) apresenta geometria trigonal plana.
Provas
Sabendo-se que, em soluções aquosas diluídas, 1 ppm equivale a 1 mg de soluto por litro de solução, que cálcio (Ca), estrôncio (Sr) e bário (Ba) são elementos que pertencem ao grupo 2A da tabela periódica, que o número atômico (Z) do carbono seja 6, que ZCa = 20, ZSr = 38 e ZBa = 56 e considerando que M CaCO3 = 100,1 g·mol-1 seja a massa molar do carbonato de cálcio, julgue o item a seguir.
Suponha-se que, em uma amostra de água natural de pH = 6,0, contendo o tampão de bicarbonato de potássio, a concentração de HCO3- seja 5,0 mol·L-1. Nesse caso, considerando-se que a constante de dissociação (Ka2) da reação de dissociação do íon HCO3- seja igual a 5.10-11 e pressupondo-se que a concentração de H2CO3 seja desprezível, é correto afirmar que a razão [HCO3-]/[CO32-] seja inferior a 1,5.104 mol·L-1.
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Sabendo-se que, em soluções aquosas diluídas, 1 ppm equivale a 1 mg de soluto por litro de solução, que cálcio (Ca), estrôncio (Sr) e bário (Ba) são elementos que pertencem ao grupo 2A da tabela periódica, que o número atômico (Z) do carbono seja 6, que ZCa = 20, ZSr = 38 e ZBa = 56 e considerando que M CaCO3 = 100,1 g·mol-1 seja a massa molar do carbonato de cálcio, julgue o item a seguir.
Considerando uma solução a 200 ppm em CaCO3, é correto afirmar que a concentração, em mol/L, de CaCO3 é superior a 2,5 x 10-3 mol.L-1.
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A rota sintética do composto alanina, preparada a partir do ácido 2-bromopropanoico, é representada pelo esquema a seguir.
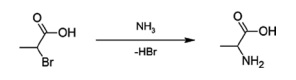
A partir dessas informações e supondo-se que uma solução foi preparada a partir de 0,89 g de alanina e 100 mL de água, e considerando-se que
M C3H7NO2 = 89 g·mol-1 e M H2O = 18 g·mol-1 sejam, respectivamente, as massas molares da alanina e da água, que a densidade da água seja 1 g/mL e que a constante universal dos gases seja 0,082 atm·L·mol-1·K-1, julgue o item seguinte.
A fração molar de alanina na solução preparada é inferior a 0,00190.
Provas
A rota sintética do composto alanina, preparada a partir do ácido 2-bromopropanoico, é representada pelo esquema a seguir.

A partir dessas informações e supondo-se que uma solução foi preparada a partir de 0,89 g de alanina e 100 mL de água, e considerando-se que
M C3H7NO2 = 89 g·mol-1 e M H2O = 18 g·mol-1 sejam, respectivamente, as massas molares da alanina e da água, que a densidade da água seja 1 g/mL e que a constante universal dos gases seja 0,082 atm·L·mol-1·K-1, julgue o item seguinte.
A alanina é um composto orgânico pertencente ao grupo dos aminoácidos.
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasPropriedades Coligativas: Tonoscopia, Ebulioscopia, Crioscopia e Pressão Osmótica.
A rota sintética do composto alanina, preparada a partir do ácido 2-bromopropanoico, é representada pelo esquema a seguir.

A partir dessas informações e supondo-se que uma solução foi preparada a partir de 0,89 g de alanina e 100 mL de água, e considerando-se que
M C3H7NO2 = 89 g·mol-1 e M H2O = 18 g·mol-1 sejam, respectivamente, as massas molares da alanina e da água, que a densidade da água seja 1 g/mL e que a constante universal dos gases seja 0,082 atm·L·mol-1·K-1, julgue o item seguinte.
A redução da temperatura de congelamento da água, após a dissolução de alanina, depende da molalidade da solução e, também, da natureza química da substância dissolvida.
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasPropriedades Coligativas: Tonoscopia, Ebulioscopia, Crioscopia e Pressão Osmótica.
A rota sintética do composto alanina, preparada a partir do ácido 2-bromopropanoico, é representada pelo esquema a seguir.

A partir dessas informações e supondo-se que uma solução foi preparada a partir de 0,89 g de alanina e 100 mL de água, e considerando-se que
M C3H7NO2 = 89 g·mol-1 e M H2O = 18 g·mol-1 sejam, respectivamente, as massas molares da alanina e da água, que a densidade da água seja 1 g/mL e que a constante universal dos gases seja 0,082 atm·L·mol-1·K-1, julgue o item seguinte.
A pressão osmótica da solução preparada será superior a 2,7 atm.
Provas
A rota sintética do composto alanina, preparada a partir do ácido 2-bromopropanoico, é representada pelo esquema a seguir.

A partir dessas informações e supondo-se que uma solução foi preparada a partir de 0,89 g de alanina e 100 mL de água, e considerando-se que
No que se refere à síntese da alanina, é correto afirmar que se trata de uma reação de eliminação.
Provas
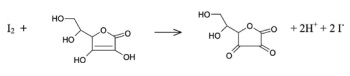
A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
Um composto da classe peróxido de metal alcalino reage com água produzindo uma base e H2O2. Caso reaja com um ácido diluído, os produtos obtidos serão sal e H2O2.
Provas
Caderno Container