Foram encontradas 775 questões.
Em um recipiente fechado com temperatura fixa, foram introduzidos nitrogênio gasoso (N2) e hidrogênio gasoso (H2) para
produzir amônia (NH3) como único produto. Após atingir o equilíbrio, as concentrações foram medidas e obtiveram-se os
seguintes valores: [N2] = 1,0 mol/L, [H2] = 2,0 mol/L e [NH3] = 3,0 mol/L. Com base nesses dados, assinale, a seguir, o valor
da constante de equilíbrio aproximada para a reação.
Provas
Questão presente nas seguintes provas
Uma solução de ácido sulfúrico foi submetida a um processo de eletrólise utilizando eletrodos inertes, durante um tempo de
2.100 segundos. O gás hidrogênio (H2) gerado no cátodo foi coletado sobre água, totalizando 6 mmol:
2e- + 2H+(aq) → H2(g)
Com base nos dados apresentados e, ainda, considerando a constante de Faraday como 96.500 C/mol, é correto afirmar que a corrente média aplicada durante a eletrólise foi de, aproximadamente:
2e- + 2H+(aq) → H2(g)
Com base nos dados apresentados e, ainda, considerando a constante de Faraday como 96.500 C/mol, é correto afirmar que a corrente média aplicada durante a eletrólise foi de, aproximadamente:
Provas
Questão presente nas seguintes provas
Em um laboratório de química industrial, o técnico André recebeu a tarefa de realizar a eletrólise de uma solução aquosa de
cloreto de sódio. O objetivo do experimento era gerar gás cloro no ânodo, de acordo com a semirreação:
2Cl−(aq) → Cl2(g) + 2e−
Para isso, André ajustou o equipamento para operar com uma corrente elétrica constante de 5,0 A, mantendo o sistema ativo por 1.930 segundos (~ 32 minutos). Considerando que a constante de Faraday é de 96.500 C/mol, a quantidade de matéria (mol) de gás cloro produzida foi de, aproximadamente:
2Cl−(aq) → Cl2(g) + 2e−
Para isso, André ajustou o equipamento para operar com uma corrente elétrica constante de 5,0 A, mantendo o sistema ativo por 1.930 segundos (~ 32 minutos). Considerando que a constante de Faraday é de 96.500 C/mol, a quantidade de matéria (mol) de gás cloro produzida foi de, aproximadamente:
Provas
Questão presente nas seguintes provas
A matéria é composta por partículas carregadas; portanto, não é surpreendente que seja possível converter energia química
em energia elétrica. Sobre os conceitos de eletroquímica, analise as afirmativas a seguir.
I. Nas células eletrolíticas, a energia química é convertida em energia elétrica.
II. Assim como a entropia, processos espontâneos são acompanhados por uma variação positiva na energia de Gibbs (∆G).
III. Ao multiplicar por dois a semirreação “Fe2+(aq) → Fe3+(aq) + e- ; E°= – 0,77V”, o valor do potencial padrão não deverá ser alterado.
Está correto o que se afirma apenas em
I. Nas células eletrolíticas, a energia química é convertida em energia elétrica.
II. Assim como a entropia, processos espontâneos são acompanhados por uma variação positiva na energia de Gibbs (∆G).
III. Ao multiplicar por dois a semirreação “Fe2+(aq) → Fe3+(aq) + e- ; E°= – 0,77V”, o valor do potencial padrão não deverá ser alterado.
Está correto o que se afirma apenas em
Provas
Questão presente nas seguintes provas
O equilíbrio químico é fundamental para entender reações reversíveis, permitindo prever concentrações de reagentes e produtos em sistemas químicos estáveis. Esse conceito é essencial em processos industriais, biológicos e ambientais, onde a eficiência
e o controle das reações são cruciais. Considerando os principais conceitos sobre o equilíbrio químico, assinale a afirmativa
correta.
Provas
Questão presente nas seguintes provas
A situação hipotética contextualiza a questão. Leia-a atentamente.
Determinado grupo de pesquisa desenvolveu um novo composto antineoplásico, codificado como XY-100. A síntese do fármaco
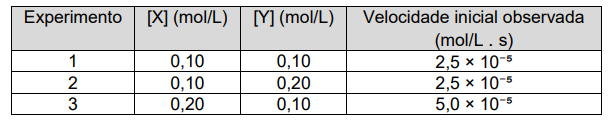
ocorre a partir dos reagentes X e Y, por meio de uma reação cujo comportamento cinético foi estudado e apresentado na tabela:
Dados de concentrações e velocidades iniciais coletadas para a síntese de XY-100:
Provas
Questão presente nas seguintes provas
A situação hipotética contextualiza a questão. Leia-a atentamente.
Determinado grupo de pesquisa desenvolveu um novo composto antineoplásico, codificado como XY-100. A síntese do fármaco
ocorre a partir dos reagentes X e Y, por meio de uma reação cujo comportamento cinético foi estudado e apresentado na tabela:
Dados de concentrações e velocidades iniciais coletadas para a síntese de XY-100:

Provas
Questão presente nas seguintes provas
A situação hipotética contextualiza a questão. Leia-a atentamente.
Determinado grupo de pesquisa desenvolveu um novo composto antineoplásico, codificado como XY-100. A síntese do fármaco
ocorre a partir dos reagentes X e Y, por meio de uma reação cujo comportamento cinético foi estudado e apresentado na tabela:
Dados de concentrações e velocidades iniciais coletadas para a síntese de XY-100:

Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Após preparar uma solução saturada de Mg(OH)2 e permitir que o equilíbrio químico fosse alcançado, o professor de química
mediu o pH da solução e registrou um valor de 9. Tendo em vista que toda a concentração de íons magnésio resulta
exclusivamente da dissociação da base, assinale, a seguir, a concentração aproximada de Mg2+ na solução.
Provas
Questão presente nas seguintes provas
Considere que o professor de química preparou uma solução tampão de acetato de sódio e ácido acético para uma aula sobre
equilíbrio químico ácido-base. Sabe-se que o pKa do ácido acético é 4,8 (Ka = 1,7 x 10-5) e que as concentrações usadas do sal
e do ácido foram de 3,0 mol/L e 0,3 mol/L, respectivamente. É correto afirmar o pH da solução preparada pelo professor é
de, aproximadamente:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container