Foram encontradas 775 questões.
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química CinéticaTransformações Químicas
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
A classificação periódica é uma forma de organização dos elementos químicos de modo a evidenciar algumas semelhanças em
suas propriedades físicas ou químicas. Vários estudiosos tentaram criar um sistema de classificação dos elementos. Os critérios
utilizados para a organização dos elementos foram estabelecidos ao longo do tempo. Sobre a tabela periódica, é INCORRETO
afirmar que:
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
No laboratório de química, o professor fez uma prática com os alunos. O objetivo da experiência era testar a condutividade
elétrica de diferentes compostos. No primeiro momento, colocou sobre a bancada sete recipientes identificados. Eram diferentes soluções que seriam analisadas. O professor pediu que, antes do teste de condutividade elétrica dos compostos, os
alunos prevessem quais soluções iriam acender a lâmpada e quais dos compostos não iriam acender. E dos que acendesse a
lâmpada, qual acenderia com maior intensidade.

De acordo com a resposta dos estudantes, analise as afirmativas a seguir.
I. Dentre as soluções dos três ácidos analisados, o ácido sulfúrico acende a lâmpada com maior intensidade.
II. Somente as soluções de sacarose e naftaleno não acendem a lâmpada.
III.Somente as soluções de sulfato de cálcio, etanol, ácido sulfúrico, ácido sulfídrico e ácido hipocloroso acendem a lâmpada.
Está correto o que se afirma em

De acordo com a resposta dos estudantes, analise as afirmativas a seguir.
I. Dentre as soluções dos três ácidos analisados, o ácido sulfúrico acende a lâmpada com maior intensidade.
II. Somente as soluções de sacarose e naftaleno não acendem a lâmpada.
III.Somente as soluções de sulfato de cálcio, etanol, ácido sulfúrico, ácido sulfídrico e ácido hipocloroso acendem a lâmpada.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
- Química CinéticaVelocidade de Reação, Energia de Ativação e Catalisadores
- Química OrgânicaGlicídios, Lipídios, Aminoácidos e Proteínas.
O colesterol é um composto normalmente produzido no fígado e que tem um papel importante em vários aspectos do
metabolismo dos organismos animais, sendo precursor de vários hormônios. Faz parte da produção de hormônios, vitamina
D e ácidos biliares que atuam na digestão e na absorção das gorduras no intestino. Porém, em taxas elevadas, o colesterol
aumenta o risco de complicações como diabetes e doenças cardiovasculares como infarto e derrame:
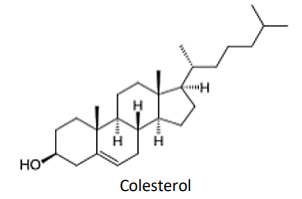
Quantos gramas de água são produzidos na oxidação de 6 g de colesterol?

Quantos gramas de água são produzidos na oxidação de 6 g de colesterol?
Provas
Questão presente nas seguintes provas
Em sua aula de química, o professor almejou aplicar um desafio para os estudantes. Pediu para que os alunos se reunissem
em quatro grupos e, para cada grupo, entregou a folha com o desafio descrito:
Desafio:
Com a fórmula C5H8 podem ser formados quantos alquinos? E com a fórmula C3H7NO podem ser formadas quantas amidas?
Após o professor marcar um tempo para que os estudantes pudessem responder o desafio, ele recolheu as respostas. Como teria dois tempos na turma, resolveu comentar as respostas dadas pelos grupos:

Qual dos grupos acertou o desafio proposto pelo professor?
Desafio:
Com a fórmula C5H8 podem ser formados quantos alquinos? E com a fórmula C3H7NO podem ser formadas quantas amidas?
Após o professor marcar um tempo para que os estudantes pudessem responder o desafio, ele recolheu as respostas. Como teria dois tempos na turma, resolveu comentar as respostas dadas pelos grupos:

Qual dos grupos acertou o desafio proposto pelo professor?
Provas
Questão presente nas seguintes provas
Em sua aula de química, o professor explicava para os estudantes sobre as propriedades dos compostos orgânicos. Ao terminar a explicação, ele passou na lousa uma atividade. Uma aluna conseguiu desenvolver rapidamente o exercício e pediu para
o professor se ela podia responder o que tinha feito. O professor, então, pediu para ela descrever na lousa suas respostas.
Ao escrever na lousa suas respostas, o professor percebeu que ela cometeu erro(s).
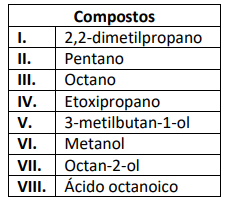
1.Dentre os pares de compostos listados a seguir, indique qual deve apresentar maior temperatura de ebulição:
a) I e II.
b) IV e V.
c) III e VI.
2.Dentre os pares de compostos listados a seguir, indique qual deve ser mais solúvel em água:
a) VI e VII.
b) VII e VIII.
c) I e IV.
Resposta da aluna:
1.
a) I.
b) V.
c) VI.
2.
a) VI.
b) VIII.
c) IV.
Quantos erros a estudante cometeu?

1.Dentre os pares de compostos listados a seguir, indique qual deve apresentar maior temperatura de ebulição:
a) I e II.
b) IV e V.
c) III e VI.
2.Dentre os pares de compostos listados a seguir, indique qual deve ser mais solúvel em água:
a) VI e VII.
b) VII e VIII.
c) I e IV.
Resposta da aluna:
1.
a) I.
b) V.
c) VI.
2.
a) VI.
b) VIII.
c) IV.
Quantos erros a estudante cometeu?
Provas
Questão presente nas seguintes provas
- Interações com Tecnologia, Sociedade e Meio Ambiente
- Química InorgânicaSoluções e Substâncias Inorgânicas
A chuva ácida, uma das manifestações da poluição atmosférica, é formada pela interação entre alguns óxidos – como o
trióxido de enxofre e o dióxido de nitrogênio – com a água da própria chuva, formando ácidos que são depositados na
superfície terrestre através das precipitações. Essa acidificação do solo e das águas superficiais exerce efeitos devastadores
nos ecossistemas e representa um grave perigo para os seres vivos. Diante do exposto, analise as afirmativas a seguir.
I. Os ácidos formados pela interação entre o trióxido de enxofre e o dióxido de nitrogênio com a água é ácido sulfúrico, ácido nítrico e ácido nitroso.
II. A equação química que representa a interação do dióxido de nitrogênio com a água é 2 NO2(g) + H2O(l) → HNO3(aq) + HNO2(aq).
III. Os óxidos trióxido de enxofre e o dióxido de nitrogênio são óxidos ácidos.
Está correto o que se afirma em
I. Os ácidos formados pela interação entre o trióxido de enxofre e o dióxido de nitrogênio com a água é ácido sulfúrico, ácido nítrico e ácido nitroso.
II. A equação química que representa a interação do dióxido de nitrogênio com a água é 2 NO2(g) + H2O(l) → HNO3(aq) + HNO2(aq).
III. Os óxidos trióxido de enxofre e o dióxido de nitrogênio são óxidos ácidos.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
- Química OrgânicaHidrocarbonetos
- Química OrgânicaPropriedades Físicas dos Compostos Orgânicos
- Química OrgânicaPropriedades Químicas dos Compostos Orgânicos
A historionicotoxina é uma toxina letal encontrada na pele do sapo arlequim. Esses sapos foram usados durante muito tempo
pelos nativos da América do Sul para envenenar suas flechas usadas em caças. O hidrato de saxitoxina é outra toxina, isolada
de algumas algas:
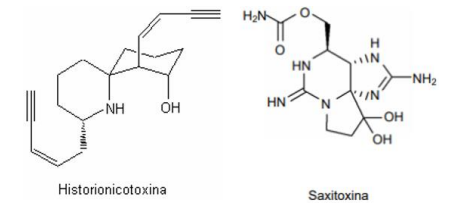
Sobre as estruturas das toxinas citadas, analise as afirmativas a seguir.
I. As funções orgânicas presentes na estrutura da historionicotoxina é álcool e amina.
II. A massa molar da historionicotoxina é 257 g/mol.
III. A saxitoxina é mais solúvel em água do que a histrionicotoxina.
Está correto o que se afirma em

Sobre as estruturas das toxinas citadas, analise as afirmativas a seguir.
I. As funções orgânicas presentes na estrutura da historionicotoxina é álcool e amina.
II. A massa molar da historionicotoxina é 257 g/mol.
III. A saxitoxina é mais solúvel em água do que a histrionicotoxina.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
O alaranjado de metila é um corante azoico também conhecido como amarelo-manteiga. É utilizado como indicador em
titulações ácido-base, apresentando coloração vermelha em pH menor que 3,1 e amarela em pH maior que 4,4.
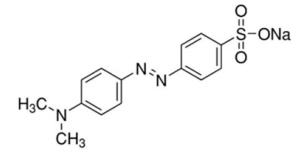
O número de átomos de H em 0,203 mol de alaranjado de metila é:

O número de átomos de H em 0,203 mol de alaranjado de metila é:
Provas
Questão presente nas seguintes provas
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química Cinética
- Transformações Químicas e EnergiaRadioatividade
As reações nucleares são muito empregadas tanto para gerar eletricidade quanto para criar armas de destruição em massa.
Elas são usadas também para ajudar a determinar os mecanismos de reações químicas, para investigar o movimento de
átomos em sistemas biológicos e para achar a idade de importantes artefatos históricos. A química nuclear é fundamental
para o desenvolvimento da energia nuclear. A química proporciona as técnicas de preparação e recirculação dos combustíveis
nucleares, e de remoção de resíduos radioativos perigosos. Sobre a química nuclear, marque V para as afirmativas verdadeiras e F para as falsas.
( ) Quando o núcleo de urânio-238 perde uma partícula alfa, o fragmento restante tem número atômico 90 e número de massa 234.
( ) Para transformar urânio-238 em rádio-226 foram emitidas 3 partículas beta (β).
( ) A radiação gama consiste em fótons de alta energia; muda a massa e o número atômico de um núcleo.
( ) Quando o rádio-226 sofre decaimento alfa o produto formado é 86Rn222.
A sequência está correta em
( ) Quando o núcleo de urânio-238 perde uma partícula alfa, o fragmento restante tem número atômico 90 e número de massa 234.
( ) Para transformar urânio-238 em rádio-226 foram emitidas 3 partículas beta (β).
( ) A radiação gama consiste em fótons de alta energia; muda a massa e o número atômico de um núcleo.
( ) Quando o rádio-226 sofre decaimento alfa o produto formado é 86Rn222.
A sequência está correta em
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Um professor de química, ao chegar em sua sala de aula, introduziu o conteúdo com a seguinte pergunta: por que o gelo
flutua? E prosseguiu: como ocorre na maioria das substâncias, a fase sólida da parafina é mais densa que a líquida e, por isso,
o sólido afunda sob a superfície do líquido. Em contraste, a fase sólida da água, o gelo, é menos densa que a sua fase líquida,
fazendo com que o gelo flutue na água. A explicação está relacionada aos conceitos de interações intermoleculares e ao
arranjo das moléculas. Então, por que a densidade do gelo é menor do que a densidade da água? Sobre a explicação do
questionamento do professor, analise as afirmativas a seguir.
I. Quando a água congela, as moléculas assumem o arranjo hexagonal aberto e ordenado. Esse arranjo otimiza as interações de ligação de hidrogênio entre as moléculas e cria uma estrutura menos densa para o gelo se comparada com a da água.
II. A densidade mais baixa do gelo comparada com a da água pode ser entendida em termos das interações de ligação de hidrogênio entre as moléculas de água.
III. Uma determinada massa de gelo ocupa maior volume que a mesma massa de água líquida.
Está correto o que se afirma em
I. Quando a água congela, as moléculas assumem o arranjo hexagonal aberto e ordenado. Esse arranjo otimiza as interações de ligação de hidrogênio entre as moléculas e cria uma estrutura menos densa para o gelo se comparada com a da água.
II. A densidade mais baixa do gelo comparada com a da água pode ser entendida em termos das interações de ligação de hidrogênio entre as moléculas de água.
III. Uma determinada massa de gelo ocupa maior volume que a mesma massa de água líquida.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container