Foram encontradas 60 questões.
Uma solução ácida contendo La3+ em concentração 0,010 mol.L-1 é tratada com NaOH até a precipitação de La(OH)3. O pH no qual a precipitação do hidróxido deve iniciar é:
Dados: pKps (La(OH)3) = 20,7; Kw = 1,0x10–14.
Provas
O fluxograma a seguir sumariza os resultados obtidos por um técnico na pesquisa de cátions do grupo I.
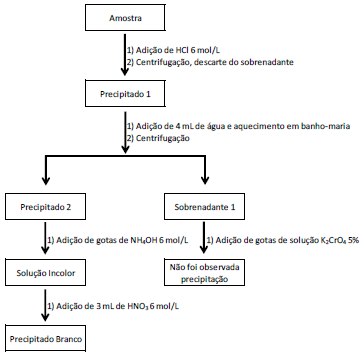
A análise deste fluxograma permite concluir que, na amostra, possivelmente está presente o cátion
Provas
A Termodinâmica é a área da físico-química que estuda as relações entre coordenadas como temperatura, volume e pressão e o comportamento de substâncias puras e misturas em processos específicos.
A Primeira Lei da Termodinâmica diz que a variação da energia interna de um sistema pode ser expressa através da diferença entre o calor trocado com o meio externo e o trabalho realizado por ele durante uma determinada transformação. Potenciais termodinâmicos permitem a avaliação da espontaneidade de transformações físico-químicas.
A esse respeito, analise as afirmativas a seguir:
I. A variação da energia interna de um gás ideal em um processo isotérmico é necessariamente nula.
II. É possível estabelecer a relação CvdT = -PdV para um gás ideal em sistema isolado sofrendo uma transformação adiabática, onde Cv é a capacidade calorífica a volume constante, P é a pressão e dT e dV são variações infinitesimais de temperatura e volume, respectivamente.
III. Um processo endotérmico espontâneo não ocorre com aumento de entropia.
Assinale:
Provas
Um resíduo pode ser classificado a partir das características de seus constituintes. Os resíduos perigosos são classificados considerando suas características de inflamabilidade, corrosividade, reatividade e patogenicidade e recebem, respectivamente os códigos D001, D002, D003 e D004.
Os componentes presentes em grande quantidade em quatro resíduos distintos, estão listados na tabela a seguir
| Resíduo | I | II | III | IV |
| Componente | Perclorato de amônio | Metanol |
Hipoclorito de sódio |
Soda cáustica |
Os códigos relacionados a estes resíduos são:
Provas
Analise o fragmento a seguir.
“Na equação balanceada correspondente à reação de oxidação do naftaleno com permanganato de potássio em meio básico, formando o-ftalato e carbonato além do dióxido de manganês, observa-se que mols de permanganato são necessários para oxidar um mol de naftaleno, com transferência de mols elétrons.”
Assinale a opção que preenche, corretamente, as lacunas do fragmento acima.
Provas
A Química Ambiental envolve o estudo das fontes, das transformações e dos efeitos de diversas espécies na atmosfera, na geosfera, na antroposfera e na hidrosfera. Os ciclos químicos da matéria são importantes para o estudo ambiental; o ciclo do enxofre envolve intercâmbios entre espécies microbiológicas, gasosas, solúveis e insolúveis.
Uma parte do ciclo do enxofre está esquematizada de forma simplificada a seguir:
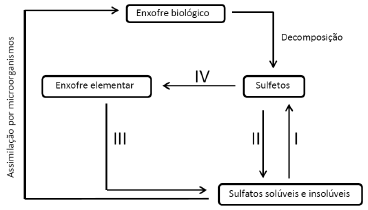
Neste ciclo, I, II, III e IV representam, respectivamente, processos de:
Provas
A estocagem dos materiais usados em laboratório deve obedecer a critérios de segurança que estão relacionados com as propriedades de cada material, com a segurança do local e com a compatibilidade entre as substâncias. Áreas separadas devem ser utilizadas para armazenar substâncias incompatíveis que podem reagir perigosamente.
Propriedades como temperatura de ebulição e ponto de fulgor devem ser conhecidas quando líquidos inflamáveis forem estocados. Na área de estocagem de líquidos inflamáveis deve estar disponível o extintor de incêndio adequado e junto com esses não podem ser armazenados
Provas
Para a reação
2 N2O5(g) → 4 NO2(g) + O2(g), a 298K, é 3,38x10–5s–1.
Considerando a cinética desta reação, assinale V a afirmativa verdadeira e F para a falsa.
( ) Espera-se um decaimento exponencial do reagente, uma vez que a lei de velocidade da reação pode ser expressa por v = k [N2O5].
( ) A reação segue a cinética de segunda ordem.
( ) Um catalisador apropriado poderá aumentar a velocidade da reação uma vez que diminui a diferença de energia livre de Gibbs da reação.
As afirmativas são, respectivamente,
Provas
O ácido glutâmico é um aminoácido não essencial, representado pela fórmula a seguir.
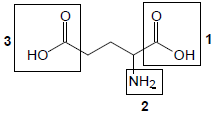
Os grupos destacados como 1, 2 (esse na forma NH3+) e 3 apresentam, respectivamente, valores de pKa iguais a 2,2; 9,6 e 4,2. Em pH igual a 6, as formas iônicas presentes correspondem à
Provas
Os ácidos graxos naturais possuem longas cadeias carbônicas, normalmente não ramificadas com números pares de carbonos.
Os ácidos behénico (ácido docosanoico, C22H44O2), erúcico (ácido cis-13-docosenoico, C22H42O2), brassídico (ácido trans-13- docosenoico, C22H42O2) e oleico (ácido cis-9-ocatadecenoico, C18H34O2) são exemplos de ácidos graxos de ocorrência natural, cujas temperaturas de fusão estão relacionadas com suas estruturas.
A ordem crescente das temperaturas de fusão destes compostos é
Provas
Caderno Container