Foram encontradas 60 questões.
A acidez do vinho é expressa em termos da concentração de ácido tartárico, cuja fórmula estrutural é representada abaixo.
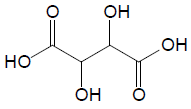
Para a determinação da acidez, 25,00mL de amostra de vinho branco foram transferidos para Erlenmeyer. Adicionou-se 100mL de água e gotas de fenolftaleína e titulou-se contra solução padronizada de NaOH 0,100mol.L-1. Foram necessários 20,00mL de solução da base na titulação.
A acidez da amostra (em unidades de gramas de ácido tartárico/100mL) é:
Dado: Massa molar do ácido tartárico: 150g.mol-1.
Provas
Para a determinação de ferro em cerveja, 10,00 mL de amostra foram transferidos para erlenmeyer.
Após desgaseificar a amostra, adicionou-se 3 mL de mistura ácida (HNO3 + H2SO4 + HC!$ \ell !$O4) e a solução foi aquecida em placa de aquecimento. Foram feitas novas adições de 1 mL da mistura ácida durante o procedimento de digestão, até que a solução final se mostrasse incolor.
A solução final, após atingir a temperatura ambiente, foi transferida para balão volumétrico de 50,00 mL, completando o volume com água ultrapura. 10,00 mL da solução final foram transferidos para tubo de ensaio e esta solução foi submetida à determinação de ferro por espectrometria de absorção atômica, apresentando absorvância 0,150.
A curva de calibração é fornecida a seguir.

O teor de ferro na amostra de cerveja, em mg.L–1, é:
Provas
O teor de Ca2+ em amostra de urina foi determinado a partir das seguintes etapas:
1. Precipitação do cátion por adição de excesso de solução padrão de C2O42- 0,010 mol.L-1 a 5,00 mL de amostra de urina.
2. Lavagem do precipitado com água gelada para remoção do oxalato livre e ressolubilização do sólido com solução ácida.
3. Titulação do H2C2O4 em solução utilizando solução padrão de MnO4- 0,0010 mol.L-1.
Após tratamento do precipitado, foram gastos 15,00 mL de solução de MnO4- para a titulação do H2C2O4.
A concentração de Ca2+ na amostra, em mol.L-1, é
Provas
Uma amostra de K2SO4 comercial, contaminada com !$ KC\ell !$, foi submetida a um ensaio gravimétrico para a determinação de sua pureza. Assim, 1,148g da amostra foi dissolvido em água e tratada com solução de Ba(NO3)2. O precipitado, após os cuidados necessários, foi pesado sendo observada a massa 1,398g.
O teor de K2SO4 na amostra é
Dados: Massas molares K2SO4 = 174g.mol–1 !$ KC\ell !$= 74,5g.mol–1 BaSO4 = 233g.mol–1
Provas
A Demanda Química de Oxigênio, DQO, é um parâmetro indispensável nos estudos de caracterização de esgotos sanitários e de efluentes industriais.
Um efluente, caracterizado com DQO de 1032 mg O2/L, é lançado sem tratamento prévio em uma lagoa. A quantidade de matéria orgânica nesse efluente
Provas
O oxigênio dissolvido é um parâmetro relevante para a avaliação da qualidade de um corpo d’água. A quantidade de oxigênio dissolvido é importante para a manutenção da vida no ambiente aquático. As águas poluídas possuem baixa concentração de oxigênio dissolvido, ao contrário de águas limpas.
As tabelas a seguir relacionam a concentração de oxigênio dissolvido com a classificação das águas e sua utilização.
|
Oxigênio dissolvido (mg.L-1) |
Classes | ||||
| Especial | I | II | III | IV | |
| 6 | 6 | 5 | 4 | 2 | |
| Classes |
Utilização da água |
|
Especial |
Própria para abastecimento humano após desinfecção |
| I |
Própria para abastecimento humano após tratamento simplificado |
| II |
Própria para abastecimento humano após tratamento convencional |
| III |
Própria para abastecimento humano após tratamento avançado |
| IV |
Própria para navegação |
De acordo com a tabela, um corpo d’água que apresenta 5 x 10–5mol de oxigênio dissolvido por litro de água pode ser utilizado para
Dado: Massa molar O = 16g.mol–1
Provas
Um material de referência, certificado para fluoreto em 1,06mg.L 1, foi analisado em um laboratório por três metodologias diferentes. Foram analisadas 6 réplicas em cada método analítico.
As médias dos resultados (em mg.L–1) são apresentados a seguir:
|
Método de análise |
Média ± Desvio padrão |
|
Cromatografia de Íons |
1,11 ± 0,02 |
|
Espectrofotometria |
1,12 ± 0,07 |
|
Potenciometria (eletrodo de íon seletivo) |
1,07 ± 0,04 |
Analisando os resultados, é correto afirmar que o método
Provas
O espectro de ultravioleta visível de uma solução com concentração 9,9 x 10–5mol.L–1 de uma hidróxi-naftoquinona de origem natural foi obtido numa cubeta de caminho óptico de 1 cm. No comprimento de onda correspondente a 330nm, o composto apresentou absorbância igual a 0,320.
Para determinar a concentração de uma segunda solução do mesmo composto, foi obtido, nas mesmas condições, um espectro que em 330nm apresentou absorbância igual 0,480. Nas condições nas quais os espectros foram obtidos as amostras obedecem à lei de Lambert-Beer.
A segunda solução, nas condições da análise, apresentou concentração (em mol.L–1) igual a
Provas
Ao ser dissolvido em água, um composto iônico tem seus íons envoltos por moléculas de água formando os íons hidratados. O íon alumínio hexaidratado [A!$ \ell !$(H2O)6]3+ é uma das formas desse cátion hidratado presente em solução aquosa de um sal de alumínio. Esse íon apresenta o seguinte equilíbrio em água:
[A!$ \ell !$(H2O)6]3+(aq) + H2O!$ \leftrightarrows !$ [A!$ \ell !$(H2O)5(OH)]2+(aq) + H3O+(aq)
Nesse equilíbrio a espécie [A!$ \ell !$(H2O)6]3+ se comporta como
Provas
Rudolph Diesel criou um motor a combustão interna cujo combustível era o óleo de amendoim, mas esse óleo vegetal é muito viscoso e entope o motor. Uma alternativa para resolver este problema é utilizar os produtos da reação representada a seguir que podem ser usados com poucas alterações do motor e não causam o entupimento.
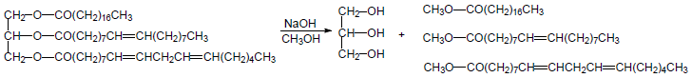
A reação apresentada pode ser classificada como uma
Provas
Caderno Container