Foram encontradas 120 questões.
A limitada solubilidade em água de muitos compostos iônicos é explorada na separação de íons por precipitação fracionada. Por exemplo, o ânion sulfeto \(S^{2-}\) costuma formar compostos pouco solúveis com cátions de metais pesados e a diferença de solubilidade dos sais formados permite a separação desses cátions. Nesse processo, a solução aquosa contendo os cátions é mantida saturada em ácido sulfídrico \(H_2S\) e, por meio de manipulação do pH, é possível controlar a concentração de íons sulfeto e, dessa forma, a precipitação dos compostos.
| \(CdS_{(s)} \leftrightarrow Cd^{2+}_{(aq)} + S^{2-}_{(aq)}\) | \(K_{\text{ps}} = 1 \times 10^{-27}\) |
| \(Tl_2S_{(s)} \leftrightarrow 2 Tl^{+}_{(aq)} + S^{2-}_{(aq)}\) | \(K_{\text{ps}} = 6 \times 10^{-22}\) |
| \(H_2S_{(aq)} + 2 H_2O_{(l)} \leftrightarrow 2 H_3O^{+}_{(aq)} + S^{2-}_{(aq)}\) | \(K_{\text{a}} = 1,2 \times 10^{-21}\) |
Considerando o assunto em questão e os dados fornecidos acima, julgue os próximos itens.
Desconsiderando eventuais desvios da idealidade, a solubilidade do \(CdS\) em uma solução aquosa de \(CdCl_2\ 1,00 \times 10^{-4}\text{mol/L}\) é igual a \(\sqrt{1 \times 10^{-27}}\text{mol/L}\).
Provas

Provas

Provas

Provas

Tendo como base a titulação em questão, a figura apresentada e os dados fornecidos, julgue os itens que se seguem.
Provas

Tendo como base a titulação em questão, a figura apresentada e os dados fornecidos, julgue os itens que se seguem.
Provas

Tendo como base a titulação em questão, a figura apresentada e os dados fornecidos, julgue os itens que se seguem.
Provas

Tendo como base a titulação em questão, a figura apresentada e os dados fornecidos, julgue os itens que se seguem.
Provas
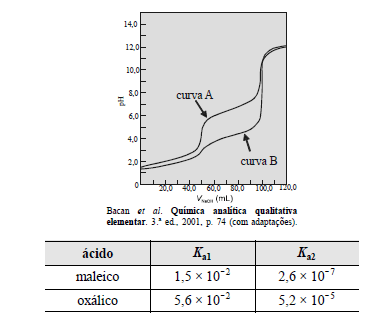
A figura acima apresenta as curvas de titulação de neutralização de 40,0 mL de soluções aquosas de ácido maleico e ácido oxálico, com concentrações iguais, com uma solução aquosa de NaOH 0,100 mol/L. A primeira e a segunda constantes de ionização desses ácidos (Ka1 e Ka2, respectivamente) encontram-se listadas na tabela acima. Com base nos dados fornecidos, julgue os itens de 54 a 57.
Provas

A figura acima apresenta as curvas de titulação de neutralização de 40,0 mL de soluções aquosas de ácido maleico e ácido oxálico, com concentrações iguais, com uma solução aquosa de NaOH 0,100 mol/L. A primeira e a segunda constantes de ionização desses ácidos (Ka1 e Ka2, respectivamente) encontram-se listadas na tabela acima. Com base nos dados fornecidos, julgue os itens de 54 a 57.
Provas
Caderno Container