Foram encontradas 120 questões.
O pH de uma solução aquosa (solução problema) foi medido utilizando-se uma célula eletroquímica constituída por um eletrodo de calomelano (eletrodo de referência) e um eletrodo de vidro. A calibração da célula foi feita medindo-se o potencial da célula quando o eletrodo de vidro foi mergulhado em uma solução tampão de pH conhecido. Na temperatura em que os procedimentos foram realizados, \(\dfrac{RT}{F}\ln_{x} = 0,05916\log{x}\), em que R representa a constante universal dos gases; T, a temperatura absoluta; e F, a constante de Faraday.
Com referência à célula eletroquímica referida no texto e considerando os dados fornecidos, julgue os itens que se seguem.
Provas
O pH de uma solução aquosa (solução problema) foi medido utilizando-se uma célula eletroquímica constituída por um eletrodo de calomelano (eletrodo de referência) e um eletrodo de vidro. A calibração da célula foi feita medindo-se o potencial da célula quando o eletrodo de vidro foi mergulhado em uma solução tampão de pH conhecido. Na temperatura em que os procedimentos foram realizados, \(\dfrac{RT}{F}\ln_{x} = 0,05916\log{x}\), em que R representa a constante universal dos gases; T, a temperatura absoluta; e F, a constante de Faraday.
Com referência à célula eletroquímica referida no texto e considerando os dados fornecidos, julgue os itens que se seguem.
Provas
O pH de uma solução aquosa (solução problema) foi medido utilizando-se uma célula eletroquímica constituída por um eletrodo de calomelano (eletrodo de referência) e um eletrodo de vidro. A calibração da célula foi feita medindo-se o potencial da célula quando o eletrodo de vidro foi mergulhado em uma solução tampão de pH conhecido. Na temperatura em que os procedimentos foram realizados, \(\dfrac{RT}{F}\ln_{x} = 0,05916\log{x}\), em que R representa a constante universal dos gases; T, a temperatura absoluta; e F, a constante de Faraday.
Com referência à célula eletroquímica referida no texto e considerando os dados fornecidos, julgue os itens que se seguem.
A reação química que se passa no eletrodo de calomelano é a seguinte: \(Hg_2 Cl_{2(s)} + 2e^{-} \rightarrow 2Hg_{(l)} + 2Cl^-_{(aq)}\).
Provas
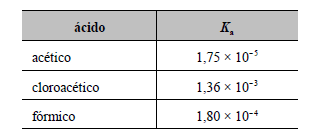
Julgue os itens a seguir, considerando os ácidos listados na tabela acima, suas respectivas constantes de ionização (Ka), e que log (1,80 × 10-4) = -3,7 e log 2 = 0,3.
Provas

Julgue os itens a seguir, considerando os ácidos listados na tabela acima, suas respectivas constantes de ionização (Ka), e que log (1,80 × 10-4) = -3,7 e log 2 = 0,3.
Provas
Com respeito ao procedimento descrito e levando-se em conta as massas molares fornecidas acima, julgue os itens a seguir.
Provas
Com respeito ao procedimento descrito e levando-se em conta as massas molares fornecidas acima, julgue os itens a seguir.
Provas
Com respeito ao procedimento descrito e levando-se em conta as massas molares fornecidas acima, julgue os itens a seguir.
Provas
Com respeito ao procedimento descrito e levando-se em conta as massas molares fornecidas acima, julgue os itens a seguir.
Provas
A limitada solubilidade em água de muitos compostos iônicos é explorada na separação de íons por precipitação fracionada. Por exemplo, o ânion sulfeto \(S^{2-}\) costuma formar compostos pouco solúveis com cátions de metais pesados e a diferença de solubilidade dos sais formados permite a separação desses cátions. Nesse processo, a solução aquosa contendo os cátions é mantida saturada em ácido sulfídrico \(H_2S\) e, por meio de manipulação do pH, é possível controlar a concentração de íons sulfeto e, dessa forma, a precipitação dos compostos.
| \(CdS_{(s)} \leftrightarrow Cd^{2+}_{(aq)} + S^{2-}_{(aq)}\) | \(K_{\text{ps}} = 1 \times 10^{-27}\) |
| \(Tl_2S_{(s)} \leftrightarrow 2 Tl^{+}_{(aq)} + S^{2-}_{(aq)}\) | \(K_{\text{ps}} = 6 \times 10^{-22}\) |
| \(H_2S_{(aq)} + 2 H_2O_{(l)} \leftrightarrow 2 H_3O^{+}_{(aq)} + S^{2-}_{(aq)}\) | \(K_{\text{a}} = 1,2 \times 10^{-21}\) |
Considerando o assunto em questão e os dados fornecidos acima, julgue os próximos itens.
Provas
Caderno Container