Foram encontradas 858 questões.
As cirurgias no globo geram dor e, em alguns casos, inflamação após o procedimento. Um anestésico de ação local, à base de procaparacaína, tem sido utilizado nestas intervenções e tem diminuído as complicações no pós-operatório. Um método de síntese da proparacaína envolve inicialmente a reação.
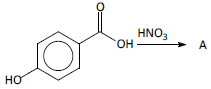
A estrutura do composto representado por A é:
Provas
A indústria química utiliza a fluorita (CaF2)para a obtenção do flúor elementar, de diversos produtos químicos designados genericamente de fluoroquímicos e do ácido fluorídrico (HF). O fluoreto de cálcio apresenta baixa solubilidade em água e sua constante do produto de solubilidade a 25ºC, é 3,9 x 10–11.
A solubilidade do fluoreto de cálcio em uma solução 0,10 mol.L–1 de fluoreto de sódio nessa temperatura é, em mol.L–1:
Provas
As constantes físico-químicas de um lago foram estudadas em um determinado período do ano e demonstraram sua estratificação. A superfície deste lago, chamada de epilíminio, apresentou altas concentrações de oxigênio dissolvido e alta atividade fotossintética; próximo ao fundo deste lago, no hipolíminio a água apresentou baixas concentrações de oxigênio e material biológico em decomposição. As espécies químicas sulfeto de hidrogênio, dióxido de carbono, metano, sulfato, nitrato e amônio foram encontradas neste lago.
De acordo com o enunciado, as espécies químicas citadas, encontradas no epilíminio e no hipolíminio foram:
Provas
O dióxido de enxofre é um gás utilizado na produção do ácido sulfúrico. Esse gás é emitido na queima de combustíveis e pode ser muito prejudicial à saúde e ao meio ambiente. Para analisar a presença de dióxido de enxofre em um determinado local, uma amostra de ar foi borbulhada em 500 mL de um meio que promoveu a conversão total do dióxido de enxofre em sulfato.
A amostra resultante foi analisada em um cromatógrafo iônico em condições apropriadas, na mesma temperatura, demonstrando que a concentração de sulfato presente corresponde a 1 mmol . L–1.
A massa (em mg) de dióxido de enxofre presente na amostra é:
Dados: Massa molares (g.mol–1) S = 32 e O = 16
Provas
A poluição causada pelo íon nitrato é um problema em algumas áreas agrícolas. Existem evidências de que o solo de fazendas de criação de gado possa ser contaminado pelos despejos nitrogenados do próprio rebanho. O íon nitrato pode também ser ingerido pelo animal e no seu estômago ser reduzido a nitrito que é tóxico.
A reação de formação de nitrito descrita no texto é representada pela equação:
Provas
O Bi3+ pode ser determinado através da formação de BiOI (oxiiodeto), neste método a solução fria contendo nitrato de bismuto (III) deve ser levemente acidulada com ácido nítrico e em seguida deve ser feita lentamente e com agitação, a adição de iodeto de potássio na forma de pó para que ocorra formação do BiI3 (triiodeto de bismuto) que em seguida é fervido com água quente. Neste procedimento é formado um precipitado de BiOI cor de cobre que deve ser filtrado, lavado com água e secado a cerca de 110ºC até peso constante e em seguida pesado.
Utilizando o método descrito em condições apropriadas, a quantidade de Bi3+ em uma amostra contendo nitrato de bismuto (III) foi determinada através da formação de um precipitado de BiOI, que após lavagem e secagem pesou 0,1g. Nestas condições, a massa (em miligramas) de Bi3+ presente na amostra é, aproximadamente:
Dados: Massa molares (g.mol–1) Bi = 209; Bi(NO3)3 = 395 e BiOI = 352
Provas
A célula eletroquímica hipotética, representada por
X (s) │ X2+ (1,00 mol.L–1) ││ Cu2+ (0,01 mol.L–1) │ Cu (s)
apresentou potencial igual 0,686 volts.
Esta célula hipotética foi construída por duas semi-células, uma formada por um eletrodo desconhecido imerso em uma solução de concentração 1,00 mol.L–1 contendo seus cátions X2+ e outra formada por um eletrodo de cobre imerso em uma solução diluída com íons Cu2+ na concentração 0,01 mol.L–1. Nas condições do enunciado, os eletrodos apresentam os potenciais padrão:
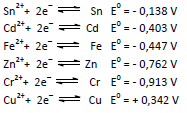
Nestas condições, X é o
Provas
Uma ampla variedade de compostos químicos utilizados como herbicida apresenta alto potencial de contaminação de águas subterrâneas.
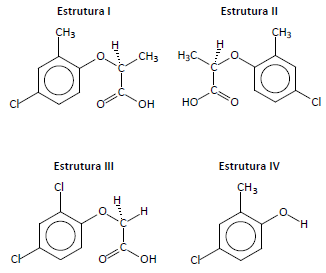
Os compostos, cujas estruturas estão representadas acima, fazem parte de uma formulação comercializada para aplicação em cultivos de trigo e cevada.
Analise as estruturas e assinale a afirmativa correta.
Provas
As propriedades químicas de uma substância podem se relacionar com o seu pKa determinado por métodos simples como titulação, condutimetria e ultravioleta. Os valores dos pKa de três ácidos carboxílicos foram determinados: ácido benzóico (I), ácido-pmetil- benzóico (II) e ácido-p-cloro-benzóico (III).
A ordem crescente dos pKa desses ácidos é
Provas
Um químico preparou, para neutralizar o rejeito de uma reação, uma solução básica de hidróxido de sódio dissolvendo óxido de sódio puro em água, em um balão volumétrico de 250 mL. Uma alíquota de 25 mL desta solução foi transferida para outro balão volumétrico e diluída com água até 500 mL. A solução resultante apresentou pH igual a 13.
No preparo da solução básica, a massa de óxido de sódio (em gramas) dissolvida foi igual a
Dados: Massa molar (g.mol–1): H = 1 O = 16 Na = 23
Provas
Caderno Container