Foram encontradas 40 questões.
Uma liga de cobre e estanho é denominada:
Provas
Uma bomba integra um conjunto que manobra o escoamento de produtos entre 16 tanques nivelados, dentre os quais 3 podem somente ser esvaziados, 5 podem somente ser enchidos e os demais podem ser esvaziados e/ou enchidos.
O número de possibilidades de manobra entre dois tanques distintos é de:
Provas
A escala do termômetro de um equipamento mede a faixa de 68 a 176°F. Para converter os valores deste termômetro para °C, precisa-se construir uma escala alternativa abrangendo a mesma faixa de medição.
Os valores inicial e final desta escala são, respectivamente, iguais a:
Provas
Para a utilização em determinados cálculos técnicos, a unidade da pressão medida em um manômetro, em psi, precisa ser substituída pela grandeza de força e área.
Sem converter o resultado da medição, a grandeza equivalente a psi é:
Provas
Um tanque cilíndrico com 12m de altura tem capacidade de armazenamento de 200 m3 de óleo. O nível de óleo em uma determinada situação foi medido em 30cm de altura.
Calcula-se que o volume de óleo nesta condição, em litros, seja de:
Provas
Considere as seguintes espécies orgânicas:
![]()
A ordem crescente de acidez dessas espécies é dada por:
Provas
Considere as seguintes substâncias:
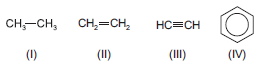
A respeito de suas cadeias carbônicas e de suas propriedades, é correto afirmar que:
Provas
A reação de neutralização entre um ácido fraco H2A e uma base fraca C(OH)3, onde A e C representam, respectivamente, um ânion e um cátion qualquer, é dada por:
3 H2A + 2 C(OH)3 !$ \rightarrow !$ C2A3 + 6 H2O !$ \Delta !$H = – X kcal
O valor da entalpia de neutralização para essa reação, em kcal, é:
Provas
Um laboratorista deseja preparar 500mL de solução 0,1 mol/L de H2SO4. Para isso, ele dispõe de ácido sulfúrico concentrado, cujo teor é de 98% em massa e cuja densidade é 1,84g/cm3.
O volume de ácido sulfúrico concentrado, em mL, a ser gasto nessa preparação é aproximadamente: (Dado: massa molar do H2SO4 = 98g/mol)
Provas
O bafômetro, utilizado para testar o teor de etanol no hálito de motoristas suspeitos de embriaguez, emprega a reação química abaixo.
CH3CH2OH + Na2Cr2O7+ H2SO4 !$ \rightarrow !$ CH3COOH + Cr2(SO4)3 + Na2SO4+ H2O
A respeito dessa reação, é correto afirmar que:
Provas
Caderno Container