Foram encontradas 1.700 questões.
Qual o valor do fluxo de radiação, em kW/m2, emitido
por um corpo a temperatura de 426,85 ºC e cuja emissividade seja igual a 0,8, adotando-se a constante de
Stefan-Boltzmann igual a 5,67 x 10-8 W/(m2.K4)?
Provas
Questão presente nas seguintes provas
O reator abaixo ilustra um Reator CSTR (Reator Tanque Agitado Contínuo). A reação A → B + C ocorre nesse reator.
A carga inicial é alimentada com uma mistura equimolar de A e inerte à temperatura de 400 K e pressão total de 10 atm.
A vazão de entrada é 8 L/s. Os dados coletados no laboratório e processados foram colocados na Tabela abaixo.
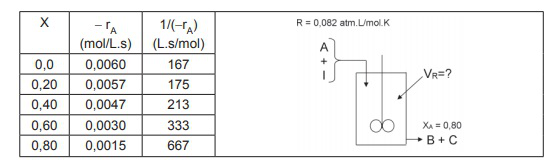
Usando os dados da Tabela e utilizando a Lei dos Gases Ideais, conclui-se que o volume do reator CSTR (em litros) necessário para alcançar uma conversão de 80% é

Usando os dados da Tabela e utilizando a Lei dos Gases Ideais, conclui-se que o volume do reator CSTR (em litros) necessário para alcançar uma conversão de 80% é
Provas
Questão presente nas seguintes provas
Na análise da absorção de um soluto (diluído), absorvido
da fase gasosa para a fase líquida (solvente), estima-se a
altura da torre l (em m) como:
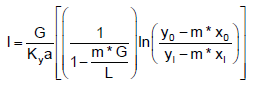
tal que G e L são, respectivamente, as vazões molares de gás e líquido por unidade de área (em kgmol/sm2); m* é a constante de equilíbrio; Ky a é o coeficiente global de transferência de massa vezes a área por volume (em kgmol/sm); y0 e yl são as frações molares do soluto no gás na entrada e na saída da torre, respectivamente, e x0 e xl são as frações molares do soluto no solvente na saída e na entrada da torre, respectivamente.
Para um dado problema, os valores numéricos (no sistema SI) são conhecidos, e os termos da equação acima foram calculados, aproximadamente, como:
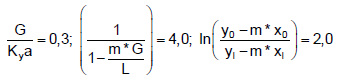
tal que as unidades (quando há) foram omitidas aqui propositadamente.
Usando-se o conceito da literatura de “número de unidades de transferência” (NTU) e “altura de uma unidade de transferência” (HTU), tem-se, nesse caso:
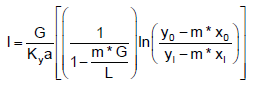
tal que G e L são, respectivamente, as vazões molares de gás e líquido por unidade de área (em kgmol/sm2); m* é a constante de equilíbrio; Ky a é o coeficiente global de transferência de massa vezes a área por volume (em kgmol/sm); y0 e yl são as frações molares do soluto no gás na entrada e na saída da torre, respectivamente, e x0 e xl são as frações molares do soluto no solvente na saída e na entrada da torre, respectivamente.
Para um dado problema, os valores numéricos (no sistema SI) são conhecidos, e os termos da equação acima foram calculados, aproximadamente, como:
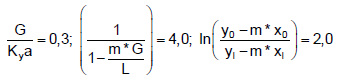
tal que as unidades (quando há) foram omitidas aqui propositadamente.
Usando-se o conceito da literatura de “número de unidades de transferência” (NTU) e “altura de uma unidade de transferência” (HTU), tem-se, nesse caso:
Provas
Questão presente nas seguintes provas
Uma mistura gasosa de hidrocarbonetos é formada por
0,4 mol de CH4, 0,7 mol de C2H6
e 0,9 mol de C3H8
. Essa
mistura se encontra em um reservatório sob pressão total
de 200 kPa.
A pressão parcial de CH4 nessa mistura é igual a
A pressão parcial de CH4 nessa mistura é igual a
Provas
Questão presente nas seguintes provas
Uma indústria de produtos alimentícios possui um reator
do tipo CSTR em um processo de mistura intensa. A
função desse reator é processar a reação de hidrólise do
anidrido acético (1a
ordem em anidrido) com excesso de
água a 25 °C e 1 atm. Essa reação está expressa abaixo:
C4H6O3 + H2 O → 2 CH3COOH
A reação deverá produzir 20 kg/h de ácido acético, a constante de velocidade é aproximadamente 0,05 min-1 , a concentração inicial de anidrido acético é de 100 g/L, e a conversão, de 80%.
O volume aproximado, em litros, desse reator é
Dados Massa Molar do Ácido Acético (CH3COOH) = 60 g/mol Massa Molar do Anidrido Acético (C4H6O3 ) = 102 g/mol
C4H6O3 + H2 O → 2 CH3COOH
A reação deverá produzir 20 kg/h de ácido acético, a constante de velocidade é aproximadamente 0,05 min-1 , a concentração inicial de anidrido acético é de 100 g/L, e a conversão, de 80%.
O volume aproximado, em litros, desse reator é
Dados Massa Molar do Ácido Acético (CH3COOH) = 60 g/mol Massa Molar do Anidrido Acético (C4H6O3 ) = 102 g/mol
Provas
Questão presente nas seguintes provas
Considere que foi desenvolvido um modelo empírico, relacionando-se dados experimentais de vazão volumétrica, q, de um
líquido através de uma válvula e a diferença entre as pressões a montante, P1, e a jusante da mesma, P2, tal que:
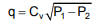
em que a constante Cv foi estimada por regressão não linear.
Considerando-se as três dimensões fundamentais MLt, a dimensão de Cv para consistência dimensional é
em que a constante Cv foi estimada por regressão não linear.
Considerando-se as três dimensões fundamentais MLt, a dimensão de Cv para consistência dimensional é
Provas
Questão presente nas seguintes provas
A formação do trióxido de enxofre (SO3(g)) ocorre a partir
da oxidação do dióxido de enxofre (SO2(g)), reagindo com
oxigênio (O2(g)) a temperatura de 960K e a constante de
equilíbrio nesta temperatura de Kp=10.
A energia de Gibbs nessas condições, em KJmol-1, é
Dado Pressões parciais, em bar, do SO2(g), O2(g), SO3(g), respectivamente, 10-3, 0,20, 10-4. Constante dos gases, R = 8,314 J.-1 .mol-1; Logaritmo Neperiano, ln(5)=1,609; ln(10)=2,303.
A energia de Gibbs nessas condições, em KJmol-1, é
Dado Pressões parciais, em bar, do SO2(g), O2(g), SO3(g), respectivamente, 10-3, 0,20, 10-4. Constante dos gases, R = 8,314 J.-1 .mol-1; Logaritmo Neperiano, ln(5)=1,609; ln(10)=2,303.
Provas
Questão presente nas seguintes provas
Um sistema formado por CO2
saturado com vapor d’água
apresenta pressão total de 100 kPa a 363 K. Nessa temperatura, a pressão de vapor da água é 70 kPa.
A fração molar do CO2 na mistura é igual a
A fração molar do CO2 na mistura é igual a
Provas
Questão presente nas seguintes provas
A reação elementar A → B ocorre em um reator tubular
(PFR – reator com escoamento uniforme), representado pela Figura abaixo, com uma vazão volumétrica de
entrada de 6 L/min. A velocidade específica de reação
é 0,25 min-1.

O volume do reator necessário para reduzir a concentração de saída a 20% da concentração de entrada é, aproximadamente,
Dado In 0,2 = -1,609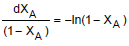

O volume do reator necessário para reduzir a concentração de saída a 20% da concentração de entrada é, aproximadamente,
Dado In 0,2 = -1,609
Provas
Questão presente nas seguintes provas
A Equação de Arrhenius, k = k0
exp(-E/RT), pode ser escrita na forma logarítmica gerando a expressão ln k = ln k0
– E/RT. Os
dados apresentados na Tabela a seguir referem-se à reação 2A → 2B + C.
T (°C) T (K) K (L mol-1 s-1) ln k 161,63 434,78 148,42 5,00 104,20 377,35 1 0 60,18 333,33 0,0067 -5,0
A partir desses dados plotados na Figura abaixo, calcula-se a Energia de Ativação desta reação.
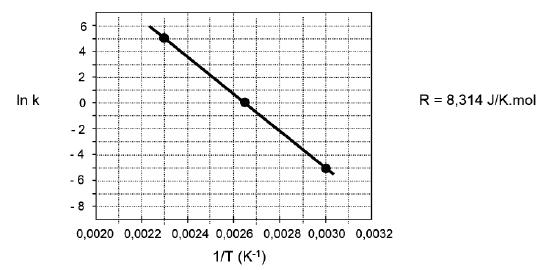
O valor da Energia de Ativação expresso em Joules/mol é
T (°C) T (K) K (L mol-1 s-1) ln k 161,63 434,78 148,42 5,00 104,20 377,35 1 0 60,18 333,33 0,0067 -5,0
A partir desses dados plotados na Figura abaixo, calcula-se a Energia de Ativação desta reação.

O valor da Energia de Ativação expresso em Joules/mol é
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container