Foram encontradas 540 questões.
Um determinado processo acarreta a liberação de dióxido
de enxofre para a atmosfera. Na atmosfera, esse composto reage com o gás oxigênio e com o vapor d’água
formando um ácido inorgânico forte.
A fórmula molecular desse ácido é
A fórmula molecular desse ácido é
Provas
Questão presente nas seguintes provas
A análise dos componentes presentes em um depósito
salino indicou a presença de nitrato de bário.
A fórmula química desse sal é
A fórmula química desse sal é
Provas
Questão presente nas seguintes provas
A protonação de uma amina biogênica requer absorção de calor, atingindo uma situação de equilíbrio no meio aquoso,
como descrito na reação abaixo.
H2 N-CH2 -CH2 -CH2 -CH2 -NH2(aq) + 2 H+ (aq) ⇌ +H3 N-CH2 -CH2 -CH2 -CH2 -NH3 + (aq)
Nesse sistema, verifica-se que o(a)
H2 N-CH2 -CH2 -CH2 -CH2 -NH2(aq) + 2 H+ (aq) ⇌ +H3 N-CH2 -CH2 -CH2 -CH2 -NH3 + (aq)
Nesse sistema, verifica-se que o(a)
Provas
Questão presente nas seguintes provas
Considere o sistema de equações a seguir, que envolvem reações de hidrocarbonetos.
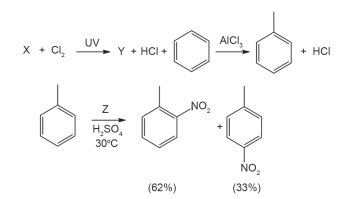
As substâncias X, Y e Z são, respectivamente
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
À luz da teoria de ácidos e bases de Brönsted-Lowry, conclui-se que um(a)
Provas
Questão presente nas seguintes provas
A distribuição eletrônica e a posição na tabela periódica,
do elemento químico com número atômico 12, em seu estado fundamental, são, respectivamente,
Provas
Questão presente nas seguintes provas
Considere as duas semirreações abaixo:
Zn2+ (aq) + 2e → Zn(s) ; Eº = -0,76 V
AgBr(s) + e → Ag(s) + Br- (aq) ; Eº = +0,07 V
Com base nos seus potenciais padrões de redução, a reação global de oxirredução é
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- FundamentosSubstâncias, Misturas e Processos de Separação
- Química InorgânicaSoluções e Substâncias Inorgânicas
- Química Orgânica
- Transformações Químicas e EnergiaTermoquímica
Um técnico recebeu um frasco contendo um cloreto de
elemento alcalinoterroso (X) de aspecto cristalino e de coloração branca. Ele selecionou uma massa da amostra
para solubilizar completamente em água e, em seguida,
reagir com excesso de carbonato de potássio. O carbonato de X precipitado foi separado, seco e armazenado em
um dessecador.
Uma massa de 1,00 g desse carbonato foi aquecida, produzindo aproximadamente 0,223 g do gás CO2
, conforme
a reação a seguir.
XCO3(s) → XO(s) + CO2(g)
Considerando-se a pureza do carbonato e a sua decomposição assumidamente completa, o elemento X em questão é o
XCO3(s) → XO(s) + CO2(g)
Considerando-se a pureza do carbonato e a sua decomposição assumidamente completa, o elemento X em questão é o
Provas
Questão presente nas seguintes provas
Uma solução aquosa de hidróxido de sódio tem densidade igual a 1,40 g mL-1
e 40% de teor do soluto, em massa.
A concentração, em mol L-1 , do hidróxido na solução é
Dado M(NaOH) = 40 g mol-1
A concentração, em mol L-1 , do hidróxido na solução é
Dado M(NaOH) = 40 g mol-1
Provas
Questão presente nas seguintes provas
A decomposição do carbonato de cálcio produz CO2
,
como representado na reação termoquímica abaixo.
CaCO3(s) → CaO(s) + CO2(g); ΔH0 = +179 kJ
Considerando-se o comportamento ideal do gás e o rendimento máximo da reação, a energia necessária, em MJ, para produzir 36 m3 de CO2 , medido nas condições normais de temperatura e pressão (CNTP) é, aproximadamente,
Dado R × T = 24,4 atm L mol-1 M = 106
CaCO3(s) → CaO(s) + CO2(g); ΔH0 = +179 kJ
Considerando-se o comportamento ideal do gás e o rendimento máximo da reação, a energia necessária, em MJ, para produzir 36 m3 de CO2 , medido nas condições normais de temperatura e pressão (CNTP) é, aproximadamente,
Dado R × T = 24,4 atm L mol-1 M = 106
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container