Foram encontradas 540 questões.
A dimetilglioxima é um reagente específico na análise gravimétrica.
Esse reagente é empregado para a determinação do cátion
Provas
Questão presente nas seguintes provas
Iodeto de hidrogênio é produzido a partir da reação química representada pelo equilíbrio a seguir:
H2 (g) + I2 (g) ⇌ 2 HI (g)
Em um reator, as concentrações iniciais de H2 e I2 foram respectivamente iguais a 3,0 mol L-1 e a 3,5 mol L-1 . Atingido o equilíbrio, a concentração de HI foi de 5 mol L-1 . Nas condições do reator, a constante de equilíbrio da reação em termos de concentrações é igual a
H2 (g) + I2 (g) ⇌ 2 HI (g)
Em um reator, as concentrações iniciais de H2 e I2 foram respectivamente iguais a 3,0 mol L-1 e a 3,5 mol L-1 . Atingido o equilíbrio, a concentração de HI foi de 5 mol L-1 . Nas condições do reator, a constante de equilíbrio da reação em termos de concentrações é igual a
Provas
Questão presente nas seguintes provas
Um recipiente de 4,0 L é completamente preenchido por
gás etano a 27ºC.
Sabendo-se que a pressão no recipiente é de 1,2 atm e que o gás apresenta comportamento ideal, a massa de etano, em gramas, presente no interior do recipiente é igual a
Dado
constante dos gases ideais: 0,08 atm L mol-1 K-1
massas molares: C = 12 g mol-1, H = 1 g mol-1
Sabendo-se que a pressão no recipiente é de 1,2 atm e que o gás apresenta comportamento ideal, a massa de etano, em gramas, presente no interior do recipiente é igual a
Dado
constante dos gases ideais: 0,08 atm L mol-1 K-1
massas molares: C = 12 g mol-1, H = 1 g mol-1
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Em um experimento, misturou-se 1.200 mL de uma solução aquosa de KF na concentração de 0,50 mol L-1
com
800 mL de uma solução aquosa de K2
SO4
de concentração 0,20 mol L-1
.
Admitindo-se que há completa dissociação dos solutos, a concentração de íons K+ , em mol L-1 , na solução formada é igual a
Admitindo-se que há completa dissociação dos solutos, a concentração de íons K+ , em mol L-1 , na solução formada é igual a
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
Dentre os elementos químicos presentes no sexto período da tabela de classificação periódica, aquele que apresenta o menor raio atômico tem como símbolo
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Deseja-se preparar 500 mL de uma solução aquosa de
CaBr2
com concentração de 0,05 mol L-1
.
A massa, em gramas, de soluto a ser empregada no preparo dessa solução corresponde a
Dado massas molares: Ca = 40 g mol-1 Br = 80 g mol-1
A massa, em gramas, de soluto a ser empregada no preparo dessa solução corresponde a
Dado massas molares: Ca = 40 g mol-1 Br = 80 g mol-1
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
- Técnicas de LaboratórioEquipamentos e Técnicas Básicas
O cálculo do Limite de Detecção (LOD) e do Limite de Quantificação (LOQ) é comumente usado como parâmetro de validação para descrever os limites de sensibilidade de uma curva de calibração. As fórmulas para calcular o LOD e o LOQ
são as seguintes:
LOD = 3 x (desvio padrão do branco / inclinação da curva de calibração) LOQ = 10 x (desvio padrão do branco / inclinação da curva de calibração)
Considere que um procedimento de validação foi feito para determinar o LOD e o LOQ de um certo método analítico em espectroscopia de absorção atômica. Foram feitas dez medições do branco que, por sua vez, produziram valor médio = 4,24 x 10-3 com desvio padrão = 3,42 x 10-4 . A equação da reta da curva de calibração do método, com os seus respectivos coeficientes angular e linear, foi:
Absorbância = 3,42 x 10-3 conc. (mg L-1 ) + 2,23 x 10-3
O coeficiente de determinação (R2 ) da curva de calibração foi 0,9994. Com base nesses dados, os valores de LOD e de LOQ, em mg L-1 , foram, respectivamente,
LOD = 3 x (desvio padrão do branco / inclinação da curva de calibração) LOQ = 10 x (desvio padrão do branco / inclinação da curva de calibração)
Considere que um procedimento de validação foi feito para determinar o LOD e o LOQ de um certo método analítico em espectroscopia de absorção atômica. Foram feitas dez medições do branco que, por sua vez, produziram valor médio = 4,24 x 10-3 com desvio padrão = 3,42 x 10-4 . A equação da reta da curva de calibração do método, com os seus respectivos coeficientes angular e linear, foi:
Absorbância = 3,42 x 10-3 conc. (mg L-1 ) + 2,23 x 10-3
O coeficiente de determinação (R2 ) da curva de calibração foi 0,9994. Com base nesses dados, os valores de LOD e de LOQ, em mg L-1 , foram, respectivamente,
Provas
Questão presente nas seguintes provas
Três termômetros são colocados em série ao longo de
uma tubulação de água para monitorar a variação de
temperatura. O primeiro marca 230°C, o segundo, 446°F,
e o terceiro, 562,15 K.
Com base nas informações apresentadas, verifica-se que, à medida que a água percorre o duto, sua temperatura
Com base nas informações apresentadas, verifica-se que, à medida que a água percorre o duto, sua temperatura
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um volume de 50,00 mL de solução de amostra contendo Fe2+
foi adicionado a um frasco Erlenmeyer, seguido da adição
de 50,00 mL de água. Foram necessários 30,00 mL de solução padrão de dicromato de potássio (0,05 mol L-1
) para reagir
totalmente e de forma estequiométrica com o Fe2+
.
6 Fe2+ (aq) + Cr2 O7 2+ (aq) + 14 H+ → 6 Fe3+ (aq) + 2 Cr3+ (aq) + 7 H2 O(l)
Com base nessas informações, a quantidade, em mol, de Fe2+ na solução de amostra é
6 Fe2+ (aq) + Cr2 O7 2+ (aq) + 14 H+ → 6 Fe3+ (aq) + 2 Cr3+ (aq) + 7 H2 O(l)
Com base nessas informações, a quantidade, em mol, de Fe2+ na solução de amostra é
Provas
Questão presente nas seguintes provas
O poliestireno é um polímero com excelentes propriedades mecânicas e isolantes, aplicado em diversos setores,
incluindo a fabricação de produtos descartáveis. Esse polímero tem unidade de repetição estireno, representada a
seguir:
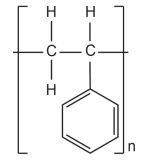
Com base na estrutura do monômero, a reação de polimerização para a formação do poliestireno é a

Com base na estrutura do monômero, a reação de polimerização para a formação do poliestireno é a
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container