Foram encontradas 85 questões.
Julgue o item a seguir.

O etileno, C2H4(g), produzido a partir da desidratação do etanol, é um hidrocarboneto saturado utilizado como matéria-prima para a produção de polímeros usados na fabricação de embalagens biodegradáveis.
Provas
Julgue o item a seguir.

A decomposição da água por eletrólise, representada na figura, resulta na produção de um volume de hidrogênio, H2(g), no tubo II, duas vezes superior ao volume de oxigênio, O2(g), no tubo I.
Provas
Julgue o item a seguir.
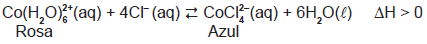
Aplicando-se o princípio de Le Chatêlier ao equilíbrio químico representado pela equação química, pode-se afirmar que o aquecimento da solução em equilíbrio favorece a intensificação da coloração azul devido ao deslocamento do equilíbrio químico, com formação de íons CoCl2– 4 (aq), e ao aumento do valor da constante de equilíbrio, Kc.
Provas
Julgue o item a segujr.
2ClO2(aq) + 2OH–(aq) → ClO–3 (aq) + ClO–2 (aq) + H2O(!$ \ell !$)
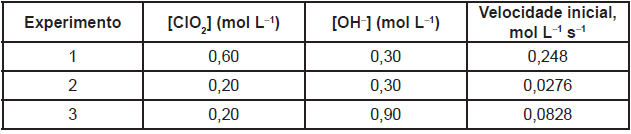
A equação de velocidade de uma reação representa a lei de velocidade e relaciona as concentrações dos reagentes elevadas a expoentes determinados experimentalmente.
Analisando-se a equação química e os dados experimentais que constam na tabela, é correto afimar que a velocidade da reação representada é dada pela equação v = k [ClO2]2. [OH–].
Provas
Julgue o item a seguir.
2NaI(s) + MnO2(s) + 3H2SO4(aq)  2NaHSO4(aq) + MnSO4(aq) + 2H2O(!$ \ell !$) + I2(g)
2NaHSO4(aq) + MnSO4(aq) + 2H2O(!$ \ell !$) + I2(g)
O iodo gasoso, I2(g), pode ser obtido em laboratório pelo aquecimento da mistura de iodeto de sódio, NaI(s), e dióxido de manganês, MnO2(s), com gotejamento contínuo de ácido sulfúrico concentrado, H2SO4(aq), de acordo com a reação representada, de maneira simplificada, pela equação química.
A equação de oxirredução representada revela que o iodeto de sódio atua como agente oxidante porque cada átomo de iodo do iodeto de sódio transfere um elétron para o átomo de manganês do dióxido de manganês.
Provas
Julgue o item a seguir.
2NaI(s) + MnO2(s) + 3H2SO4(aq)  2NaHSO4(aq) + MnSO4(aq) + 2H2O(!$ \ell !$) + I2(g)
2NaHSO4(aq) + MnSO4(aq) + 2H2O(!$ \ell !$) + I2(g)
O iodo gasoso, I2(g), pode ser obtido em laboratório pelo aquecimento da mistura de iodeto de sódio, NaI(s), e dióxido de manganês, MnO2(s), com gotejamento contínuo de ácido sulfúrico concentrado, H2SO4(aq), de acordo com a reação representada, de maneira simplificada, pela equação química.
Considerando-se as informações apresentadas, é correto afirmar que a massa de dióxido de manganês, que reage totalmente com 60,0g de iodeto de sódio, na presença de ácido sulfúrico suficiente, é de 17,4g.
Provas
Julgue o item a seguir.
Em um experimento realizado para a determinação da densidade de um gás a 27ºC e 1,0atm, foi utilizado um recipiente fechado, inicialmente vazio, e com capacidade para 2,0L e massa de 836,2g, que, depois da introdução da amostra de gás, pesou 839,0g.
Considerando-se essas informações, pode-se concluir que a densidade e a massa molar do gás são, respectivamente, 1,4g L–1 e 34,4g mol–1.
Provas
Julgue o item a seguir.
A adição de água a uma solução de álcool e gasolina forma um sistema monofásico devido às fracas interações intermoleculares que serão formadas entre a água e as substâncias químicas que constituem a mistura álcool e gasolina.
Provas
Julgue o item a seguir.
Considerando a estrutura e os elementos químicos que constituem a molécula do trióxido de enxofre, SO3, é correto afirmar que esse óxido tem caráter ácido e é formado por moléculas apolares.
Provas
Julgue o item a seguir.
A posição do zinco e do cádmio na Tabela Periódica permite afirmar que, apesar desses elementos químicos pertencerem a um mesmo grupo periódico, o raio atômico do zinco é maior do que o raio atômico do cádmio.
Provas
Caderno Container