Foram encontradas 273 questões.
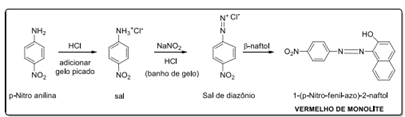
Uma das rotas sintéticas para a produção do corante vermelho de monolite está descrita abaixo:
Provas
Questão presente nas seguintes provas
A corrosão é um processo natural e
espontâneo, cujo funcionamento é análogo ao das
pilhas que utilizamos no nosso dia a dia. Nas ligas
metálicas, principais componentes das estruturas
dos navios, essa mudança pode ser identificada
como oxidação, o que deixa o metal desgastado e
poroso. Em cidades litorâneas a maresia agrava
em até 40 vezes o processo de corrosão, pois o ar
é carregado de partículas de água e íons
salinos, o que forma uma ponte salina,
contribuindo para que ocorram as reações
eletroquímicas. Esse cenário faz aumentar o
processo corrosivo para a indústria naval.
Por isso, há diversos métodos que podem ser utilizados para a prevenção das corrosões. O principal método, é o revestimento com tintas especiais; estas dão aos cascos dos navios uma proteção extra, pois isolam a estrutura metálica do meio corrosivo. Tintas com ânodo de sacrifício utilizam o princípio da proteção catódica, que se corrói no lugar do metal da estrutura, protegendo-o da corrosão.
Disponível em: https://peqengenhariajr.com.br/corrosao-na-industria nava. Acesso em: 17 jun. 2025.
Das tintas de ânodos de sacrifício, o ânodo de sacrifício mais utilizado é com magnésio, pois apesar de sua eficiência ser baixa (aproximadamente 50%), ele tem um potencial bastante negativo que permite elevados valores de correntes.
O valor da diferença de potencial formada entre o casco do navio, material de aço cuja liga é constituída essencialmente por zinco, revestido por uma tinta à base de magnésio é
Dados:
Zn2+ + 2e- → Zn(s) E0 redução = - 0,76 V
Mg2+ + 2e- → Mg(s) E0 redução = - 2,37 V
Por isso, há diversos métodos que podem ser utilizados para a prevenção das corrosões. O principal método, é o revestimento com tintas especiais; estas dão aos cascos dos navios uma proteção extra, pois isolam a estrutura metálica do meio corrosivo. Tintas com ânodo de sacrifício utilizam o princípio da proteção catódica, que se corrói no lugar do metal da estrutura, protegendo-o da corrosão.
Disponível em: https://peqengenhariajr.com.br/corrosao-na-industria nava. Acesso em: 17 jun. 2025.
Das tintas de ânodos de sacrifício, o ânodo de sacrifício mais utilizado é com magnésio, pois apesar de sua eficiência ser baixa (aproximadamente 50%), ele tem um potencial bastante negativo que permite elevados valores de correntes.
O valor da diferença de potencial formada entre o casco do navio, material de aço cuja liga é constituída essencialmente por zinco, revestido por uma tinta à base de magnésio é
Dados:
Zn2+ + 2e- → Zn(s) E0 redução = - 0,76 V
Mg2+ + 2e- → Mg(s) E0 redução = - 2,37 V
Provas
Questão presente nas seguintes provas
Atualmente a Talidomida é um medicamento
seguro, mas em função dos efeitos teratogênicos
(malformação congênita), historicamente comprovados, possui controle sanitário rigoroso, sob
responsabilidade entre os gestores em saúde dos três
entes federativos, profissionais de saúde e pacientes.
É produzida somente por laboratório público, conforme
programação do Ministério da Saúde, o qual realiza a
distribuição para os estados e Distrito Federal. O
atendimento das pessoas que necessitam utilizar a
talidomida ocorre no âmbito do SUS, em unidades
públicas da atenção primária, de média ou alta
complexidade.
No Brasil a talidomida está indicada somente para tratamento das doenças previstas nos protocolos clínicos e diretrizes terapêuticas do Ministério da Saúde, as quais são: o eritema nodoso hansênico, lúpus eritematoso, úlceras aftoides em pacientes portadores de HIV-Aids, doença do enxerto contra hospedeiro, mieloma múltiplo e síndrome mielodisplásica. É proibido o uso da talidomida por gestantes.
(Informações obtidas do site do Ministério da Saúde, Governo Federal) https://www.gov.br/saude Lei nº 10.651, de 16/04/2003 - Dispõe sobre o controle do uso da talidomida RDC ANVISA n° 11, de 22/03/2011 – Dispõe sobre o controle da substância Talidomida
A seguir, as duas formas da talidomida, R e S:
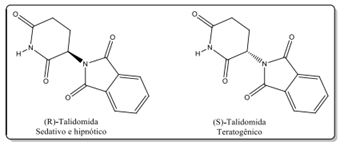
Sobre esse composto é correto afirmar que
No Brasil a talidomida está indicada somente para tratamento das doenças previstas nos protocolos clínicos e diretrizes terapêuticas do Ministério da Saúde, as quais são: o eritema nodoso hansênico, lúpus eritematoso, úlceras aftoides em pacientes portadores de HIV-Aids, doença do enxerto contra hospedeiro, mieloma múltiplo e síndrome mielodisplásica. É proibido o uso da talidomida por gestantes.
(Informações obtidas do site do Ministério da Saúde, Governo Federal) https://www.gov.br/saude Lei nº 10.651, de 16/04/2003 - Dispõe sobre o controle do uso da talidomida RDC ANVISA n° 11, de 22/03/2011 – Dispõe sobre o controle da substância Talidomida
A seguir, as duas formas da talidomida, R e S:

Sobre esse composto é correto afirmar que
Provas
Questão presente nas seguintes provas
O butanoato de etila é um éster etílico volátil,
de odor frutado, encontrado em bebidas alcoólicas
e produzido durante a fermentação por leveduras.
As concentrações de éster etílico diminuem com o
tempo, à medida que a bebida alcoólica
envelhece, devido à hidrólise espontânea.
É um éster responsável por aromas que lembram maçã, abacaxi e queijo gorgonzola, formados pela reação de esterificação, entre o etanol e o ácido butanoico.
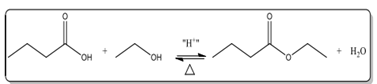
A substância que corresponde a um metâmero do produto da reação de esterificação descrita acima é:
É um éster responsável por aromas que lembram maçã, abacaxi e queijo gorgonzola, formados pela reação de esterificação, entre o etanol e o ácido butanoico.

A substância que corresponde a um metâmero do produto da reação de esterificação descrita acima é:
Provas
Questão presente nas seguintes provas
No Brasil, o café é uma das paixões
nacionais. Os brasileiros consomem, em média,
duas doses diárias, mesmo nos dias mais
quentes. Em alguns períodos da década de 1980,
o café era a segunda mercadoria mais negociada
no mundo por valor monetário, atrás apenas
do petróleo. (Portillo, L. El Convenio Internacional del Café y la
crisis del mercado. Comercio Exterior 43: 378-391, 1993)
O café é originário das terras altas da Etiópia, de um local chamado Kaffa. No entanto, a palavra "café" é originária do árabe qahwa, que significa "vinho". Por essa razão o café ficou conhecido como "vinho da Arábia" quando chegou à Europa no Século XIV. (A História do Café: web.archive.org)
É um estimulante, por possuir cafeína (cerca de 80 a 140 mg para cada 207 mL), dependendo do método de preparação. Na figura a seguir, é dada a fórmula estrutural da cafeína:
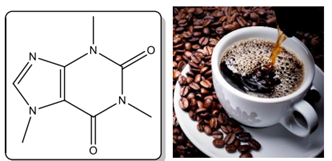
Sobre a cafeína é correto afirmar que
O café é originário das terras altas da Etiópia, de um local chamado Kaffa. No entanto, a palavra "café" é originária do árabe qahwa, que significa "vinho". Por essa razão o café ficou conhecido como "vinho da Arábia" quando chegou à Europa no Século XIV. (A História do Café: web.archive.org)
É um estimulante, por possuir cafeína (cerca de 80 a 140 mg para cada 207 mL), dependendo do método de preparação. Na figura a seguir, é dada a fórmula estrutural da cafeína:

Sobre a cafeína é correto afirmar que
Provas
Questão presente nas seguintes provas
A hidroxiapatita é o principal constituinte
mineral dos ossos e dos dentes humanos, sendo
sua fórmula molecular Ca10(PO4)6(OH)2. Além de
apresentar grande importância na saúde dentária
e óssea, a hidroxiapatita tem sido estudada por
diversos grupos de pesquisa das engenharias, na
produção de biocerâmicas, na indústria de
alimentos, e em procedimentos estéticos.
Os fosfatos de cálcio são materiais cerâmicos que apresentam propriedades particulares como biocompatibilidade e similaridade química com os tecidos ósseos e dentários dos seres vivos. Sua morfologia porosa permite que estes se apresentem como material apropriado para a utilização em substituição de pequenas partes de tecido ósseo, já que proporciona o crescimento de canais de sistemas nervosos, suporte para vasos sanguíneos como também suporte para deposição de fármacos.
(M. V. B. dos Santos, J. A. Osajima, E. C. da Silva Filho, Hidroxiapatita: suporte para liberação de fármacos e propriedades antimicrobianas, Cerâmica, 62, 256-265, 2016) http://dx.doi.org/10.1590/0366-69132016623631980
Dada a fórmula molecular do fosfato de cálcio, Ca3(PO4)2, o número de oxidação do cálcio, do fósforo e do oxigênio, são, respectivamente
Os fosfatos de cálcio são materiais cerâmicos que apresentam propriedades particulares como biocompatibilidade e similaridade química com os tecidos ósseos e dentários dos seres vivos. Sua morfologia porosa permite que estes se apresentem como material apropriado para a utilização em substituição de pequenas partes de tecido ósseo, já que proporciona o crescimento de canais de sistemas nervosos, suporte para vasos sanguíneos como também suporte para deposição de fármacos.
(M. V. B. dos Santos, J. A. Osajima, E. C. da Silva Filho, Hidroxiapatita: suporte para liberação de fármacos e propriedades antimicrobianas, Cerâmica, 62, 256-265, 2016) http://dx.doi.org/10.1590/0366-69132016623631980
Dada a fórmula molecular do fosfato de cálcio, Ca3(PO4)2, o número de oxidação do cálcio, do fósforo e do oxigênio, são, respectivamente
Provas
Questão presente nas seguintes provas
A laranja é uma fruta cítrica, excelente fonte
de vitamina C e outros nutrientes vitais. A vitamina
C é um ótimo antioxidante natural, pois age no
fortalecimento do sistema imunológico, ajudando
o corpo a combater infecções, doenças e
impulsionar as defesas imunológicas.
O Brasil é o maior produtor global de suco de laranja, representando 62% do volume mundial. A produção concentra-se entre São Paulo e Minas Gerais. Em 2022/23, a safra de suco de laranja no Brasil atingiu 586.313 toneladas, com um aumento de 17% nas exportações.
Para garantir a qualidade e a durabilidade do produto, as indústrias alimentícias precisam ter o controle do pH, que resulta em melhores características e benefícios à saúde humana. Na prática, um pH muito baixo pode favorecer à proliferação de bactérias e leveduras que deterioram o produto; e pH acima de 7,0 a 7,5 pode favorecer a atividade da enzima pectina metil esterase que também resulta na degradação do produto. De modo geral, a literatura indica que o suco de laranja tenha um pH ácido, entre 3 e 4.
O laboratório de controle de qualidade de uma indústria alimentícia coletou cinco amostras de sucos de laranja, processadas em dias diferentes, e analisou a concentração de íons H3O+ de cada uma:
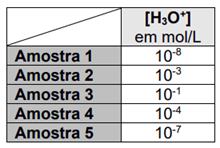
Sobre as amostras coletadas pelo controle de qualidade, é correto afirmar que
O Brasil é o maior produtor global de suco de laranja, representando 62% do volume mundial. A produção concentra-se entre São Paulo e Minas Gerais. Em 2022/23, a safra de suco de laranja no Brasil atingiu 586.313 toneladas, com um aumento de 17% nas exportações.
Para garantir a qualidade e a durabilidade do produto, as indústrias alimentícias precisam ter o controle do pH, que resulta em melhores características e benefícios à saúde humana. Na prática, um pH muito baixo pode favorecer à proliferação de bactérias e leveduras que deterioram o produto; e pH acima de 7,0 a 7,5 pode favorecer a atividade da enzima pectina metil esterase que também resulta na degradação do produto. De modo geral, a literatura indica que o suco de laranja tenha um pH ácido, entre 3 e 4.
O laboratório de controle de qualidade de uma indústria alimentícia coletou cinco amostras de sucos de laranja, processadas em dias diferentes, e analisou a concentração de íons H3O+ de cada uma:

Sobre as amostras coletadas pelo controle de qualidade, é correto afirmar que
Provas
Questão presente nas seguintes provas
O cloreto de sódio é um composto iônico muito
utilizado no cotidiano, pois o sal é essencial para a vida
animal, além de ser um importante conservante de
alimentos. Essa é uma técnica bastante antiga, usada
há séculos para prolongar a vida útil dos alimentos, e
fundamental na história da alimentação, pois garantiu
a preservação dos nutrientes, armazenamento e
conservação a longo prazo.
Há diferentes métodos para sintetizar o cloreto de sódio; um deles se dá a partir do sódio metálico e do gás cloro.
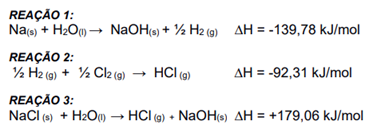
(CASTELLAN, G. Fundamentos de Físico-Química. 9ª Ed., Rio de Janeiro: LTC, página 141, 2011).
O valor do ∆H da reação global da formação do cloreto de sódio é
Considere as seguintes equações termoquímicas:
Há diferentes métodos para sintetizar o cloreto de sódio; um deles se dá a partir do sódio metálico e do gás cloro.
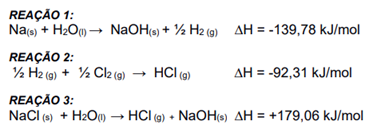
(CASTELLAN, G. Fundamentos de Físico-Química. 9ª Ed., Rio de Janeiro: LTC, página 141, 2011).
O valor do ∆H da reação global da formação do cloreto de sódio é
Considere as seguintes equações termoquímicas:
Provas
Questão presente nas seguintes provas
Recentemente, escavações arqueológicas
no Nordeste dos Estados Unidos descobriram
uma pilha eletroquímica feita com eletrodos de
cobre e ferro; a invenção foi datada entre os anos
300 a.C e 300 d.C. Existe alguma evidência de
que já no ano 2500 a.C. os egípcios sabiam como
galvanizar os objetos.
(CASTELLAN, G. Fundamentos de Físico-Química. 9ª Ed., Rio de Janeiro: LTC, páginas 410 - 427, 2011).
A galvanização é um processo em que se reveste peças de ferro ou de aço com zinco metálico. Essa camada de zinco atua como uma barreira física e, em alguns casos, como um metal de sacrifício. Esse processo protege contra a corrosão e a ferrugem, prolongando a vida útil do material.
Analise as semirreações a seguir:

A opção que representa o que ocorre no anodo e no catodo, respectivamente, desse processo é:
(CASTELLAN, G. Fundamentos de Físico-Química. 9ª Ed., Rio de Janeiro: LTC, páginas 410 - 427, 2011).
A galvanização é um processo em que se reveste peças de ferro ou de aço com zinco metálico. Essa camada de zinco atua como uma barreira física e, em alguns casos, como um metal de sacrifício. Esse processo protege contra a corrosão e a ferrugem, prolongando a vida útil do material.
Analise as semirreações a seguir:

A opção que representa o que ocorre no anodo e no catodo, respectivamente, desse processo é:
Provas
Questão presente nas seguintes provas
O gás acetileno ou etino, pela nomenclatura
PIN (Preferred IUPAC Name), é um
hidrocarboneto inflamável amplamente utilizado
em processos industriais, tais como: solda, corte
de metais, produção de uma série de produtos
químicos etc. Uma das formas de sintetizá-lo é
pela equação química abaixo:
CaC2 (s) + 2 H2O (l) → C2H2 (g) + Ca(OH)2 (s)
Com relação à polaridade do acetileno e sua geometria molecular, é correto afirmar que a molécula é
CaC2 (s) + 2 H2O (l) → C2H2 (g) + Ca(OH)2 (s)
Com relação à polaridade do acetileno e sua geometria molecular, é correto afirmar que a molécula é
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container