Foram encontradas 50 questões.
O processo de fotossíntese, efetuado pelos vegetais clorofilados, permite que, na presença de luz, estessintetizem seu próprio alimento, a glicose (C6H12O6), empregando água e gás carbônico como reagentes,além de liberarem gás oxigênio para a atmosfera, de acordo com a equação abaixo:
luz e clorofila 6 H2O (I) + 6 CO2 (g) → C6H12O6 (aq) + O2 (g)
Sobre essa reação química, é correto afirmar:
luz e clorofila 6 H2O (I) + 6 CO2 (g) → C6H12O6 (aq) + O2 (g)
Sobre essa reação química, é correto afirmar:
Provas
Questão presente nas seguintes provas
Reações envolvendo anéis aromáticos são importantes para a indústria de bens de consumo, como a
indústria farmacêutica. Considere a molécula abaixo, contendo um anel aromático com substituinte acila.
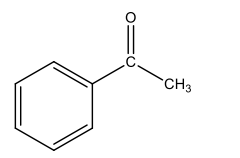
Assinale a alternativa que apresenta o reagente para a síntese dessa molécula

Assinale a alternativa que apresenta o reagente para a síntese dessa molécula
Provas
Questão presente nas seguintes provas
- Química OrgânicaReações OrgânicasReações Orgânicas: Substituição, Adição e Eliminação
- Química OrgânicaTipos de Reagentes e Mecanismos das Reações Orgânicas
O potente explosivo conhecido como TNT (trinitrotolueno) é útil na exploração de jazidas minerais, como
bauxita, carvão mineral, calcário, entre outras.
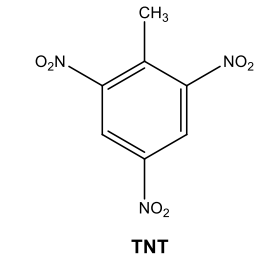
A obtenção desse explosivo, cuja molécula é visualizada acima, é possível devido

A obtenção desse explosivo, cuja molécula é visualizada acima, é possível devido
Provas
Questão presente nas seguintes provas
Na comunicação informal, qual é o tipo de rede de boatos que se caracteriza por ser um pouco interessante,
mas insignificante, em que os indivíduos contam aleatoriamente, indiferentes com relação à pessoa a quem
dão a informação?
Provas
Questão presente nas seguintes provas
- OrtografiaPontuaçãoDois-pontos
- OrtografiaPontuaçãoPonto de Exclamação e Interrogação
- OrtografiaPontuaçãoVírgula
- Sintaxe
Leia o texto abaixo de Walcyr Carrasco, Revista Veja Ed. 2668, e responda à questão.
Início de ano é sempre assim: a gente faz promessas, ambiciona novidades. Como o ano só começa
realmente depois do Carnaval, costumo aguardar até lá. Mas aí já é tarde: o ano ganhou seu ritmo e eu deixo
as mudanças para o futuro. Em 2019 pensei no que realmente desejaria para este 2020. Há uma palavra que
não me sai da cabeça: segurança. É claro que o país tem problemas de todo tipo. Mas a segurança toca no
meu cotidiano diretamente. [...] Eu me admiro ver as pessoas convivendo com a violência como se fosse
absolutamente normal. Uma amiga sai sempre com dois celulares. Um velho e um bom, escondido. O mais
antigo é para, no caso de assalto, entregar ao ladrão. Já ouvi um conhecido dizer que o “meliante” foi legal,
pois o deixou ficar com os documentos. Ou seja: o sujeito assalta, ameaça, mas é “legal”? Recentemente, um
amigo fez aniversário. Tínhamos um evento, mas queríamos nos reunir depois das dez da noite. Foi difícil
achar um restaurante: a maioria está fechando mais cedo. Em São Paulo, no centro, as mulheres andam
agarradas às bolsas. O pior, porém, repito, é nossa atitude passiva. Nós nos acostumamos ao absurdo. [...].
Há alguns anos, eu saía do Leblon e andava até o Arpoador pela praia. É uma boa e saudável
distância. Não tenho mais coragem. Quero voltar a andar pelo calçadão sem medo. Se caminhar, realizarei
meu segundo desejo de Ano Novo: perder a barriga. Mas quando? A falta de segurança mudou a minha vida.
Sem dúvida, continuarei barrigudo.
Provas
Questão presente nas seguintes provas
- Modelo OSIIntrodução ao Modelo OSI
- Modelo OSIModelo OSI: Camada Física
- Modelo OSIModelo OSI: Camada de Enlace
- Modelo OSIModelo OSI: Camada de Aplicação
Para prover uma estrutura para o projeto de protocolos de rede, projetistas de redes organizam protocolos em
camadas. A pilha de protocolo é formada por camadas, na seguinte ordem:
Provas
Questão presente nas seguintes provas
- Interações com Tecnologia, Sociedade e Meio Ambiente
- Técnicas de LaboratórioEquipamentos e Técnicas Básicas
A gasolina Tipo C (comum), comercializada nos postos de combustíveis, deve conter, de acordo com as
normas da ANP, um teor padronizado de 27% (volume/volume) de etanol, permitido por lei. Um teste de
verificação foi realizado na seguinte sequência:
Adicionar 50,0 mL de gasolina a uma proveta de 100 mL com tampa esmerilhada; Adicionar, na mesma proveta, 50,0 mL da solução de cloreto de sódio 10% (massa/volume), recém preparada; Tampar a proveta e inverter 10 vezes a proveta e aguardar 10 minutos para realizar a leitura; Após os 10 minutos (tempo para a nítida separação entre as fases), registrar o volume da fase aquosa. O volume da fase aquosa, inicialmente 50,0 mL, sofre um aumento após a mistura com a fase orgânica.
Adicionar 50,0 mL de gasolina a uma proveta de 100 mL com tampa esmerilhada; Adicionar, na mesma proveta, 50,0 mL da solução de cloreto de sódio 10% (massa/volume), recém preparada; Tampar a proveta e inverter 10 vezes a proveta e aguardar 10 minutos para realizar a leitura; Após os 10 minutos (tempo para a nítida separação entre as fases), registrar o volume da fase aquosa. O volume da fase aquosa, inicialmente 50,0 mL, sofre um aumento após a mistura com a fase orgânica.
Resultado: Após três determinações, o volume da fase aquosa aumentou de 50,0 mL para 64,0 mL, nas três determinações.
A porcentagem encontrada de etanol na gasolina foi:
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um técnico do laboratório de ensino em Química Orgânica preparou um experimento envolvendo sacarose e
glicose. Foram preparadas 3,000 L de uma solução de sacarose (de formula molecular C12H22O11) com
concentração 0,150 mol/L e 2,500 L de uma solução de glicose (de fórmula molecular C6H12O6) com
concentração 0,150 mol/L. As massas, em gramas, necessárias à preparação dessas soluções de sacarose e
glicose são, respectivamente:
Dados: Massas Molares (em g/mol): H=1; C=12; O= 16
Dados: Massas Molares (em g/mol): H=1; C=12; O= 16
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaVelocidade de Reação, Energia de Ativação e Catalisadores
Uma pessoa comeu muito no jantar e passou, meia hora depois, a ter uma sensação de azia, resultante do excesso de ácido clorídrico, o HCl, produzido pelo estômago. Então, a pessoa ingeriu, num intervalo de 18horas, 3 comprimidos de remédio antiácido. Suponha que cada comprimido desse remédio contenha 450 mg de hidróxido de alumínio, Al(OH)3, e 450 mg de hidróxido de magnésio, Mg(OH)2. As reações de neutralização ocorrem segundo as equações balanceadas a seguir:
Al(OH)3(s) + 3 HCl(aq) → AlCI3(aq) + 3 H2O(I)
Mg(OH)2(s) + 2 HCl(aq) → MgCl2(aq) + 2 H 2O(I)
No período de 18 horas, a massa de ácido clorídrico neutralizado em miligramas e a quantidade de moléculas de HCl consumida, na neutralização, foram respectiva e aproximadamente:
Dados: Massas Molares: Mg(OH)2 = 58 g/mol; Al(OH)3 = 78 g/mol; HCl = 36,5 g/mol; Constante de Avogadro = 6,0.1023
Al(OH)3(s) + 3 HCl(aq) → AlCI3(aq) + 3 H2O(I)
Mg(OH)2(s) + 2 HCl(aq) → MgCl2(aq) + 2 H 2O(I)
No período de 18 horas, a massa de ácido clorídrico neutralizado em miligramas e a quantidade de moléculas de HCl consumida, na neutralização, foram respectiva e aproximadamente:
Dados: Massas Molares: Mg(OH)2 = 58 g/mol; Al(OH)3 = 78 g/mol; HCl = 36,5 g/mol; Constante de Avogadro = 6,0.1023
Provas
Questão presente nas seguintes provas
Um químico deseja saber se o acetileno, C2H2, pode sofrer uma reação de hidrogenação para se tornar oetano, de acordo com a reação abaixo:
C2H2 (g) + 2 H2 (g) → C2 H 6 (g) HΔº= ?
Embora não tenha encontrado o valor do ΔH de hidrogenação dessa reação em tabelas, encontrou asseguintes entalpias-padrão de combustão:
C2H2 + 5/2 O2 (g) → 2 CO2 (g) + H2O (I) ΔHCº = - 1.301 kJ/mol C2H6 (g) + 7/2 O2 (g) → 2 CO2 (g) + 3 H2O (I) ΔHCº = - 1.561 kJ/mol H2 (g) + 1/2 O2 (g) → H2O (l) ΔHCº = - 286 kJ/mol
C2H2 (g) + 2 H2 (g) → C2 H 6 (g) HΔº= ?
Embora não tenha encontrado o valor do ΔH de hidrogenação dessa reação em tabelas, encontrou asseguintes entalpias-padrão de combustão:
C2H2 + 5/2 O2 (g) → 2 CO2 (g) + H2O (I) ΔHCº = - 1.301 kJ/mol C2H6 (g) + 7/2 O2 (g) → 2 CO2 (g) + 3 H2O (I) ΔHCº = - 1.561 kJ/mol H2 (g) + 1/2 O2 (g) → H2O (l) ΔHCº = - 286 kJ/mol
De posse desses valores, calculando corretamente o ΔH, em kJ/mol, deverá encontrar valor igual a:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container