Foram encontradas 400 questões.
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Provas
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Com relação à titulação de neutralização de um ácido fraco monoprótico por uma base forte, considere as afirmativas abaixo.
I No ponto de equivalência, o ácido fraco remanesce sem se ionizar.
II No ponto de equivalência, o pH será sempre maior que 7.
III Na metade do volume para o ponto de equivalência, o pH é igual ao pKa do ácido fraco.
IV Após o ponto de equivalência, o pH corresponde ao de uma solução tampão.
Das afirmativas, estão corretas
Provas
O sulfato ferroso (FeSO4) reage com o permanganato de potássio (KMnO4) em meio ácido seguindo a reação não balanceada reproduzida abaixo.
aFeSO4(aq) + bKMnO4(aq) + cH2SO4(aq) → dFe2(SO4)3(aq) + eMnSO4(aq) + ƒK2SO4(aq) + gH2O(l)
Os coeficientes estequiométricos indicados por a e f correspondem, respectivamente, a
Provas
Considere a figura abaixo, que representa um sistema utilizado em laboratório de química.
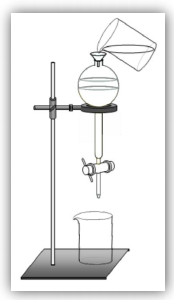
Esse sistema é útil para
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um dado importante para avaliar a qualidade da água é a determinação do índice de dureza da água, que corresponde à presença dos íons Ca2+ e Mg2+. As equações envolvidas para essa avaliação são as seguintes:
Ca2+ + H2Y2- ⇋ CaY2- + 2H+
Ca2+ + MgY2- ⇋ CaY2- + Mg2+
Mg2+ + HIn2- ⇋ MgIn- + H+
MgIn- + H2Y2- ⇋ MgY2- + HIn2- + H+
O técnico do laboratório recebeu e protocolou uma amostra de água para análise de dureza. O volume da amostra utilizado na titulação foi de 100,0 mL, e o volume de solução de EDTA 0,0100 mol L-1 gasto na titulação foi de 25,0 mL. Considere o resultado expresso em mg de CaCO3 por 1000 mL e a classificação da dureza da água, presentes na tabela abaixo.

Com base nas equações e na tabela, essa amostra é classificada como água
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
O técnico recebeu a tarefa de determinar o teor de vitamina C (C6H8O6 – MM=176,12 g mol-1 ) em amostra de comprimidos. Após pulverização e homogeneização pesou uma amostra de 0,1852 g do pó, transferiu para erlenmeyer e dissolveu com cerca de 20,0 mL de águ a destilada. Completada a dissolução adicionou 2,0 g de iodeto de potássio (KI) e 5 mL de ácido sulfúrico (H2SO4) 0,5 mol L-1 . Titulou com solução padrão de iodato de potássio (KIO3) 0,0250 mol L-1 , utilizando como indicador solução de amido a 1%, o volume da solução de iodato de potássio gasto foi de 13,2 mL. Considere a sequência de reações abaixo.
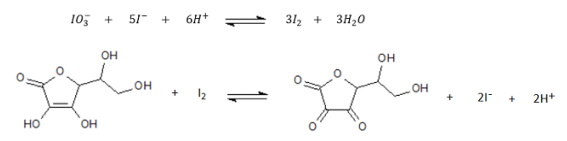
Com base nessas informações conclui-se que o teor de vitamina C no comprimido é de aproximadamente:
Provas
Na Central Analítica do Instituto de Química da UFRN, o técnico de laboratório tem, à disposição, diversos reagentes, utensílios e equipamentos de laboratório. Baseado no princípio das técnicas instrumentais, considere os analitos e as respectivas técnicas de análise abaixo.
I NaCl em soro fisiológico por fotometria de chama e acetona em removedor de esmalte por espectrofotometria UV-VIS.
II NaF em pasta de dente por potenciometria e CaCO3 em comprimido anti-ácido por espectrometria de absorção atômica.
III NaCl em soro fisiológico por espectrofotometria UV-VIS e acetona em removedor de esmalte por espectrometria de absorção atômica.
IV NaF em pasta de dente por cromatografia gasosa e CaCO3 em comprimido anti-ácido por potenciometria.
Os itens que contêm a correlação correta entre os analitos e as respectivas técnicas são
Provas
Considere a figura abaixo que apresenta a curva de calibração obtida para a determinação de DQO pela técnica de espectrofotometria utilizando dicromato de potássio em meio ácido, bem como a equação da reta.
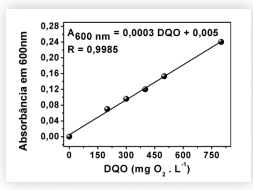
Em uma indústria de processamento de castanha de caju, coletou-se uma amostra de efluente de 100,0 mL para análise de DQO. Após o tratamento apropriado da amostra com dicromato de potássio em meio ácido, mediu-se a sua absorbância em 600 nm e obteve-se um valor de 0,138. Nessa amostra, o valor de DQO em mg O2 L -1 é
Provas
Após uma aula experimental, o técnico de laboratório armazenou uma solução 0,015 mol L-1 de KMnO4 num recipiente de prata. Nesse contexto, considere os dados abaixo.
Dados:
E°(Ag+ /Ag0 )= 0,880 V e E°(MnO4- /Mn2+) = 1,510 V
∆G° = -n F ∆E° (sendo n o número de elétrons e F a constante de Faraday - 96450 C mol-1 )
Com base nesses dados e de acordo com os valores dos potenciais padrão de redução para as duas semi-reações da célula eletroquímica, o recipiente de prata é
Provas
Caderno Container