Foram encontradas 351 questões.
A tabela abaixo mostra alguns dados termodinâmicos para reações não balanceadas na obtenção de H2 (g) a partir de alguns hidrocarbonetos.

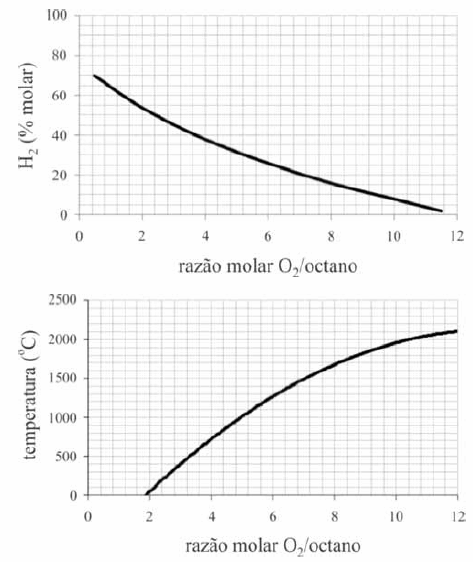
Os gráficos a seguir mostram a influência da razão molar inicial O2/C8H18 na temperatura final e na concentração de hidrogênio produzido, sendo atingido o equilíbrio, quando a reação IV, mostrada na tabela acima, ocorre por um processo adiabático.
M. Krumpelt, T. R. Krause, J. D. Carter, J. P. Kopasz, S. Ahmed. Fuel
processing for fuel cell systems in transportations and portable power
aplications. In: Catalysis Today, v. 77, 2002, p. 3-16.
Tendo como referência as informações acima, julgue o item a seguir.
De acordo com os gráficos, quantidades estequiométricas de O2 (g) e C8H18 (g), reagindo como representado na equação IV, produzem um percentual molar maior que 50% para o H2 (g).
Provas
A tabela abaixo mostra alguns dados termodinâmicos para reações não balanceadas na obtenção de H2 (g) a partir de alguns hidrocarbonetos.

Os gráficos a seguir mostram a influência da razão molar inicial O2/C8H18 na temperatura final e na concentração de hidrogênio produzido, sendo atingido o equilíbrio, quando a reação IV, mostrada na tabela acima, ocorre por um processo adiabático.

M. Krumpelt, T. R. Krause, J. D. Carter, J. P. Kopasz, S. Ahmed. Fuel
processing for fuel cell systems in transportations and portable power
aplications. In: Catalysis Today, v. 77, 2002, p. 3-16.
Tendo como referência as informações acima, julgue o item a seguir.
Na reação IV, apresentada na tabela, a massa de oxigênio gasoso necessária para liberar 632 kJ de calor é maior que 500 g.
Provas
A tabela abaixo mostra alguns dados termodinâmicos para reações não balanceadas na obtenção de H2 (g) a partir de alguns hidrocarbonetos.

Os gráficos a seguir mostram a influência da razão molar inicial O2/C8H18 na temperatura final e na concentração de hidrogênio produzido, sendo atingido o equilíbrio, quando a reação IV, mostrada na tabela acima, ocorre por um processo adiabático.

M. Krumpelt, T. R. Krause, J. D. Carter, J. P. Kopasz, S. Ahmed. Fuel
processing for fuel cell systems in transportations and portable power
aplications. In: Catalysis Today, v. 77, 2002, p. 3-16.
Tendo como referência as informações acima, julgue o item a seguir.
Considerando-se a reação de um mol de cada hidrocarboneto listado nas equações de I a IV na tabela, tem-se a seguinte sequência decrescente dos coeficientes estequiométricos, nas suas respectivas reações balanceadas: j > l > k > i.
Provas
A tabela abaixo mostra alguns dados termodinâmicos para reações não balanceadas na obtenção de H2 (g) a partir de alguns hidrocarbonetos.

Os gráficos a seguir mostram a influência da razão molar inicial O2/C8H18 na temperatura final e na concentração de hidrogênio produzido, sendo atingido o equilíbrio, quando a reação IV, mostrada na tabela acima, ocorre por um processo adiabático.

M. Krumpelt, T. R. Krause, J. D. Carter, J. P. Kopasz, S. Ahmed. Fuel
processing for fuel cell systems in transportations and portable power
aplications. In: Catalysis Today, v. 77, 2002, p. 3-16.
Tendo como referência as informações acima, julgue o item a seguir.
Para a reação II, o rendimento da produção de hidrogênio a partir do octano aumenta à medida que o processo se realiza em temperaturas mais baixas.
Provas
As células combustíveis despontam como a alternativa mais viável para a obtenção de energia elétrica. A figura I, abaixo, mostra a variação da eficiência na conversão de energia com a potência máxima de saída de várias fontes de energias renováveis.
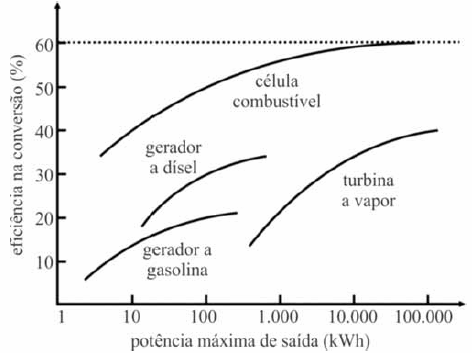
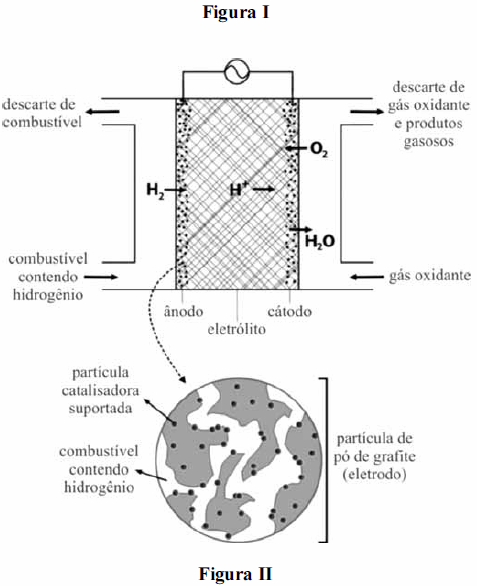
As células combustíveis são, em princípio, baterias que convertem a energia química de uma reação eletroquímica em energia elétrica, como exemplificado na figura II. Na tabela abaixo, são apresentadas semirreações das células e o potencial padrão de redução.

Tendo como referência as informações acima, julgue o item a seguir.
Suponha que, em um processo de conversão energética que envolve uma das máquinas representadas na figura I, foi fornecido ao sistema, durante uma hora, 1,8 × 109 J de energia, sendo produzidos 100 kWh de potência de saída. Nesse caso, o conversor utilizado foi o(a)
Provas
As células combustíveis despontam como a alternativa mais viável para a obtenção de energia elétrica. A figura I, abaixo, mostra a variação da eficiência na conversão de energia com a potência máxima de saída de várias fontes de energias renováveis.


As células combustíveis são, em princípio, baterias que convertem a energia química de uma reação eletroquímica em energia elétrica, como exemplificado na figura II. Na tabela abaixo, são apresentadas semirreações das células e o potencial padrão de redução.

Tendo como referência as informações acima, julgue o item a seguir.
Se a reação na célula combustível representada na figura II é catalisada, então a presença do catalisador aumenta a energia de ativação, o que faz que essa reação se processe mais rapidamente.
Provas
As células combustíveis despontam como a alternativa mais viável para a obtenção de energia elétrica. A figura I, abaixo, mostra a variação da eficiência na conversão de energia com a potência máxima de saída de várias fontes de energias renováveis.


As células combustíveis são, em princípio, baterias que convertem a energia química de uma reação eletroquímica em energia elétrica, como exemplificado na figura II. Na tabela abaixo, são apresentadas semirreações das células e o potencial padrão de redução.

Tendo como referência as informações acima, julgue o item a seguir.
Na situação ilustrada na figura II, o eletrólito tem a função de conduzir elétrons e os íons H+ em direções opostas, para que seja mantido o balanço de cargas na solução aquosa.
Provas
As células combustíveis despontam como a alternativa mais viável para a obtenção de energia elétrica. A figura I, abaixo, mostra a variação da eficiência na conversão de energia com a potência máxima de saída de várias fontes de energias renováveis.


As células combustíveis são, em princípio, baterias que convertem a energia química de uma reação eletroquímica em energia elétrica, como exemplificado na figura II. Na tabela abaixo, são apresentadas semirreações das células e o potencial padrão de redução.

Tendo como referência as informações acima, julgue o item a seguir.
A equação química da reação global que ocorre na célula combustível representada na figura II é dada por 2 2 , e sua força eletromotriz é igual 2H2O(l)→ 2H2 (g) + O2 (g) a 1,22 V.
Provas
As células combustíveis despontam como a alternativa mais viável para a obtenção de energia elétrica. A figura I, abaixo, mostra a variação da eficiência na conversão de energia com a potência máxima de saída de várias fontes de energias renováveis.


As células combustíveis são, em princípio, baterias que convertem a energia química de uma reação eletroquímica em energia elétrica, como exemplificado na figura II. Na tabela abaixo, são apresentadas semirreações das células e o potencial padrão de redução.

Tendo como referência as informações acima, julgue o item a seguir.
Durante o funcionamento da célula combustível representada na figura II, os elétrons fluem pelo circuito externo, do ânodo para o cátodo.
Provas
As células combustíveis despontam como a alternativa mais viável para a obtenção de energia elétrica. A figura I, abaixo, mostra a variação da eficiência na conversão de energia com a potência máxima de saída de várias fontes de energias renováveis.


As células combustíveis são, em princípio, baterias que convertem a energia química de uma reação eletroquímica em energia elétrica, como exemplificado na figura II. Na tabela abaixo, são apresentadas semirreações das células e o potencial padrão de redução.

Tendo como referência as informações acima, julgue o item a seguir.
As perdas energéticas causadas pelo efeito Joule nos geradores a gasolina constituem uma das razões da baixa eficiência desses dispositivos, se comparada à eficiência das células combustíveis.
Provas
Caderno Container