Foram encontradas 50 questões.
Qual é o conjunto solução da inequação x+1 ≤0?
x2-5x+6
Provas
O texto a seguir fundamenta as questões 48 a 50
O Brasil produz, em média, 350 milhões de toneladas de minério de Ferro por ano. Essas rochas são compostas majoritariamente por Hematita (Fe2O3). O Ferro metálico é obtido por meio desse óxido e, quando o metal está em contato com o ar e com a atmosfera úmida, algumas reações químicas podem acontecer. Em relação a esses processos, responda as questões 48 a 50.
O processo de produção da ferrugem é natural. Porém, em regiões litorâneas, a observação de materiais com pontos de ferrugem é mais frequente. A alternativa que explica esse fato é:
Provas
O texto a seguir fundamenta as questões 48 a 50
O Brasil produz, em média, 350 milhões de toneladas de minério de Ferro por ano. Essas rochas são compostas majoritariamente por Hematita (Fe2O3). O Ferro metálico é obtido por meio desse óxido e, quando o metal está em contato com o ar e com a atmosfera úmida, algumas reações químicas podem acontecer. Em relação a esses processos, responda as questões 48 a 50.
A equação química que representa o processo de produção da ferrugem é enunciada como:
Fe(s) + O2(g) + H2O(l) -> 2Fe(OH)2 (aq)
Nesse processo, indique o que acontece com as espécies reagentes e os produtos:
Provas
O texto a seguir fundamenta as questões 48 a 50
O Brasil produz, em média, 350 milhões de toneladas de minério de Ferro por ano. Essas rochas são compostas majoritariamente por Hematita (Fe2O3). O Ferro metálico é obtido por meio desse óxido e, quando o metal está em contato com o ar e com a atmosfera úmida, algumas reações químicas podem acontecer. Em relação a esses processos, responda as questões 48 a 50.
Os estados de oxidação do Ferro na hematita e no ferro metálico são, respectivamente:
Provas
O texto a seguir fundamenta as questões 45 a 47
 O pH do suco gástrico está em aproximadamente 2,5. Quando esse líquido presente no estômago se torna ainda mais ácido, normalmente, fazemos uso de um “Antiácido” que geralmente é composto de uma base fraca. Um antiácido muito utilizado no mercado é descrito de acordo com a composição química apresentada no rótulo da imagem ao lado. As equações químicas não balanceadas que representam a ação do antiácido são:
O pH do suco gástrico está em aproximadamente 2,5. Quando esse líquido presente no estômago se torna ainda mais ácido, normalmente, fazemos uso de um “Antiácido” que geralmente é composto de uma base fraca. Um antiácido muito utilizado no mercado é descrito de acordo com a composição química apresentada no rótulo da imagem ao lado. As equações químicas não balanceadas que representam a ação do antiácido são:
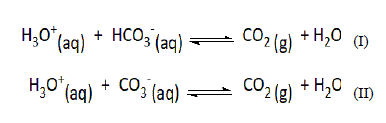
Sendo a equação (I) relativa à ação do bicarbonato de sódio e a equação (II) relativa à ação do carbonato de sódio.
Dados: H: 1g/mol; C: 12 g/mol; O: 16g/mol; Na: 23 g/mol.
Em relação ao apresentado responda as questões de 45 a 47.
As duas equações têm como produto da reação do gás o dióxido de carbono. Considerando o comportamento desse gás como ideal, o que aconteceria com o equilíbrio químico caso a pressão do sistema aumentasse?
Provas
O texto a seguir fundamenta as questões 45 a 47
 O pH do suco gástrico está em aproximadamente 2,5. Quando esse líquido presente no estômago se torna ainda mais ácido, normalmente, fazemos uso de um “Antiácido” que geralmente é composto de uma base fraca. Um antiácido muito utilizado no mercado é descrito de acordo com a composição química apresentada no rótulo da imagem ao lado. As equações químicas não balanceadas que representam a ação do antiácido são:
O pH do suco gástrico está em aproximadamente 2,5. Quando esse líquido presente no estômago se torna ainda mais ácido, normalmente, fazemos uso de um “Antiácido” que geralmente é composto de uma base fraca. Um antiácido muito utilizado no mercado é descrito de acordo com a composição química apresentada no rótulo da imagem ao lado. As equações químicas não balanceadas que representam a ação do antiácido são:
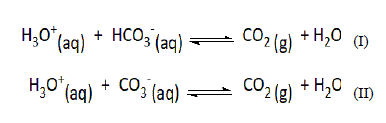
Sendo a equação (I) relativa à ação do bicarbonato de sódio e a equação (II) relativa à ação do carbonato de sódio.
Dados: H: 1g/mol; C: 12 g/mol; O: 16g/mol; Na: 23 g/mol.
Em relação ao apresentado responda as questões de 45 a 47.
Considerando que um comprimido de antiácido tem 5g, qual a porcentagem relativa de bicarbonato de sódio e o número de mols total presente nesse sal?
Provas
O texto a seguir fundamenta as questões 45 a 47
 O pH do suco gástrico está em aproximadamente 2,5. Quando esse líquido presente no estômago se torna ainda mais ácido, normalmente, fazemos uso de um “Antiácido” que geralmente é composto de uma base fraca. Um antiácido muito utilizado no mercado é descrito de acordo com a composição química apresentada no rótulo da imagem ao lado. As equações químicas não balanceadas que representam a ação do antiácido são:
O pH do suco gástrico está em aproximadamente 2,5. Quando esse líquido presente no estômago se torna ainda mais ácido, normalmente, fazemos uso de um “Antiácido” que geralmente é composto de uma base fraca. Um antiácido muito utilizado no mercado é descrito de acordo com a composição química apresentada no rótulo da imagem ao lado. As equações químicas não balanceadas que representam a ação do antiácido são:
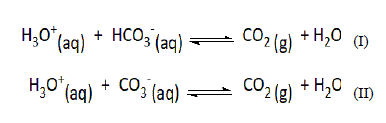
Sendo a equação (I) relativa à ação do bicarbonato de sódio e a equação (II) relativa à ação do carbonato de sódio.
Dados: H: 1g/mol; C: 12 g/mol; O: 16g/mol; Na: 23 g/mol.
Em relação ao apresentado responda as questões de 45 a 47.
Os Coeficientes estequiométricos das equações serão:
Provas
O gráfico abaixo representa a variação da solubilidade em água em função da temperatura do nitrato de chumbo.
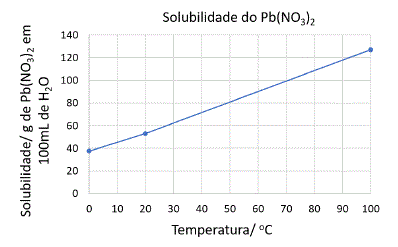
Se 125g de solução saturada de Pb(NO3)2 a 100ºC forem resfriados até 50ºC a massa total do sal que se precipita será de:
Provas
Fulerenos são formas alotrópicas do carbono, de fórmula química C60. Possuem diversas aplicações, com destaque para as áreas de bioquímica e medicina. O representante mais estável e conhecido da família apresenta sua estrutura representada a seguir, e apresenta características apolares.
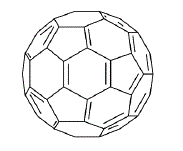
Um estudante, trabalhando com essa classe de moléculas, resolveu solubilizá-la para a realização de testes químicos. Qual solvente dentre as opções listadas abaixo teria o maior poder de solubilização da molécula:
Provas
O medicamento conhecido como sulfadiazina de prata é bastante conhecido e é um potente bactericida de uso tópico historicamente utilizado para o tratamento de queimaduras de segundo e terceiro graus. A sulfadiazina de prata pode ser representada por:
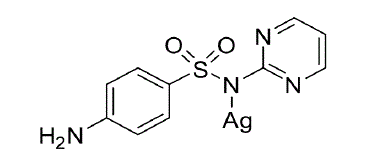
Durante o tratamento, uma pessoa aplica cerca de 119 mg desse fármaco, ou seja, essa pessoa está absorvendo: Dados: H=1 g/mol; C= 12g/mol; N=14g/mol; O= 16 g/mol; S=32 g/mol e Ag=108 g/mol;
Provas
Caderno Container