Foram encontradas 50 questões.
Os óxidos de nitrogênio, denominados NOx, podem ser formados naturalmente por descargas elétricas na atmosfera (raios).
Dessa forma, é produzido o NO gasoso pela reação entre os gases N2 e O2 presentes na atmosfera, de acordo com a equação:
N2(g) + O2(g) + energia !$ \rightarrow !$ NO (g)
O processo natural de produção do monóxido de nitrogênio NÃO é uma reação
Provas
Os metais, em condições ambientes e em estado puro, compõem um grupo de elementos químicos sólidos (com exceção do mercúrio, que é líquido). Dentre esses elementos, alguns apresentam densidade ainda mais elevada que a dos demais em virtude das estruturas compactas dos seus retículos cristalinos. Uma pequena barra metálica pesa 114 g e tem dimensões de 6 cm × 2 cm × 0,5 cm.
Qual a densidade, em g/cm3, desse metal?
Provas
O aroma de frutas deve-se principalmente à presença de algumas substâncias orgânicas, que são bastante utilizadas na indústria alimentícia (as embalagens de alimentos trazem os dizeres: sabor artificial de... ou aroma artificial de...).
Analise a fórmula estrutural de um dos componentes do aroma da maçã verde.
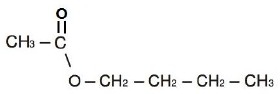
A função orgânica a que pertence essa substância e o nome IUPAC dela são, respectivamente:
Provas
A água do mar representa 97% da água da Terra, cobre 71% da superfície do Planeta e é rica em cloreto de sódio, com 2,5% em massa.
Qual a massa, em quilogramas, de água do mar que deve ser evaporada para se obter 200 g desse sal?
Provas
Para ocorrer uma reação química entre duas substâncias, é preciso fornecer certa quantidade de energia, geralmente na forma de calor, que favoreça o encontro e a colisão entre tais substâncias. A energia também é necessária para romper ligações químicas existentes entre os átomos de cada substância, favorecendo, assim, a ocorrência de outras ligações químicas e a síntese de uma nova substância a partir de duas iniciais.
O “caminho” da energia do processo é mostrado no diagrama abaixo.
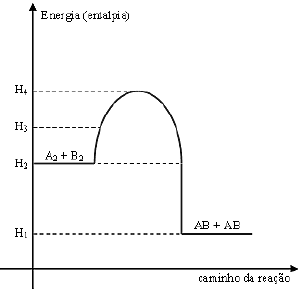
A coluna da esquerda apresenta dados energéticos característicos do andamento da reação (quantidades de energia das respectivas etapas da reação) (H1 a H4) e a da direita, a especificação de cada um deles.
Numere a coluna da direita de acordo com a da esquerda.
1 - H1
2 - H2
3 - H3
4 - H4
( ) A energia do sistema é maior, mas ainda insuficiente para que ocorra uma colisão efetiva.
( ) A energia, nesse ponto, é suficiente para a reação. Dá-se aqui a formação de um estado de transição.
( ) As moléculas do produto (AB) estão definitivamente formadas.
( ) As moléculas reagentes (A2 e B2) não possuem energia suficiente para reagirem.
Marque a sequência correta.
Provas
Os ácidos estão muito presentes no organismo humano. Muitos são fornecidos pela alimentação, como frutas cítricas, nas quais se encontram os ácidos cítrico e ascórbico (vitamina C).
São alguns dos ácidos mais comuns na química do cotidiano das pessoas:
- Ácido clorídrico (HCl) (Ka !$ \approx !$ 107): reagente muito usado na indústria e no laboratório, é encontrado no suco gástrico e tem o papel de auxiliar na digestão.
- Ácido fosfórico (H3PO4) (Ka = 7,5 × 10-3): usado como acidulante em refrigerantes, balas e gomas de mascar.
- Ácido carbônico (H2CO3) (Ka = 4,6 × 10-7): as águas e refrigerantes gaseificados têm seu diferencial (mais refrescantes) graças a esse ácido, formado na reação do gás carbônico com a água.
- Ácido fluorídrico (HF) (Ka = 6,8 × 10-4): utilizado em tratamento de água de abastecimento público com o objetivo de combater cárie dentária, possui a capacidade de corroer o vidro, sendo, por isso, armazenado apenas em frascos de polietileno.
Sobre esses ácidos, é correto afirmar:
Provas
Diariamente, várias vezes, até sem que se perceba, realiza-se o processo de diluição de soluções. Em laboratórios químicos e em indústrias, esse processo é muito importante, porque o Técnico Químico precisa preparar diversas soluções com concentrações conhecidas.
Sobre a diluição das soluções, analise as afirmativas.
I - Diluir uma solução significa diminuir sua concentração (diluição e concentração são processos opostos).
II - A retirada de solvente de uma solução deixa-a mais diluída, uma vez que é aumentada a relação soluto-solvente.
III - Um litro de determinado suco tem 42 g de soluto; diluindo-o a 3 litros com água, a concentração passa a ser de 14 g/L, mas, nessa solução, a massa do soluto permanece inalterada.
IV - Uma substância química preparada em uma diluição de 1/100 (1:100) v/v indica que um frasco de 100 mL contém 1 mL da substância (soluto) e 100 mL do solvente.
Está correto o que se afirma em
Provas
Em um recipiente fechado, certa massa de carbamato de amônio sólido (NH2COONH4) decompõe-se em amônia (NH3) e dióxido de carbono (CO2), ambos gasosos. A massa da NH3 formada nessa reação de decomposição é igual a 17 gramas.
Nessas condições, sobre essa reação, pode-se afirmar:
Provas
Na presença do oxigênio do ar, o monóxido de nitrogênio (NO) oxida-se rapidamente a dióxido de nitrogênio (NO2), um gás de coloração vermelho-tijolo. Uma vez formado, o dióxido de nitrogênio produz, em ambiente fechado, o tetróxido de dinitrogênio (N2O4) e entra em equilíbrio com este de acordo com a equação N2O4 !$ \leftrightharpoons !$ NO2. A 150ºC, o valor da constante de equilíbrio para esse equilíbrio gasoso é igual a 3,2. Na mesma temperatura, os valores das concentrações desses gases são apresentados a seguir, em quatro sistemas diferentes.
| Sistema \ Conc. molar | I | II | III | IV |
| NO2 | 2 | 3 | 4 | 5 |
| N2O4 | 3 | 4 | 5 | 6 |
Dentre os sistemas dados, o único que se encontra em equilíbrio é o
Provas
A solubilidade dos sais em água pode ser estabelecida pela quantidade máxima de soluto numa solução saturada a uma dada temperatura.
O gráfico a seguir mostra a variação da solubilidade de um dado sal na água em função da temperatura.
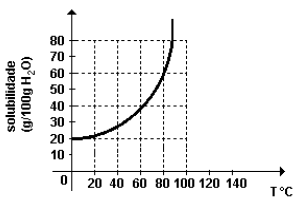
A partir das informações do gráfico, assinale a afirmativa correta.
Provas
Caderno Container