Foram encontradas 13.431 questões.
Internet: <brasilescola.uol.com.br>.
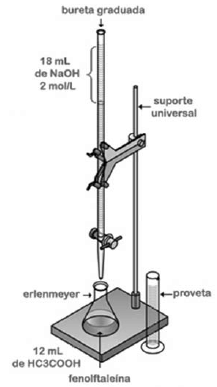
Tendo como referência a figura precedente, que representa uma titulação volumétrica, julgue o próximo item.
Entre as vidrarias empregadas em análises analíticas, a bureta e a proveta são as que exibem o mais elevado grau de precisão e exatidão, em comparação com o balão volumétrico.
Provas
Acerca da eliminação de resíduos químicos, julgue o item a seguir.
Compostos orgânicos não halogenados com menos de 5 carbonos devem ser descartados na rede de esgoto.
Provas
Acerca do uso e da conservação de aparelhagens comuns de laboratório, julgue o item a seguir.
Para a melhor conservação de eletrodos de vidro para a medida de pH, é indicado o uso de soluções de ácido fluorídrico 3 mol/L como líquido de repouso para os eletrodos.
Provas
É atividade essencial do técnico de laboratório o preparo de soluções. Além das propriedades físicas, como densidade, o técnico deve conhecer, na prática, as definições de concentração e saber fazer diluições. É comum preparar, diluir e manipular soluções com concentração expressa em massa, em quantidade de matéria, fração molar e fração em massa. Acerca desse assunto e de aspectos correlatos, julgue o item que se segue.
Uma solução 0,1 mol/L de NaOH tem concentração em massa maior que 5,0 g/L de NaOH, considerando-se a massa molar do NaOH igual a 40 g/mol.
Provas
O hidróxido de sódio, sólido bastante higroscópico e reativo com o CO2 do ar, é comumente utilizado na padronização e na dosagem de soluções ácidas em laboratórios. Normalmente, para essas titulações, são utilizadas soluções diluídas de NaOH. Em relação a esse assunto, julgue o item a seguir.
Quanto maior a massa molar de um reagente, maior será o erro relativo associado com a pesagem desse reagente, principalmente no preparo de soluções mais diluídas.
Provas
Considere as seguintes afirmações sobre equilíbrio de fases e propriedades coligativas.
I. A adição de um soluto não volátil a um solvente puro, em uma dada temperatura constante, sempre provoca uma diminuição na pressão de vapor.
II. A pressão de vapor de uma solução formada por dois líquidos voláteis é sempre menor que a pressão de vapor dos líquidos puros a uma mesma temperatura.
III. O valor absoluto do abaixamento no ponto de congelamento de uma solução é menor se o soluto dimeriza parcialmente no solvente, comparado ao sistema nas mesmas condições em que não há a dimerização do soluto.
IV. A pressão osmótica é a pressão exercida pelas moléculas de soluto numa membrana semipermeável.
V. Uma mistura formada por duas substâncias nunca solidifica inteiramente em uma única temperatura.
Assinale a opção que contém a(s) afirmação(ões) CORRETA(S):
Provas
Em um reator mantido à temperatura constante, PCl5(g) encontra-se em equilíbrio com 1 atm de Cl2(g) e 2 atm de PCl3(g). Sabendo-se que a constante de equilíbrio da reação de dissociação do PCl5(g) nessa temperatura é kp = 4, assinale a alternativa que apresenta a nova pressão de equilíbrio do PCl5(g) (em atm) após adição de mais 2 atm desse gás ao reator.
Provas
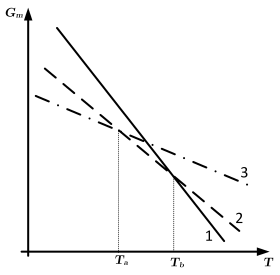
O gráfico qualitativo abaixo ilustra a relação da energia livre de Gibbs molar !$ (G_m) !$ de uma substância pura com a temperatura !$ (T) !$ em seus estados sólido, líquido e gasoso.
Considere as afirmativas abaixo:
I. As três retas são decrescentes, pois a expressão !$ G_m = H_m - TS_m !$ é representada por uma reta com inclinação definida pelo termo !$ (-S_m) !$.
II. As retas 1, 2 e 3 representam a substância nos estados sólido, líquido e gasoso, respectivamente.
III. A temperatura !$ T_a !$ indica o ponto de fusão da substância nas condições em que o gráfico foi obtido.
IV. Em temperaturas mais altas do que !$ T_b !$, a fase 1 da substância é a mais estável.
Assinale as alternativas que são verdadeiras.
Provas
Uma reação entre dois líquidos !$ A !$ e !$ B !$ produz dois compostos gasosos !$ C !$ e !$ D !$, de acordo com a estequiometria!$ A + B \rightarrow C + D !$. Se conduzida a pressão e temperatura constantes, pode-se afirmar que:
Provas
A densidade é uma propriedade que relaciona massa e volume de um material. Um estudante iniciou um procedimento de determinação da densidade de uma amostra sólida desconhecida. Primeiro ele determinou a massa da amostra, obtendo 27,8 g. Em seguida, utilizou uma proveta, graduada em mililitro, com água para determinar o volume da amostra, conforme esquematizado na figura. Considere a densidade da água igual a 1 g/mL.
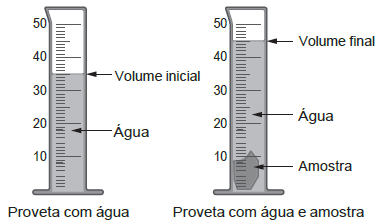
A densidade da amostra obtida, em g/mL, é mais próxima de
Provas
Caderno Container