Foram encontradas 13.432 questões.
Os espetáculos de fogos de artifício são mais que uma forma de entretenimento: os efeitos e as cores visualizadas resultam de reações entre diferentes sais, agentes oxidantes e redutores. Na pólvora (a carga explosiva dos fogos), agentes oxidantes, como o perclorato de potássio (KClO4), estão misturados com agentes redutores, como o enxofre, o que é responsável pela produção da energia necessária para a explosão. A seguir, são apresentadas as equações químicas não balanceadas das reações que ocorrem no processo de explosão de determinados tipos de fogos de artifício.
reação I: KClO4(s) → KCl(s) + O2(g)
reação II: S(s) + O2(g) → SO2(g)
As luzes coloridas emitidas durante a queima de fogos são resultado da luminescência, fenômeno que ocorre quando os elétrons dos átomos dos sais metálicos, previamente excitados pela energia da explosão, retornam aos níveis energéticos de origem, liberando energia na forma de fótons de luz visível. A tabela a seguir mostra alguns elementos e as cores características que eles produzem na luminescência.
|
elemento(s) |
coloração |
|
Li |
rosa |
|
Cu |
azul |
|
Mg, Al ou Ti |
prateado |
|
Ca |
vermelho |
|
Ba |
verde |
|
K |
violeta |
A partir das informações do texto, julgue os itens de 11 a 18 e faça o que se pede no item 19, que é do tipo B.
Diferentemente dos materiais sólidos incandescentes, cujo espectro de emissão é contínuo, átomos isolados em fase gasosa possuem espectro de emissão descontínuo e característico, com picos estreitos e bem definidos, podendo, contudo, uma ou mais linhas do espectro de emissão de átomos distintos apresentar frequências coincidentes.
Provas
Os espetáculos de fogos de artifício são mais que uma forma de entretenimento: os efeitos e as cores visualizadas resultam de reações entre diferentes sais, agentes oxidantes e redutores. Na pólvora (a carga explosiva dos fogos), agentes oxidantes, como o perclorato de potássio (KClO4), estão misturados com agentes redutores, como o enxofre, o que é responsável pela produção da energia necessária para a explosão. A seguir, são apresentadas as equações químicas não balanceadas das reações que ocorrem no processo de explosão de determinados tipos de fogos de artifício.
reação I: KClO4(s) → KCl(s) + O2(g)
reação II: S(s) + O2(g) → SO2(g)
As luzes coloridas emitidas durante a queima de fogos são resultado da luminescência, fenômeno que ocorre quando os elétrons dos átomos dos sais metálicos, previamente excitados pela energia da explosão, retornam aos níveis energéticos de origem, liberando energia na forma de fótons de luz visível. A tabela a seguir mostra alguns elementos e as cores características que eles produzem na luminescência.
|
elemento(s) |
coloração |
|
Li |
rosa |
|
Cu |
azul |
|
Mg, Al ou Ti |
prateado |
|
Ca |
vermelho |
|
Ba |
verde |
|
K |
violeta |
A partir das informações do texto, julgue os itens de 11 a 18 e faça o que se pede no item 19, que é do tipo B.
O fenômeno da luminescência dos materiais não está restrito à emissão de fótons na frequência do espectro visível. Conforme sua estrutura atômica, um átomo pode emitir fótons na região do ultravioleta, dos raios X e até mesmo dos raios gama, uma vez que os níveis de energia eletrônicos são quantizados.
Provas
Provas
Provas
Em alguns casos, há necessidade de coletar-se o produto de uma reação sob a água para evitar que ele escape e misture-se com o ar atmosférico. Uma amostra de 500 mL de oxigênio foi coletada sob a água a 23 oC e pressão de 1 atm. Sabendo-se que a pressão de vapor da água a 23 oC é 0,028 atm, o volume que o O2 seco ocupará naquelas condições de temperatura e pressão será
Provas
Ao adicionar um corante vegetal vermelho solúvel na água de um jarro cheio de rosas brancas, um participante da feira de ciências de uma escola pública do interior do Estado do Ceará transformou as rosas brancas em rosas vermelhas. O transporte do líquido até as pétalas ocorreu por conta da
Provas
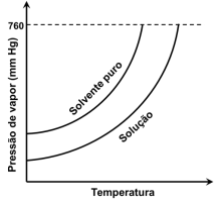
A partir do gráfico, é CORRETO afirmar:
Provas
A Figura abaixo mostra um diagrama de fases de uma substância pura.
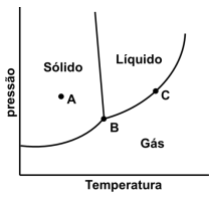
O número de fases que estão presentes em cada um dos pontos circulares identificados como A, B e C, respectivamente, nessa figura, é
Provas
As diferentes etapas do tratamento da água para abastecimento requerem a realização de análises físico-químicas, com o objetivo de acompanhar a eficiência dessas etapas, determinando a necessidade ou não da implementação de medidas preventivas e/ou corretivas, e monitorando os principais parâmetros relativos à potabilidade da água.
Considerando as análises realizadas em cada etapa do tratamento de água, atente aos itens a seguir e escreva V ou F conforme sejam verdadeiros ou falsos.
( ) Água Bruta: pH, cloro residual, alcalinidade, cor, turbidez e alumínio.
( ) Água Coagulada: pH, alcalinidade, cor, turbidez e alumínio.
( ) Água Decantada: cor, turbidez, pH e alcalinidade.
( ) Água Tratada: os mesmos parâmetros avaliados na água bruta, sendo acrescidas as análises bacteriológicas.
Está correta, de cima para baixo, a seguinte sequência:
Provas
O ensaio com jartest (teste de jarros) é um ensaio utilizado rotineiramente em Estações de tratamento de água (ETA) com o objetivo de controlar as operações das ETAs. Nele são simuladas as etapas de coagulação, floculação e decantação.
Em relação às informações obtidas a partir desse ensaio, é correto afirmar que
Provas
Caderno Container