Foram encontradas 13.432 questões.
Provas
Provas
Provas
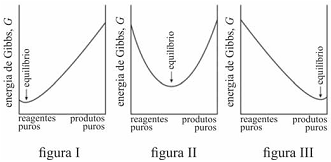
É possível prever, termodinamicamente, se os reagentes de uma mistura têm a tendência espontânea para se transformarem em produtos, se a composição, no equilíbrio, será modificada ao se alterarem as condições de um sistema, entre outros comportamentos termodinâmicos. Acerca de equilíbrio químico e considerando os gráficos representados nas figuras I, II e III, que mostram três situações de equilíbrio, julgue o item que se segue.
Na reação representada pelo gráfico da figura I, quantidades muito pequenas dos reagentes se convertem em produtos antes que G alcance seu valor mínimo e a reação se processe lentamente.
Provas

É possível prever, termodinamicamente, se os reagentes de uma mistura têm a tendência espontânea para se transformarem em produtos, se a composição, no equilíbrio, será modificada ao se alterarem as condições de um sistema, entre outros comportamentos termodinâmicos. Acerca de equilíbrio químico e considerando os gráficos representados nas figuras I, II e III, que mostram três situações de equilíbrio, julgue o item que se segue.
O critério termodinâmico para uma transformação espontânea, à temperatura e à pressão constantes, é que a variação da energia de Gibbs seja maior que zero.
Provas

É possível prever, termodinamicamente, se os reagentes de uma mistura têm a tendência espontânea para se transformarem em produtos, se a composição, no equilíbrio, será modificada ao se alterarem as condições de um sistema, entre outros comportamentos termodinâmicos. Acerca de equilíbrio químico e considerando os gráficos representados nas figuras I, II e III, que mostram três situações de equilíbrio, julgue o item que se segue.
Em uma reação química, a variação da energia de Gibbs de reação com a temperatura depende da entropia de reação. A energia de Gibbs de uma reação que produz gás aumenta com o aumento da temperatura.
Provas

Caso G varie como apresentado no gráfico da figura III, uma proporção alta de produtos tende a se formar antes de G alcançar seu mínimo.
Provas
Com relação à energia interna e à primeira lei da termodinâmica, julgue o item a seguir.
Um processo é considerado espontâneo quando ocorre sem a influência externa. A entropia de um sistema isolado aumenta durante qualquer mudança espontânea.
Provas
Com relação à energia interna e à primeira lei da termodinâmica, julgue o item a seguir.
Se, em um sistema adiabático, ocorre um processo reversível, a variação da entropia é maior que zero.
Provas
Com relação à energia interna e à primeira lei da termodinâmica, julgue o item a seguir.
A única forma de mudar a energia interna de um sistema fechado é transferir energia para ele na forma de calor ou trabalho.
Provas
Caderno Container