Foram encontradas 13.432 questões.
Alta pureza e solubilidade, grande massa molar, além de fácil obtenção, são características necessárias para um bom
Provas
Leia a tabela 2 a seguir.
Tabela 2
|
Indicador |
Faixa de viragem (pH) |
|
Azul de bromofenol |
3,0 - 4,6 |
|
Alaranjado de metila |
3,1 - 4,1 |
|
Vermelho de metila |
4,4 - 6,2 |
|
Fenolftaleína |
8,2 - 10,0 |
|
Carmim-de-índigo |
11,4 - 13,0 |
Dos indicadores apresentados na tabela, quais deles podem ser, respectivamente, utilizados sem causar um erro analítico na titulação para os pares 1) ácido forte-base forte, 2) ácido fraco-base forte e 3) base fraca-ácido forte?
Provas
Na análise química qualitativa, para a identificação de substâncias de interesse analítico são comuns dois tipos de ensaios: aqueles feitos por via seca e aqueles que são realizados por via úmida. A técnica que caracteriza um ensaio por via seca é a
Provas
O sistema termodinâmico em estudo pode ser demarcado por uma fronteira ou superfície de controle, podendo ser caracterizado como um sistema fechado ou volume de controle. Para este último, tem-se a seguinte representação gráfica de um compressor (C):
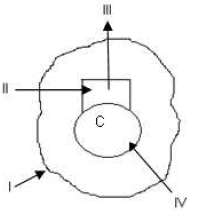
Na representação, os elementos I, II, III e IV são, respectivamente:
Provas
O iodo é uma das poucas substâncias que passam do estado sólido para o estado gasoso e vice-versa em um processo conhecido como sublimação. A equação que representa essa transformação é a seguinte:
I2 (s) à I2 (g) \( \Delta \)H = 62,4 kJ
Considerando essa equação, a quantidade de energia necessária para sublimar 25 g de iodo sólido é, aproximadamente:
Provas
A sacarose e o cloreto de sódio apresentam semelhanças físicas, pois ambos se constituem como sólidos brancos e cristalinos. Qual é a propriedade mais adequada para a identificação e a diferenciação dessas substâncias em laboratório?
Provas
A adição de cloro na água forma ácido hipocloroso e íon hipoclorito. Devido à sua polaridade, o ácido hipocloroso tem facilidade de penetração na membrana celular, inativando as enzimas por reações de oxidação, e ação bacteriana mais forte que o íon hipoclorito. O pH e a temperatura da água são fatores que afetam a cloração, conforme demonstrado no gráfico a seguir:
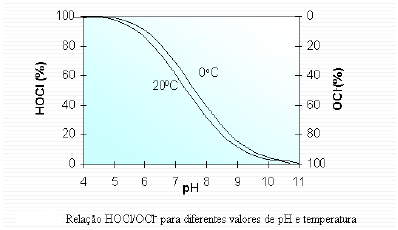
Disponível em: <http://www.ens.ufsc.br/corseuil/antigo//parametros/clorores.html>. Acesso em: 05 fev. 2014.
Considerando as informações do gráfico, para uma ação mais eficaz de desinfecção pelo uso de cloro, a concentração hidrogeniônica de uma amostra de água a 20 ºC deve ser:
Provas
Para uma aula experimental será necessário utilizar uma solução padronizada de ácido clorídrico 0,05 mol/L. Para a padronização, o técnico realizou a análise em triplicata utilizando as seguintes alíquotas de carbonato de sódio, como padrão primário: m1 = 0,0647 g; m2 = 0,0650 g; m3 = 0,0674 g. Considerando que foram gastos, em média, 23,40 mL da solução ácida na titulação, assinale a alternativa que apresenta a concentração real da solução de ácido clorídrico, expressa em mol/L.
Provas
Um analista precisou verificar a concentração de uma solução aquosa de sacarose recentemente preparada. Para a verificação, estava disponível no laboratório um refratômetro de Abbae, e uma curva de calibração para soluções aquosas de sacarose, mostrada a seguir. A leitura do índice de refração da solução analisada apresentou valor de 1,104. Qual a concentração em % da solução de sacarose ?
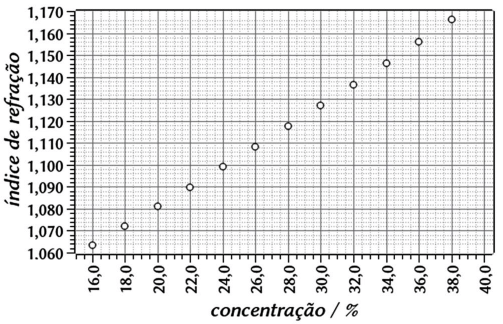
Provas
Uma aula experimental aborda a verificação do ponto de equivalência da reação de uma solução aquosa de ácido sulfúrico 0,10 mol/L com uma solução aquosa de hidróxido de potássio 5% (m/V). O laboratório de química dispõe dos seguintes indicadores de pH (acompanhados dos valores de pH da zona de transição):
1. azul de timol (1,2 - 2,8)
2. amarelo de metila (2,9 - 4,0)
3. verde de bromocresol (4,0 - 5,6)
4. azul de bromotimol (6,0 - 7,6)
5. azul de timol (8,0 - 9,6)
Assinale a opção que correspondente ao indicador que deve ser utilizado no experimento descrito.
Provas
Caderno Container