Foram encontradas 13.431 questões.
A figura abaixo apresenta a configuração geral de um instrumento para realização de:
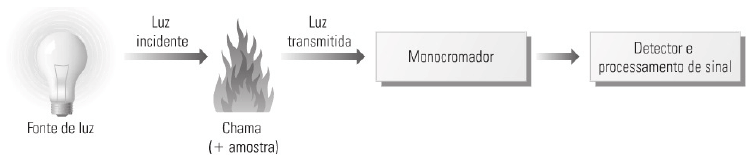
(Hage, D.S. & Carr, J.D. Química analítica e análise quantitativa. 1ª Ed. – São Paulo: Pearson Prentice Hall, 2012)
Provas
A chama, num espectrômetro de absorção atômica tem como principal função a:
Provas
O material particulado atmosférico tem recebido atenção devido a problemas que causam à saúde humana. É correto afirmar que:
Provas
São equipamentos indicados para coletar amostras de águas superficiais e sedimentos, respectivamente:
Provas
O padrão primário é uma substância extremamente importante em química analítica e é usada como material de referência em titulações. Assinale a alternativa incorreta em relação ao padrão primário:
Provas
A absortividade molar de certo composto A em 370 nm é igual a 3200 cm-1/(mol/L). A faixa linear adequada para quantificação deste composto é de 0,05 – 0,90 de absorbância. Três amostras líquidas distintas foram submetidas a medidas de absorbância no comprimento de onda supracitado usando uma cubeta de 15 mm de caminho ótico. Os dados obtidos por espectrofotometria estão na tabela abaixo:
| AMOSTRA | ABSORBÂNCIA |
| 1 | 0,33 |
| 2 | 0,48 |
| 3 | 0,70 |
Considerando que a absorbância exibida na tabela é oriunda apenas do composto A, a concentração (mmol/L) deste composto nas amostras 1, 2 e 3 são, respectivamente:
Provas
Considere uma solução A que apresenta 82% de transmitância numa cubeta de 1,5cm de caminho ótico. A alternativa que representa o comprimento da cubeta (caminho ótico) para que se tenha 82% de transmitância triplicando-se a concentração da Solução A é (A solução segue a lei de Lambert-Beer):
Provas
Uma análise espectrofotométrica foi realizada numa certa amostra para determinação do teor de cobre. Os seguintes procedimentos foram adotados:
1- Pesou-se 9,000 g de amostra e a mesma foi tratada com ácido sulfúrico em recipiente adequado (convertendo todo o cobre em CuSO4).
2- Todo o conteúdo do procedimento 1 foi transferido para um balão volumétrico 200mL e completado com água.
3- Uma alíquota da solução obtida em 2 foi usada para leitura direta no espectrofotômetro.
4- Uma curva analítica foi construída com um reagente de CuSO4 para determinação do teor de cobre na amostra.
As absorbâncias dos pontos da curva e da amostra foram obtidas no comprimento de onda igual a 670 nm. Os dados obtidos foram:
| [CuSO4]/ mol.L-1 | ABSORVÂNCIA |
| 0,00 | 0,000 |
| 0,10 | 0,355 |
| 0,20 | 0,723 |
| 0,30 | 1,025 |
| 0,40 | 1,435 |
| 0,50 | 1,756 |
| 0,000 | 0,850 |
Admitindo-se que a única espécie absorvente em 670 nm pós-tratamento advém apenas do sulfato de cobre formado e o “branco” tem valor igual à zero, o teor de cobre (%m/m) na amostra é de:
Provas
O ácido etilenodiamino tetra-acético (EDTA) é um composto orgânico que age como agente quelante, formando complexos com diversos íons metálicos. Observe a figura abaixo:
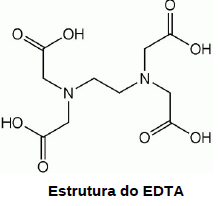
Sobre titulações complexométricas com esse composto, marque a opção CORRETA.
Provas
A glicose (C6H12O6), se presente na urina, pode ter sua concentração determinada pela medida da intensidade (I) da cor resultante da sua reação com um reagente específico, o ácido 3,5-dinitrossalicílico (DNS, amarelo), formando o ácido 3-amino-5-nitrosalicílico (DANS, vermelho), segundo o esquema abaixo:
!$ C_6 H_{12} O_6 + { \underset{amarelo} {DNS}} \rightarrow { \underset{vermelho} {DNS}} + açúcar\,oxidado !$
O gráfico, abaixo, ilustra a variação da intensidade da coloração vermelha de uma solução tratada com diferentes concentrações de glicose [ Cgli / (g/100 mL) ].
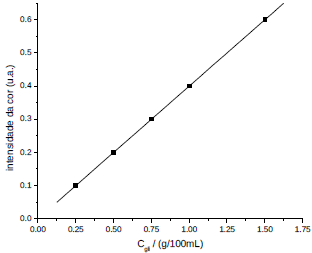
Com base nessas informações, a equação que melhor se ajusta aos pontos apresentados no gráfico é:
Provas
Caderno Container