Foram encontradas 13.430 questões.
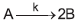 , é dada por !$ kC^n_A !$, onde !$ C_A !$ é a concentração do reagente A, n é a ordem da reação, e k é a sua velocidade específica.
, é dada por !$ kC^n_A !$, onde !$ C_A !$ é a concentração do reagente A, n é a ordem da reação, e k é a sua velocidade específica.Provas
Provas
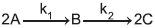 constante.
constante.Provas
Provas
Qual das misturas abaixo representa um exemplo de dispersão coloidal?
Provas
Ácido acético e acetato de sódio foram misturados de forma que a concentração de acetato fosse, no equilíbrio, duas vezes maior que a de ácido acético.
O pH dessa solução é:
Dado !$ CH_3 COOH_{(AQ)} \rightleftarrows CH_3 COO_{(aq)}^- + H_{(aq)}^+\,\, K_a=2,0x10^{-5} !$
Provas
Um mol de gás hidrogênio reage com um mol de gás cloro, em presença de luz, dando origem a dois mols de gás clorídrico.
H2(g) + C2(g) → 2 HC!$ \ell !$(g)
Admitindo-se comportamento de gases ideais, reação irreversível e rendimento de 100%, qual é o volume máximo de gás clorídrico, em L, que se obtém a partir da reação 20,0 L de gás hidrogênio com 20,0 L de gás cloro?
Provas
Soluções aquosas contendo os íons cloreto e iodeto podem ser obtidas pela solubilização completa dos sais KI e KC !$ \ell !$ em água ou pela preparação de soluções saturadas de AgI e AgC !$ \ell !$.
Sobre tais soluções, constata-se que
Dados
Kps AgC !$ \ell !$ = 1,8 x 10−10
Kps AgI = 1,0 x 10−18
Provas
Considere a seguinte reação de oxidação do monóxido de carbono:
!$ C_{(S)} + O_{2(g)} \rightleftarrows CO_{2(g)} !$
A equação que define a constante de equilíbrio dessa transformação química, em termos de concentração em quantidade de matéria (Kc) ou em termos de pressão parcial do gás (Kp), é
Provas
A obtenção de ácido sulfúrico passa, resumidamente, pelas seguintes reações: queima de enxofre, oxidação dos óxidos formados e reação com água, como indicado nas seguintes equações não balanceadas:
S(s) + O2(g) → SO(g)
SO(g) + O2(g) → SO2(g)
SO2(g) + O2(g) → SO3(g)
SO3(g) + H2O( !$ \ell !$) → H2SO4(aq)
A partir de 1.280g de S(s) qual a quantidade máxima, em g, de H2SO4 que se pode obter sabendo-se que o rendimento é de 90%?
Provas
Caderno Container