Foram encontradas 35.976 questões.
Em uma rotina de titulação ácido fraco × base forte (por exemplo, ácido acético padronizado com NaOH), o técnico analista precisa
escolher um indicador ácido–base adequado para leitura do ponto final. Sabe-se que, para esse sistema, o pH no ponto de equivalência é
maior que 7, e a curva apresenta uma região de variação abrupta de pH próxima ao equivalente.
Considerando o critério teórico de seleção de indicadores, assinale a alternativa CORRETA.
Considerando o critério teórico de seleção de indicadores, assinale a alternativa CORRETA.
Provas
Questão presente nas seguintes provas
Numa titulação ácido–base, a solução de concentração conhecida (o TITULANTE) é dispensada por um dispositivo graduado,
enquanto a amostra (o TITULADO) permanece em um recipiente adequado à reação, após ser medida em alíquota exata e transferida
para esse recipiente. Também é utilizado um acessório para carregar com segurança o dispositivo do titulante.
Associe os nomes dos itens do conjunto de titulação (Grupo I) às imagens correspondentes (Grupo II), considerando função e alocação de TITULANTE/TITULADO.
Grupo I - Itens do conjunto de titulação (Classe Aquando aplicável) I- Pipeta volumétrica - mede e transfere alíquota exata do TITULADO para o recipiente da reação.
II- Bureta - contém o TITULANTE e permite dispensa controlada com leitura de volume.
III- Erlenmeyer - recipiente do TITULADO onde ocorre a reação (com indicador/eletrodo).
IV- Funil de vidro (para bureta) - usado para carregar o TITULANTE no dispositivo; e ser retirada antes da leitura.
Grupo II - Vidrarias
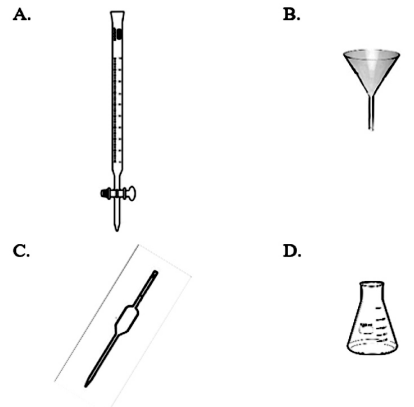
É CORRETA a associação apresentada em:
Associe os nomes dos itens do conjunto de titulação (Grupo I) às imagens correspondentes (Grupo II), considerando função e alocação de TITULANTE/TITULADO.
Grupo I - Itens do conjunto de titulação (Classe Aquando aplicável) I- Pipeta volumétrica - mede e transfere alíquota exata do TITULADO para o recipiente da reação.
II- Bureta - contém o TITULANTE e permite dispensa controlada com leitura de volume.
III- Erlenmeyer - recipiente do TITULADO onde ocorre a reação (com indicador/eletrodo).
IV- Funil de vidro (para bureta) - usado para carregar o TITULANTE no dispositivo; e ser retirada antes da leitura.
Grupo II - Vidrarias

É CORRETA a associação apresentada em:
Provas
Questão presente nas seguintes provas
Durante a rotina de um laboratório de análises de água, o técnico realiza a determinação da concentração de nitrato em amostras
coletadas de diferentes pontos de um reservatório. Para isso, utiliza o método espectrofotométrico, no qual ocorre a formação de um
composto colorido cuja intensidade é medida em um comprimento de onda específico.
Considerando os fundamentos e aplicações da espectrofotometria de absorção molecular, assinale a alternativa CORRETA.
Considerando os fundamentos e aplicações da espectrofotometria de absorção molecular, assinale a alternativa CORRETA.
Provas
Questão presente nas seguintes provas
Durante a reorganização do almoxarifado do Laboratório de Análise de Águas, a equipe decidiu segregar reagentes por classe de perigo
usando os pictogramas Globally Harmonized System of Classification and Labelling of Chemicals (GHS, Sistema Globalmente
Harmonizado de Classificação e Rotulagem de Produtos Químicos), conforme as Fichas de Informação de Segurança de Produtos
Químicos (FISPQ)/Safety Data Sheets (SDS).
Associe cada classe (Grupo 1) ao pictograma correspondente (Grupo 2).
Grupo 1 - Classes de perigo:
I- Inflamável II- Oxidante III- Corrosivo (a metais/pele/olhos) IV- Irritante/Nocivo (toxicidade aguda moderada, irritação)
Grupo 2 - Pictogramas GHS
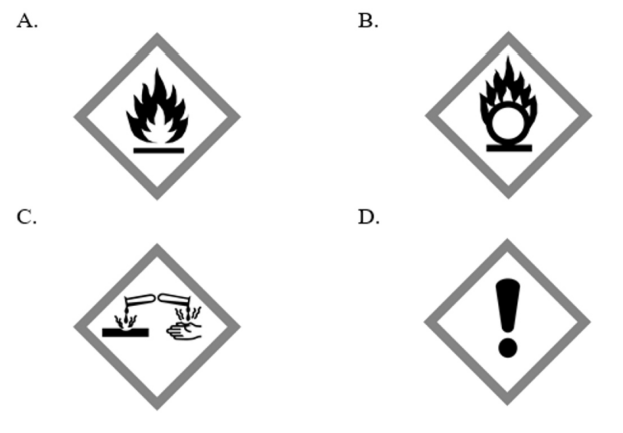
É CORRETA a sequência apresentada em:
Associe cada classe (Grupo 1) ao pictograma correspondente (Grupo 2).
Grupo 1 - Classes de perigo:
I- Inflamável II- Oxidante III- Corrosivo (a metais/pele/olhos) IV- Irritante/Nocivo (toxicidade aguda moderada, irritação)
Grupo 2 - Pictogramas GHS

É CORRETA a sequência apresentada em:
Provas
Questão presente nas seguintes provas
A qualidade da água está diretamente relacionada às suas propriedades físicas e químicas, que influenciam tanto o seu uso quanto os
processos de tratamento.
Sobre as características da água, analise as afirmativas a seguir e assinale a alternativa CORRETA.
Sobre as características da água, analise as afirmativas a seguir e assinale a alternativa CORRETA.
Provas
Questão presente nas seguintes provas
Um dos parâmetros organolépticos de qualidade da água de abastecimento público é o teor de cloretos (Cl-), com um limite permitido de 250 mg.L-1, conforme Portaria GM/MS Nº 888/2021 do Ministério da Saúde. Para a quantificação desse parâmetro, recomenda-se a utilização do método de Mohr, uma técnica de titulometria de precipitação. Nessa análise, em uma amostra contendo cloretos é
adicionada uma solução padrão de nitrato de prata (AgNO3), gradualmente mediante uma bureta, na presença de um indicador, o cromato de potássio (K2CrO4). Inicialmente, os íons Ag+ precipitam os íons Cl para formar o cloreto de prata (AgCl), um precipitado branco. Quando todos os íons Cl forem precipitados, os íons Ag+ irão precipitar os íons CrO42-, formando o cromato de prata (Ag2CrO4), um precipitado vermelho, que sinaliza o ponto final da titulação. O processo descrito acima, que permite a separação de compostos com solubilidades diferentes é chamado de:
Provas
Questão presente nas seguintes provas
O ácido acetilsalicílico – AAS (C9H8O4), popularmente comercializado com o nome Aspirina®, é um ácido monoprótico orgânico fraco, utilizado como medicamento para tratar dor, febre e inflamação, pelo efeito inibidor da enzima ciclo-oxigenase. Num copo de
200 mL, estão dissolvidos 1,8 g desse ácido, dos quais apenas 8,0% estão na forma ionizada (α). Nessas condições, qual o valor
aproximado da constante de ionização desse ácido (Ka),dado que massas molares em g.mol-1 (C = 12; O = 16; H =1)?
Provas
Questão presente nas seguintes provas
O tratamento de um determinado tipo de esgoto doméstico deve ser escolhido em função de suas características e da composição desse
efluente. Um dos parâmetros de maior interesse, nesse caso, é o teor de matéria orgânica presente na água residuária. Uma
possibilidade para se avaliar indiretamente a carga de matéria orgânica consiste em tratar a amostra com um excesso de oxidante forte
(dicromato de potássio), em meio fortemente ácido, sob aquecimento por um determinado intervalo. Após resfriamento, o excesso de
K2Cr2O7 é então titulado com sulfato ferroso amoniacal, e a quantidade de oxigênio necessária para estabilizar quimicamente a matéria orgânica é calculada estequiometricamente. Essa técnica é conhecida como:
Provas
Questão presente nas seguintes provas
O teor de ferro num comprimido de suplemento alimentar foi determinado por gravimetria. Para tanto, 1 comprimido pesando 0,6548 g
foi triturado até formar um pó finamente dividido. Em seguida, a amostra foi dissolvida e tratada com ácido nítrico e excesso de
hidróxido de amônio, para formar um precipitado de hidróxido de ferro III. Após filtração em papel de filtro quantitativo e calcinação a
900°C por 30 min, restou um resíduo de Fe2O3 pesando 0,0573 g. Dado: massas molares em g.mol-1 (Fe = 55,8; O = 16), qual a massa de ferro na amostra em mg?
Provas
Questão presente nas seguintes provas
O sal dissódico do ácido etilenodiaminotetracético Na2-EDTA (Na2H2C10H12O8N2) é amplamente utilizado na conservação de cosméticos e alimentos, em que atua como agente complexante. Também é muito útil na química analítica, sendo utilizado na
quantificação de íons metálicos por complexometria, em que forma um complexo estável com diversos íons na proporção de 1:1. Por
isso, é possível padronizar soluções de EDTA reagindo-o com soluções de carbonato de cálcio (CaCO3). Considere que a titulação de uma solução contendo 0,0330 g de carbonato de cálcio consumiu 16,5 mL de uma solução de EDTA. Dado: massas molares em g.mol-1
(Ca = 40; C = 12; O = 16), qual a concentração da solução de EDTA em mol.L-1?
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container