Foram encontradas 35.922 questões.
A estrutura geral de um aminoácido pode ser representada pela seguinte estrutura.
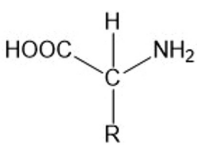
Observa-se que o carbono central está ligado a um grupo amino (–NH2), a um grupo carboxila (–COOH), a um átomo de hidrogênio e a uma cadeia lateral variável (R). Com base nessa estrutura, o caráter anfótero dos aminoácidos decorre do fato de que essas moléculas:

Observa-se que o carbono central está ligado a um grupo amino (–NH2), a um grupo carboxila (–COOH), a um átomo de hidrogênio e a uma cadeia lateral variável (R). Com base nessa estrutura, o caráter anfótero dos aminoácidos decorre do fato de que essas moléculas:
Provas
Questão presente nas seguintes provas
Uma amostra de gás ideal sofre uma transformação isobárica. Se a temperatura absoluta for duplicada, o volume do gás:
Provas
Questão presente nas seguintes provas
A finalidade do Teste de Baeyer é:
Provas
Questão presente nas seguintes provas
Em um laboratório de Química, um estudante realizou dois procedimentos distintos. No primeiro, ao misturar duas substâncias, observou-se aumento da temperatura do recipiente, mesmo sem aquecimento externo. No segundo procedimento, foi necessário fornecer calor ao sistema para que a transformação ocorresse. Com base nessas observações, os processos descritos são classificados, respectivamente, como:
Provas
Questão presente nas seguintes provas
A melatonina é um hormônio produzido pela glândula pineal
e está relacionada à regulação do ciclo sono-vigília. Analise a
estrutura molecular da melatonina a seguir:
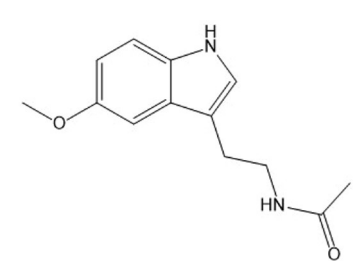
A função orgânica presente na molécula da melatonina é:

A função orgânica presente na molécula da melatonina é:
Provas
Questão presente nas seguintes provas
É um aspecto químico que justifica uma
armazenagem complexa de óleo diesel:
Provas
Questão presente nas seguintes provas
A espectroscopia no infravermelho é uma poderosa ferramenta para identificação de compostos, especialmente orgânicos.
A atribuição da presença de tipos de cadeias carbônicas e grupos funcionais é possível a partir do modelo de modos
vibracionais de simetria, uma vez que esses modos apresentam frequências e formatos de bandas típicos no espectro. A
seguir, é mostrado um espectro de infravermelho por transformada de Fourier (FTIR) de um composto orgânico.
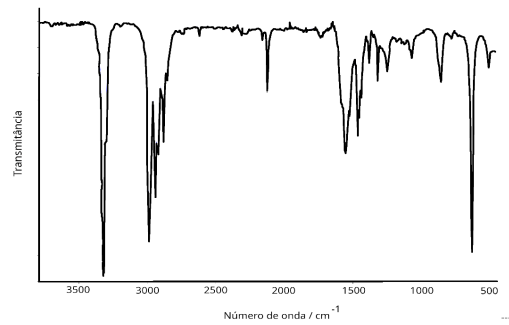
O espectro FTIR apresentado é atribuído a qual molécula orgânica?

O espectro FTIR apresentado é atribuído a qual molécula orgânica?
Provas
Questão presente nas seguintes provas
Quando o oxigênio líquido é derramado entre dois polos de um ímã, ele fica aprisionado, evidenciando o seu
paramagnetismo. A Teoria do Orbital Molecular (TOM) ganhou grande aceitação na ciência por explicar justamente
essa propriedade, o que a Teoria da Ligação de Valência (TLV) é incapaz de fazer, uma vez que, ao considerar a
estrutura de Lewis, coloca os elétrons emparelhados numa dupla ligação entre os dois átomos de oxigênio. Na TOM,
cada estado é descrito por um termo espectroscópico, que simplificadamente é um símbolo dado pela notação 2S+1Λ,
em que S é spin total e Λ é o momento angular orbital, atribuindo-se Σ, Π e Δ para momentos iguais a 0, 1 e 2,
respectivamente. O momento angular orbital de um elétron em um orbital molecular é dado por λ = |ml|, em que ml é o
número quântico magnético. Para o orbital σ, λ = 0 e para orbital π, λ = 1.
A molécula de oxigênio molecular no seu estado fundamental possuirá os elétrons de valência e termo espectroscópico, respectivamente, iguais a:
A molécula de oxigênio molecular no seu estado fundamental possuirá os elétrons de valência e termo espectroscópico, respectivamente, iguais a:
Provas
Questão presente nas seguintes provas
Compostos inter-halogênios são formados por dois ou mais átomos diferentes de elementos pertencentes ao
grupo XVII. Em sua maioria, esses compostos são binários, e suas fórmulas são geralmente XYn, em que n varia
de 1 a 7. O átomo Y é o mais eletronegativo e assume NOX −1. A ligação química pode ser descrita pela Teoria de
Ligação de Valência, e as geometrias podem ser previstas pelo modelo de Repulsão de Pares de Elétrons da Camada
de Valência (conhecida pela sigla em inglês VSEPR). O trifluoreto de cloro apresenta-se como um gás incolor com odor
irritante. Bastante reativo, é suscetível a hidrólise e, em contato com materiais orgânicos, pode resultar em ignição
espontânea. É corrosivo para metais e tecidos e, sob calor intenso, o recipiente pode romper-se violentamente e ser
projetado como um foguete.
Com base nas informações do texto, quais são a geometria molecular e a hibridação de orbitais atômicos do átomo central da molécula inter-halogênio mencionada?
Com base nas informações do texto, quais são a geometria molecular e a hibridação de orbitais atômicos do átomo central da molécula inter-halogênio mencionada?
Provas
Questão presente nas seguintes provas
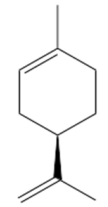
O limoneno, estrutura ilustrada a seguir, é o principal componente do óleo essencial das cascas de frutas cítricas e é utilizado como
fragrância na indústria alimentícia, solvente e precursor de outras moléculas. Ele possui um isômero, que tem propriedades
físicas – como temperatura de ebulição, densidade e índice de refração – idênticas à molécula ilustrada e que é comumente
associada em livros didáticos ao aroma de limão, enquanto a molécula desenhada seria responsável pelo aroma de tangerina. No
entanto, um artigo no Journal of Chemical Education de 2021 afirma que essa informação deriva da repetida citação de uma
publicação de 1971, que não se comprova experimentalmente.
Kvittingen, L. Sjursnes, B.J., Schmid, R. Limonene in Citrus: A String of Unchecked Literature Citings? J. Chem. Educ. 2021, 98, 11, 3600–3607. Disponível
em https://doi.org/10.1021/acs.jchemed.1c00363.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container