Foram encontradas 35.922 questões.
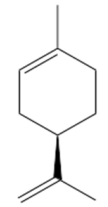
O limoneno, estrutura ilustrada a seguir, é o principal componente do óleo essencial das cascas de frutas cítricas e é utilizado como
fragrância na indústria alimentícia, solvente e precursor de outras moléculas. Ele possui um isômero, que tem propriedades
físicas – como temperatura de ebulição, densidade e índice de refração – idênticas à molécula ilustrada e que é comumente
associada em livros didáticos ao aroma de limão, enquanto a molécula desenhada seria responsável pelo aroma de tangerina. No
entanto, um artigo no Journal of Chemical Education de 2021 afirma que essa informação deriva da repetida citação de uma
publicação de 1971, que não se comprova experimentalmente.
Kvittingen, L. Sjursnes, B.J., Schmid, R. Limonene in Citrus: A String of Unchecked Literature Citings? J. Chem. Educ. 2021, 98, 11, 3600–3607. Disponível
em https://doi.org/10.1021/acs.jchemed.1c00363.
Provas
Questão presente nas seguintes provas
A alta demanda por cobre, impulsionada pela eletrificação de carros e intensa produção de componentes eletrônicos,
tem criado escassez do material e alta de preços. A obtenção de cobre metálico a partir de seu minério não requer
grande quantidade de energia e pode ser alcançada pela redução do seu óxido por monóxido de carbono. A redução
de óxido de cobre (II) passa pelo intermediário óxido de cobre (I) até chegar a cobre metálico. Considere as seguintes
equações químicas e correspondentes entalpias de reação:
2 Cu + ½ O2 → Cu2O ΔH = −170 kJ Cu2O + ½ O2 → 2 CuO ΔH = 16 kJ CO + ½ O2 → CO2 ΔH = −283 kJ
Utilizando monóxido de carbono como redutor, qual é o valor de entalpia mais próximo para a redução de 1 mol de óxido de cobre (II) a cobre?
2 Cu + ½ O2 → Cu2O ΔH = −170 kJ Cu2O + ½ O2 → 2 CuO ΔH = 16 kJ CO + ½ O2 → CO2 ΔH = −283 kJ
Utilizando monóxido de carbono como redutor, qual é o valor de entalpia mais próximo para a redução de 1 mol de óxido de cobre (II) a cobre?
Provas
Questão presente nas seguintes provas
A manutenção de aquários e lagos ornamentais requer cuidados com a qualidade da água. Para o uso de água da rede
de saneamento, muitas vezes é necessária a remoção de cloro e cloraminas, que podem levar à morte de peixes e
outros animais, ou mesmo prejudicar o desenvolvimento da biota. Essa remoção pode ser realizada com o uso de
condicionadores baseados em tiossulfato de sódio (Na2S2O3), que reage de forma espontânea com cloro e cloroaminas
para gerar espécies químicas inofensivas. No caso da reação com cloroaminas, esses condicionadores possuem
também aditivos que neutralizam a amônia produzida na reação. Considere a remoção de cloro de uma amostra e os
diagramas de Latimer a seguir.
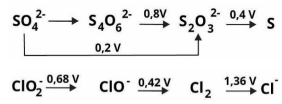
A reação, que provoca o condicionamento da água da rede de saneamento própria para uso, possui a diferença de potencial padrão de:

A reação, que provoca o condicionamento da água da rede de saneamento própria para uso, possui a diferença de potencial padrão de:
Provas
Questão presente nas seguintes provas
O éster diisononílico do ácido 1,2-ciclohexanodicarboxílico (DINC) é um importante plastificante não baseado em ftalatos, usado na
fabricação de artigos de plástico flexíveis em áreas de aplicação sensíveis, como brinquedos, dispositivos médicos e embalagens
de alimentos. Esse composto pode ser obtido por uma sequência de reações, que parte do ácido fumárico (ácido 2-butenodióico,
M = 116 g mol–1) para formar um derivado do ciclohexeno na etapa I, cujo rendimento é de 80%, seguida de hidrogenação obtida de
forma quantitativa e, por fim, esterificação com 1-nonanol (M = 144 g mol–1), com rendimento de 90%, conforme mostrado no
esquema a seguir.
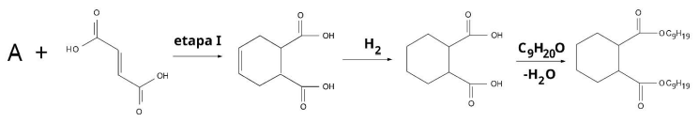
Dados: Massa molar (g mol–1): C = 12, O = 16, H = 1.
Provas
Questão presente nas seguintes provas
O éster diisononílico do ácido 1,2-ciclohexanodicarboxílico (DINC) é um importante plastificante não baseado em ftalatos, usado na
fabricação de artigos de plástico flexíveis em áreas de aplicação sensíveis, como brinquedos, dispositivos médicos e embalagens
de alimentos. Esse composto pode ser obtido por uma sequência de reações, que parte do ácido fumárico (ácido 2-butenodióico,
M = 116 g mol–1) para formar um derivado do ciclohexeno na etapa I, cujo rendimento é de 80%, seguida de hidrogenação obtida de
forma quantitativa e, por fim, esterificação com 1-nonanol (M = 144 g mol–1), com rendimento de 90%, conforme mostrado no
esquema a seguir.

Dados: Massa molar (g mol–1): C = 12, O = 16, H = 1.
Provas
Questão presente nas seguintes provas
O eletrodo de referência prata-cloreto de prata é amplamente usado em medidas eletroquímicas, por exemplo, em
sistemas de controle de corrosão por proteção catódica em ambientes costeiros, e é uma alternativa aos eletrodos de
calomelano, que têm riscos ambientais. Ele consiste em um fio de prata recoberto por uma fina camada de cloreto de
prata mergulhado numa solução eletrolítica. Para que o potencial de eletrodo não varie, a concentração de íons prata
deve ser constante. Considere que um fio é recoberto por uma camada de 1,0 mg de cloreto de prata e está imerso
em 0,1 mL de uma solução 3 mol L–1 de cloreto de sódio.
Dados: Massas molares (g mol–1): Ag = 107; Cl = 35,5. KPS (AgCl) = 1,8 x 10–10.
Na situação descrita, a concentração de prata, em mol L–1, na solução é de:
Dados: Massas molares (g mol–1): Ag = 107; Cl = 35,5. KPS (AgCl) = 1,8 x 10–10.
Na situação descrita, a concentração de prata, em mol L–1, na solução é de:
Provas
Questão presente nas seguintes provas
Em 1999, o Laboratório Nacional Lawrence Berkeley (EUA) anunciou a descoberta dos elementos superpesados de
números atômicos 116 e 118. Porém, mais tarde, descobriu-se que as evidências haviam sido forjadas por um de seus
cientistas, e o trabalho científico teve que ser retratado. Um ano depois, pesquisadores do Centro Conjunto
Internacional de Pesquisa Nuclear, na Rússia, liderados por Yuri Oganessian, em parceria com Laboratório Nacional
Lawrence Livermore nos EUA, descobriram esses dois novos elementos, os quais foram nomeados livermório (116Lv)
e oganésson (118Og), em homenagem ao laboratório e ao pesquisador líder, respectivamente. Og é atualmente o último
elemento da tabela periódica. Ambos os elementos superpesados foram sintetizados por meio do bombardeamento
de elementos actinídeos (An) por íons do isótopo Ca-48, conforme esquemas I e II. O Og também decai radioativamente
e produz Lv, como mostrado no esquema III.
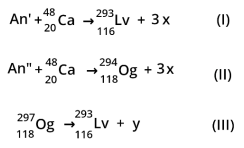
Nos esquemas, os actinídeos An’ e An” e as partículas x e y são, respectivamente:
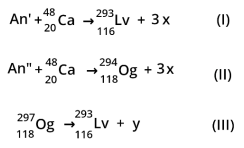
Nos esquemas, os actinídeos An’ e An” e as partículas x e y são, respectivamente:
Provas
Questão presente nas seguintes provas
Em 2025 houve um aumento muito grande de casos de intoxicação por metanol, especialmente no estado de São Paulo.
Os sintomas da intoxicação aparecem em até 12 horas, e a substância age na medula e no cérebro, causando confusão
mental, lesão no nervo óptico, acidose no sangue e respiratória. Com a ingestão do metanol, em vez de metabolizá-lo
em substâncias facilmente processadas, o fígado o converte em compostos ainda mais perigosos, capazes de
provocar cegueira e de levar à morte, como o formaldeído e o ácido fórmico.
A qual classe pertence a reação mencionada no texto, que converte o metanol em compostos mais perigosos?
A qual classe pertence a reação mencionada no texto, que converte o metanol em compostos mais perigosos?
Provas
Questão presente nas seguintes provas
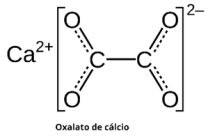
Além de alcaloides, muitas plantas são tóxicas por conter oxalato de cálcio (M = 128 g mol–1). As beladonas e a
comigo-ninguém-pode são altamente tóxicas devido à presença desse composto na forma cristalina de ráfides (agulhas), que são
perfurantes. Quando em contato com a pele e/ou mucosas, podem causar lesões e, em casos mais sérios, asfixia, podendo levar a
óbito devido à obstrução das vias aéreas. No entanto, outras folhas, como espinafre, são ricas em oxalato, mas nesse caso o
composto se encontra na forma cristalina de drusas e prismas pequenos, que não são tóxicos.
5 C2O4 2−(aq) + 2 MnO4 −(aq) + 16 H+(aq) → 10 CO2(g) + 2 Mn2+(aq) + 8H2O(l)
Considerando os dados descritos da análise, a quantidade de oxalato, em miligramas, por 100 g de folha seca, é mais próxima de:
Provas
Questão presente nas seguintes provas
Além de alcaloides, muitas plantas são tóxicas por conter oxalato de cálcio (M = 128 g mol–1). As beladonas e a
comigo-ninguém-pode são altamente tóxicas devido à presença desse composto na forma cristalina de ráfides (agulhas), que são
perfurantes. Quando em contato com a pele e/ou mucosas, podem causar lesões e, em casos mais sérios, asfixia, podendo levar a
óbito devido à obstrução das vias aéreas. No entanto, outras folhas, como espinafre, são ricas em oxalato, mas nesse caso o
composto se encontra na forma cristalina de drusas e prismas pequenos, que não são tóxicos.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container