Foram encontradas 36.174 questões.
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Leia o texto para responder às questões de 32 a 34. Ao ser contratado, o técnico observou que foram acumulados, no laboratório, vários frascos com resíduos químicos que devem ser tratados e/ou encaminhados para descarte correto. Consultando uma central de resíduos já estabelecida, ele encontrou algumas informações que poderiam auxiliar nesse processo. Por exemplo, soluções aquosas de sais inorgânicos de metais alcalinos e alcalinos terrosos: NaCl, KCl, CaCl2, MgCl2, Na2SO4, MgSO4 e tampões PO43-, não contaminados com outros produtos, devem ser diluídos e descartados diretamente na rede de esgoto. Soluções de ácidos ou bases inorgânicas: H2SO4, HCl, H3PO4, HNO3, KOH, NaOH, Na2CO3, K2CO3, NaHCO3, KHCO3. devem ser diluídas e neutralizadas, podendo, então, serem desprezadas na rede de esgoto, desde que não contaminadas com outros produtos.
A primeira etapa foi a identificação dos frascos buscando segregar os resíduos que são passíveis de destruição /neutralização no próprio laboratório, para posterior descarte na pia. Três frascos foram separados, pois se enquadravam nessa situação. Eles estavam classificados como descrito abaixo:
| Frasco | Quantidade | Composição sugerida |
|---|---|---|
| 1 | 9,6L | Resíduo da reação de H2SO412 mol L-1 com Magnésio metálico e água de lavagem. |
| 2 | 12,4L | Solução de Bicarbonato de sódio (NaHCO3) e Ácido clorídrico (HCl). |
| 3 | 11,2L | Resíduo de KOH 6 mol L-1 com água de lavagem. |
Prezando pela segurança, este técnico buscou confirmar o máximo de informações apresentadas nesses rótulos, antes de proceder a qualquer tratamento. Assim, ele realizou alguns ensaios com amostras dos resíduos de forma a verificar aspecto físico, coloração, presença de precipitados, pH e ainda testes qualitativos para íons.
Disponível em: <https://www.sgas.ufscar.br/degr/residuos/residuos-quimicos/tratamento-no-laboratorio> (Com adaptações). Acesso em: 17. Abr. 2024.
O técnico separou 200 ml de cada frasco para analisar. Após análise, o frasco 3 indicou uma concentração de 4,3mol L-1 de KOH e a ausência de contaminantes, podendo apenas neutralizar e descartar a solução na pia. Dentre as opções disponíveis e menos dispendiosas, o técnico optou por um resíduo de HCl 1,5 mol L-1 que tinha sido gerado e que também precisava ser descartado.
Considerando os volumes e as concentrações apresentados, qual alternativa apresenta o volume mais próximo do necessário para neutralizar totalmente os 11 litros restantes da solução de KOH?
Provas
Leia o texto para responder às questões de 32 a 34. Ao ser contratado, o técnico observou que foram acumulados, no laboratório, vários frascos com resíduos químicos que devem ser tratados e/ou encaminhados para descarte correto. Consultando uma central de resíduos já estabelecida, ele encontrou algumas informações que poderiam auxiliar nesse processo. Por exemplo, soluções aquosas de sais inorgânicos de metais alcalinos e alcalinos terrosos: NaCl, KCl, CaCl2, MgCl2, Na2SO4, MgSO4 e tampões PO43-, não contaminados com outros produtos, devem ser diluídos e descartados diretamente na rede de esgoto. Soluções de ácidos ou bases inorgânicas: H2SO4, HCl, H3PO4, HNO3, KOH, NaOH, Na2CO3, K2CO3, NaHCO3, KHCO3. devem ser diluídas e neutralizadas, podendo, então, serem desprezadas na rede de esgoto, desde que não contaminadas com outros produtos.
A primeira etapa foi a identificação dos frascos buscando segregar os resíduos que são passíveis de destruição /neutralização no próprio laboratório, para posterior descarte na pia. Três frascos foram separados, pois se enquadravam nessa situação. Eles estavam classificados como descrito abaixo:
| Frasco | Quantidade | Composição sugerida |
|---|---|---|
| 1 | 9,6L | Resíduo da reação de H2SO412 mol L-1 com Magnésio metálico e água de lavagem. |
| 2 | 12,4L | Solução de Bicarbonato de sódio (NaHCO3) e Ácido clorídrico (HCl). |
| 3 | 11,2L | Resíduo de KOH 6 mol L-1 com água de lavagem. |
Prezando pela segurança, este técnico buscou confirmar o máximo de informações apresentadas nesses rótulos, antes de proceder a qualquer tratamento. Assim, ele realizou alguns ensaios com amostras dos resíduos de forma a verificar aspecto físico, coloração, presença de precipitados, pH e ainda testes qualitativos para íons.
Disponível em: <https://www.sgas.ufscar.br/degr/residuos/residuos-quimicos/tratamento-no-laboratorio> (Com adaptações). Acesso em: 17. Abr. 2024.
Uma das propriedades relevantes dessas soluções que deve ser confirmada é o pH, que indicaria se a solução é ácida, neutra ou básica, como se espera para os frascos 1, 2 e 3, respectivamente. Essa medida de acidez e basicidade pode ser feita, qualitativa ou quantitativamente, no laboratório de Química usando diferentes equipamentos, vidrarias e/ou reagentes.
Das alternativas abaixo, qual apresenta as três possibilidades adequadas para estimar o pH das soluções?
Provas
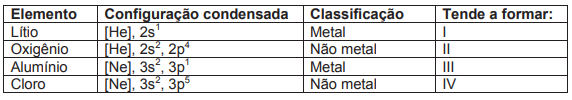
Os estudos em mecânica quântica possibilitaram a organização dos elétrons em orbitais, permitindo conhecer a configuração eletrônica de cada elemento químico representado na tabela periódica. Uma das aplicações dessa configuração é conhecer o número de elétrons na camada de valência, e, com isso, prever o número de elétrons envolvidos e/ou o tipo de ligação química que esse elemento tende a fazer.
Dessa forma, considerando os elementos abaixo, assinale a alternativa que apresente, em I, II, III e IV, os íons que cada elemento tende a formar.
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Uma das teorias ácido-base mais conhecidas refere-se aos conceitos de Bronsted-Lowry, em que ácido é definido como doador de prótons H+, ao passo que as bases são as receptoras de prótons, independente de possuir ou não íons hidroxila. Assim, uma reação ácido-base é uma reação em que há a transferência de um próton de uma espécie a outra, gerando, portanto, duas novas substâncias com caráter ácido e básico, que chamamos de par ácido-base conjugado.
Dessa forma, na equação representada abaixo:
HNO3(aq)+HPO42-(aq) NO–(aq)+H2PO4–(aq)
qual é o ácido conjugado e a base conjugada, respectivamente?
Provas
Um dos tipos de extintores existentes é de CO2, preenchido por esse gás pressurizado. De forma simplificada, ele age diminuindo a concentração de oxigênio e assim extinguindo a chama, além de contribuir para o abaixamento da temperatura pela expansão do gás. Por conta disso, o manuseio desse extintor desse ser feito com cautela, pois esse gás atinge baixas temperaturas ao ser liberado.
Se um extintor operasse com as condições fictícias a seguir: 2kg de CO2, com um volume de gás pressurizado de 2,5L, operando a uma pressão de 27 MPa, qual temperatura em graus Celsius, o gás deve atingir ao ser liberado?
Disponível em: <https://www.extintoresporto.pt/conheca-o-extintor-co2-e-para-que-serve#:~:text=O%20difusor%20tem%20uma%20dupla,segura%20direcionada%20para%20as%20chamas.&text=No%20extintor%20de%20CO2%2C%20existe,do%20volume%20interno%20do%20recipiente>. (Com adaptações).
Acesso em: 17 abr. 2024.
Considere que o gás se comporta como um gás ideal; utilize R = 8,3 cm3 MPa K−1 mol−1; considere a relação Temp (K) = Temp (°C) + 273.
Provas
Um técnico do laboratório de Química encontrou um frasco sem rótulo com um metal desconhecido. Para descobrir que metal era esse, ele reagiu o mesmo com ácido clorídrico, obtendo a formação do gás hidrogênio, segundo a equação: M(s)+xHCl(aq)→MClx(aq)+H2(g)
Assim, ele montou um sistema para coletar o gás formado e utilizou um pedaço de metal de 0,09 g na reação; a temperatura ambiente era de 22ºC e a pressão atmosférica na cidade era de 0,91 atm. O técnico recolheu, no sistema montado, 36,5mL de gás hidrogênio.
Utilizando a equação dos gases ideais (p.V=n.R.T) e a fórmula da massa molar (MM=m/n), responda que metal deve ser esse.
Dados: T(K) = T(°C) +273. Constante dos gases (R) = 0,0821 L atm Mol-1 K-1 ou 8,206 x 10−5 m3 atm K−1 mol−1 ou 8,314 cm3 MPa K−1 mol−1 ou 8,314 L kPa K−1 mol−1.
Provas
Uma das atividades comuns no laboratório de Química da UNIFAL-MG refere-se ao preparo dos resíduos que são encaminhados para a correta destinação. Essa atividade é necessária, pois, muitas vezes, os alunos descartam, incorretamente, as substâncias usadas em aula, produzindo misturas que devem ser separadas antes da destinação final. Considerando que, no final da aula, os alunos descartaram tetracloreto de carbono (CCl4) junto às soluções aquosas, o técnico optou por separar a mistura por decantação.
Essa técnica é possível de ser usada graças à diferença de qual propriedade entre as substâncias?
Provas
Mercúrio (e seus compostos) é um tipo de contaminante que, em hipótese alguma, pode ser descartado na rede de esgoto, dado seu potencial tóxico e cumulativo. Contudo, sem ter como recuperar esse metal de um galão com 5 litros de resíduo de sais de mercúrio (I), o técnico do laboratório de Química Geral optou por reduzir o volume para encaminhar uma quantidade menor ao descarte. Para evitar riscos ou gasto de energia, ele optou pela técnica de precipitação. Consultando a tabela disponível nos manuais e na internet, ele encontrou as seguintes opções para a constante de produto de solubilidade (Kps) dos sais de mercúrio:
| Fórmula do sal que será formado | Kps |
|---|---|
| Hg2Cl2 | 1,5x10-18 |
| HgI2 | 2,8x10-19 |
| Hg2(SCN)2 | 3,1x10-20 |
| Hg2Br2 | 6,4x10-23 |
| Hg(OH)2 | 3,1x10-26 |
| Hg2I2 | 5,3x10-29 |
| HgS | 1,6×10-54 |
Com base na tabela, qual contra-íon o técnico deve usar para que a precipitação do resíduo que ele possui seja máxima?
Provas
Sobre ligações covalentes, é correto afirmar que:
Provas
Leia o texto a seguir para responder às questões de 21 a 23.
Alfenas está situada no Sul de Minas, às margens do Lago de Furnas, um dos maiores lagos artificiais do Brasil. Embora o objetivo inicial da construção desse lago tenha sido a geração de energia a partir da construção de uma usina hidrelétrica, ao longo destes 60 anos as atividades turísticas e recreativas se intensificaram nessa região e não é mais possível imaginá-la sem visitantes. Contudo, recentemente uma reportagem trouxe uma preocupação para a região. Um estudo da UFMG indicou que atividades humanas como a agricultura, pecuária e lançamento do esgoto in natura podem ter afetado a qualidade da água do Lago de Furnas. Em suas análises, a pesquisadora considerou dados oficiais de monitoramento das águas em Minas Gerais relativos às bacias que alimentam o Lago de Furnas, considerando os parâmetros de turbidez, pH, densidade de cianobactérias e os níveis de E. coli.
Quando nos referimos a contaminantes inorgânicos, como cromo, mercúrio, chumbo ou cadmio, a presença destes em fontes hídricas ou até mesmo nos peixes que ocupam essas fontes é comum, dadas as atividades cotidianas ou industriais que ocorrem nos municípios ao redor. E outra atividade frequente na região de Furnas refere-se à pesca esportiva ou como fonte de renda, com criação especialmente de tilápias em tanques. Embora não tenha sido apontado no estudo, o monitoramento constante dos níveis de contaminantes, sobretudo os inorgânicos, nas águas do lago, é crucial para garantir a qualidade do peixe que chega à mesa dos mineiros e seus visitantes.
Disponível em: <https://ufmg.br/comunicacao/noticias/presenca-de-contaminantes-fecais-no-lago-de-furnas-pode-estar-acima-do-permitido> (Com adaptações). Acesso em: 17 abr. 2024.
No estudo realizado na UFMG, é mencionado que uma das análises feitas foi do pH das amostras de água do lago. O pH é uma escala bastante útil em Química já que a concentração dos íons hidrônio [H3O+] pode variar em várias ordens de grandezas. Assim, evitando uma faixa extensa de valores, o pH é expresso em termos do logaritmo negativo (na base 10) da concentração dos íons hidrônio, em mol por litro, ou seja, pH = - log [H3O+]. Contudo, essa definição é uma simplificação que se aplica às soluções suficientemente diluídas, já que o pH dessas soluções é medido orginalmente com base na ___________ dos íons H3O+.
Assinale a alternativa que completa corretamente a lacuna do texto:
Provas
Caderno Container