Foram encontradas 36.174 questões.
Os métodos de análise térmica medem as variações
que ocorrem em função da temperatura ou em função do
tempo em uma determinada temperatura constante. Estes
métodos vêm sendo amplamente utilizados em processos
de caracterização. A termogravimetria avalia a variação de
massa em função do tempo. Com relação ao calorímetro
de varredura diferencial (DSC), é INCORRETO afirmar que:
Provas
Questão presente nas seguintes provas
O método Karl Fischer é muito utilizado e foi desenvolvido pelo alemão que dá nome à metodologia. O método
é usado para quantificar:
Provas
Questão presente nas seguintes provas
A Cromatografia de Camada Delgada (CCD) é uma
técnica de cromatografia usada para separar substâncias
químicas de uma mistura em compostos individuais. Com
relação a esta técnica podemos afirmar que:
Provas
Questão presente nas seguintes provas
As técnicas espectrofotométricas são fundamentadas
na absorção da energia eletromagnética por moléculas, o
que depende tanto da concentração quanto de suas estruturas químicas. Sobre a espectrofotometria de absorção no
Ultravioleta-visível (UV-Vis), avalie se são verdadeiras ou
falsas as afirmativas a seguir:
I. Os elétrons passam de um estado de maior energia para um de menor energia.
II. Ao selecionar o tipo de solvente para dissolver a amostra é preciso levar em consideração o Cut-Off do mesmo.
III. A conjugação de dois cromóforos resulta em um efeito hipsocrômico.
IV. Auxocrômo é um grupo funcional que não absorve na região ultravioleta, logo não interferindo na intensidade de absorção da molécula a que está ligado.
As afirmativas I, II, III e IV são respectivamente:
I. Os elétrons passam de um estado de maior energia para um de menor energia.
II. Ao selecionar o tipo de solvente para dissolver a amostra é preciso levar em consideração o Cut-Off do mesmo.
III. A conjugação de dois cromóforos resulta em um efeito hipsocrômico.
IV. Auxocrômo é um grupo funcional que não absorve na região ultravioleta, logo não interferindo na intensidade de absorção da molécula a que está ligado.
As afirmativas I, II, III e IV são respectivamente:
Provas
Questão presente nas seguintes provas
“Para obter resultados quantitativamente significativos
sem as substâncias padrão dos analitos identificados, uma
série de estratégias diferentes vem sendo desenvolvidas
em análises não-direcionadas por cromatografia líquida
acoplada à espectrometria de massas de alta resolução
(LC-HRMS).” (KRUVE, A. Anal. Chem. 2020;92:4691-4699)
Segundo Kruve (2020), algumas das abordagens mais empregadas são as abaixo relacionadas, EXCETO:
Segundo Kruve (2020), algumas das abordagens mais empregadas são as abaixo relacionadas, EXCETO:
Provas
Questão presente nas seguintes provas
A cromatografia a líquido acoplada à espectrometria
de massas de alta resolução em instrumento híbrido com
analisadores de massa quadrupolo e por tempo de voo
(LC-Q-TOF HRMS) foi utilizada por Chakkar et al (2024)
para a identificação e a caracterização de produtos de
degradação do enasidenib (ver fi gura abaixo), Ingrediente
Farmacêutico Ativo (IFA) de um medicamento aprovado
em 2017 pela Agência Americana para Medicamentos e
Alimentos (U.S. Food and Drug Administration, FDA), para
terapia dirigida em pacientes com leucemia mieloide aguda
recidivante ou refratária. Além disso, a avaliação de risco
de N-nitrosaminas, prováveis agentes carcinógenos para
humanos, segundo a Agência Internacional de Pesquisa
sobre o Câncer (IARC), foi realizada usando um ensaio
de nitrosação modificado (NAP). (CHAKKAR et al. Rapid
Commun. Mass Spectrom. 2024;38:e9696)
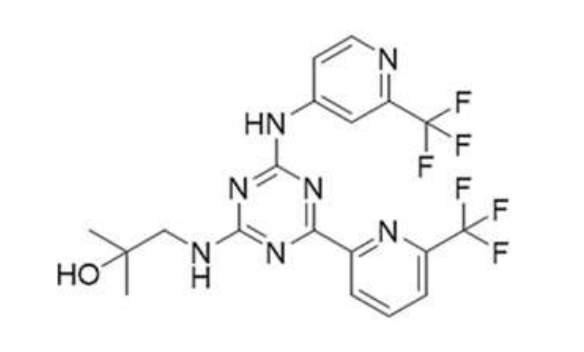
Fórmula estrutural do enasidenib. Fonte: Chakkar et al. Rapid Commun. Mass Spectrom. 2024;38:e9696.
Com base na estrutura apresentada e nas massas atômicas dos isótopos mais abundantes C=12,00000 u, N=14,00307 u, O=15,99491 u, H=1,007825 u, F=18,99840 u, Na=22,98977 u e K=38,96371 u, é INCORRETO afirmar que:

Fórmula estrutural do enasidenib. Fonte: Chakkar et al. Rapid Commun. Mass Spectrom. 2024;38:e9696.
Com base na estrutura apresentada e nas massas atômicas dos isótopos mais abundantes C=12,00000 u, N=14,00307 u, O=15,99491 u, H=1,007825 u, F=18,99840 u, Na=22,98977 u e K=38,96371 u, é INCORRETO afirmar que:
Provas
Questão presente nas seguintes provas
O ácido de Arrhenius é toda substância que em
solução aquosa libera H+
. Embora esta seja a definição
clássica dos livros didáticos do ensino médio no Brasil,
ao nos debruçarmos sobre a obra de Arrhenius, nenhuma
definição de ácido é oferecida. No entanto, a partir dos
seus estudos de eletrólise é possível se inferir uma
definição de ácido como toda substância que em solução
aquosa produz H+
. A partir destas considerações e das
equações abaixo, avalie as afirmativas I a V abaixo:

I. somente o HCl é um ácido de Arrhenius dentre os compostos HCl, NH4Cl e Al2(SO4)3.
II. Al2(SO4)3 e NH4Cl não são ácidos de Arrhenius.
III. HCl e NH4Cl são ácidos de Arrhenius porque possuem H na fórmula, podendo liberar ou produzir H+ em solução aquosa.
IV. Os três compostos envolvidos nas reações - HCl, NH4Cl e Al2(SO4)3 - são ácidos de Arrhenius.
V. O conceito de acidez e basicidade, além de sua importância organizacional na história da química, é um conceito relacional e, portanto, não deve ser determinado apenas pela classificação das substâncias em termos de funções (ácido, base, sal e óxido).
Das afirmativas acima, apenas:

I. somente o HCl é um ácido de Arrhenius dentre os compostos HCl, NH4Cl e Al2(SO4)3.
II. Al2(SO4)3 e NH4Cl não são ácidos de Arrhenius.
III. HCl e NH4Cl são ácidos de Arrhenius porque possuem H na fórmula, podendo liberar ou produzir H+ em solução aquosa.
IV. Os três compostos envolvidos nas reações - HCl, NH4Cl e Al2(SO4)3 - são ácidos de Arrhenius.
V. O conceito de acidez e basicidade, além de sua importância organizacional na história da química, é um conceito relacional e, portanto, não deve ser determinado apenas pela classificação das substâncias em termos de funções (ácido, base, sal e óxido).
Das afirmativas acima, apenas:
Provas
Questão presente nas seguintes provas
Considerando que o a substância X possui massa molar
de 90g, a molaridade de uma solução contendo 22,5g da
substância X e cujo volume é 250mL é de:
Provas
Questão presente nas seguintes provas
O suco gástrico em nosso estômago é composto principalmente por ácido clorídrico (HCl). Determinados alimentos, algumas doenças ou até mesmo tensão nervosa, podem aumentar a quantidade de HCl no estômago e causar sensação de ardência. O hidróxido de magnésio é uma base fraca que, quando entra em contato com o suco gástrico, leva a uma reação que neutraliza o meio. A massa, em gramas, de hidróxido de magnésio necessária para neutralizar o ácido clorídrico (HCl) contido em 150 mL de suco gástrico com concentração de HCl de 0,1 mol/L é:
Dado: massa molecular Mg(OH)2 = 58,3 g/mol.
Provas
Questão presente nas seguintes provas
Para que exista a ação do fogo é necessário que
tenha a presença de combustível em sua
composição e identifica-lo irá definir qual será a
melhor maneira de iniciar o combate ao incêndio.
Assinale a alternativa que descreve um material
que pode ser considerado como combustível
sólido para o fogo:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container