Foram encontradas 36.242 questões.
Óxido de ferro II pode ser reduzido a ferro, tanto por carbono, como por monóxido de carbono, de acordo com o mostrado nas equações
1 e 2: 1. FeO(s) + C(s) −−→ Fe(s) + CO(g)
2. FeO(s) + CO(g) −−→ Fe(s) + CO2(g)
Os valores de entalpia de formação e de entropia-padrão das substâncias envolvidas em ambas reações são apresentados na tabela:
| FeO(s) | Fe(s) | C(s) | CO(g) | CO2(g) |
|
| \( \Delta H^o_f \) (kJ.mol−1) |
−271,9 | 0 | 0 | -110,5 | -393,5 |
| Sº (J.K−1.mol−1) |
60,8 | 27,3 | 5,7 | 197,9 | 213,7 |
Considere um meio reacional fechado onde ocorrem as duas reações e que os valores acima permanecem constantes na faixa de 298 a 650 K. A ÚNICA alternativa correta é:
Provas
Analise as afirmativas abaixo.
I. A imersão de limalha de ferro em um béquer aberto contendo uma solução de ácido clorídrico provoca a liberação de bolhas de gás. Nesse processo, não há realização nem recebimento de trabalho.
II. Uma solução de ácido iodídrico de concentração igual a 1,0 \( \times \) 10−8 mol.L−1 tem pH igual a 8.
III. Se dois béqueres, um contendo água pura e o outro contendo uma solução insaturada de sacarose, forem submetidos ao aquecimento, a solução de sacarose ebulirá a uma temperatura constante e superior à temperatura de ebulição da água pura.
IV. Para a reação de combustão completa do gás metano, gerando apenas produtos gasosos, as variações de entalpia e de energia interna têm o mesmo valor.
A única alternativa CORRETA é:
Provas
Em todos os seres vivos, as proteínas são um importante grupo de substâncias. Sobre a estrutura das proteínas, analise as afirmativas abaixo.
I. A estrutura primária de uma proteína é a sequência de alfa-aminoácidos, tais como glicina, alanina e citosina, ligados por ligações peptídicas.
II. A estrutura secundária é mantida por ligações de hidrogênio entre os grupos −NH e C−− O, próximos entre si, na disposição espacial da proteína.
III. A estrutura terciária é estabilizada por interações hidrofóbicas, hidrofílicas, iônicas e ligações dissulfeto.
IV. A estrutura quaternária refere-se ao arranjo de múltiplas subunidades polipeptídicas que podem, por ação de agentes químicos ou físicos, ser alteradas ou destruídas através do fenômeno conhecido como desnaturação proteica, perdendo sua atividade biológica.
V. As proteínas apresentam estruturas geométricas de vários tipos e podem ser caracterizadas pela produção de colorações, como por exemplo, a reação da proteína da pele com ácido nítrico, formando uma coloração azulada.
A opção que apresenta APENAS afirmativas verdadeiras é:
Provas
Uma solução foi preparada com 1800 g de ácido sulfúrico puro e 2000 L de água deionizada, sendo, em seguida, eletrolisada. Uma amostra de 100 mL da solução resultante foi titulada com soluçãopadrão 0,1 M de hidróxido de sódio, tendo sido necessários 20,4 mL dessa solução para neutralizar a amostra. Considere que a massa específica do ácido sulfúrico vale 1800 g.L−1 e que misturas desse ácido em água se comportam idealmente no que se refere ao volume de mistura.
A alternativa que contém o volume aproximado de gás gerado na eletrólise, em m3, medido nas CNTP, é:
Provas
A figura a seguir mostra esquematicamente um dispositivo eletroquímico composto pelas meiascélulas X e Y.
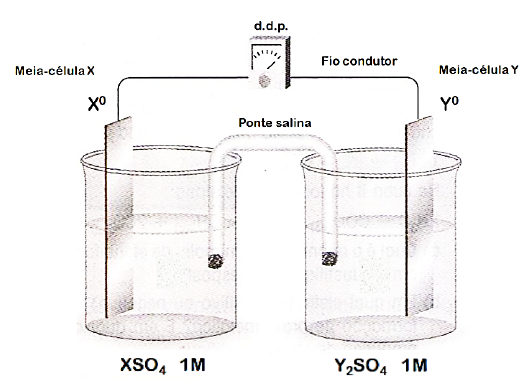
Dados: Potenciais-padrão de redução das espécies químicas envolvidas.
| \( E^o_X = -1,85V \) | \( E^o_Y = -2,93V \) |
Com base no esquema eletroquímico apresentado na figura e nos dados fornecidos, analise as proposições a seguir na condição do circuito fechado.
I. A semirreação representada pela equação estequiométrica \( X^0 \rightarrow X^{+2} + 2 e^- \) é espontânea por ser de oxidação.
II. O fluxo de elétrons ocorre no sentido horário, indo do anodo para catodo.
III. A corrente iônica circula pelos eletrodos e fios metálicos.
IV. O eletrodo da meia-célula \( X \) é o catodo onde ocorre reação de redução.
V. As reações eletroquímicas podem ser representadas pelas seguintes equações estequiométricas:
\( X^{+2} + 2e^- \rightarrow X^0 \)
\( 2Y^0 \rightarrow 2Y^+ + 2e^- \)
A opção que apresenta APENAS afirmativas verdadeiras é:
Provas
O carbono (C) é um elemento presente no dia a dia. Ele está na gasolina (octano), no álcool de limpeza e combustível (etanol), no vinagre (ácido acético), entre outros. Quantas ligações do tipo sigma o carbono é capaz de realizar?
Provas
Na natureza, os átomos dos elementos nunca estão sozinhos, mas sempre ligados com outros átomos, doando, compartilhando e recebendo elétrons. Como são chamadas as espécies formadas quando um átomo recebe um elétron e quando perde um elétron, respectivamente?
Provas
Um químico está trabalhando em um laboratório químico e está incumbido de receber novos reagentes. Ao abrir as caixas que contêm os frascos dos reagentes, nota-se que, em alguns frascos, há estes dois pictogramas de perigo:

Assinale a alternativa que apresenta, respectivamente, o significado desses dois pictogramas de perigo.
Provas
Apesar de sua imensa variedade, os compostos orgânicos podem ser compreendidos em termos de grupos funcionais, isto é, pequenos grupos de átomos com funções características. Enquanto os hidrocarbonetos são construídos com átomos de carbono e hidrogênio, os grupos funcionais podem incluir átomos de outros elementos e, por isso, conferem propriedades aos compostos químicos. Nesse contexto, qual das alternativas a seguir NÃO é uma função orgânica?
Provas
36 Considere uma célula eletroquímica, em que as semirreações e os potenciais padrões de redução são dados a seguir:
Cátodo: Cu2+(aq) + 2e- → Cu(s) Eº = +0,34V
Ânodo: Zn2+(aq) + 2e- → Zn(s) Eº = -0,76V
Qual é o potencial-padrão dessa célula?
Provas
Caderno Container