Foram encontradas 36.242 questões.
O eteno, matéria-prima para a fabricação do polímero conhecido como polietileno, pode ser obtido por desidratação catalítica do etanol, um recurso natural renovável, conforme a reação:
\( C_2H_5OH (\ell) \longrightarrow H_2C = CH_2 (g) + H_2O (\ell) \)
Essa reação é catalisada por íons H+ (aq), cuja função é
Provas
Losartana (\( C_{22}H_{23}C\ell N_6O; \) massa molar = 423 g/mol) é um fármaco utilizado para o controle da pressão arterial. A massa do elemento carbono presente em uma dose de 50 mg desse fármaco é, aproximadamente,
Provas
A ação explosiva da nitroglicerina, fórmula molecular C3H5(NO3)3, é consequência da reação de sua decomposição, representada pela equação, parcialmente balanceada:
\( C_3H_5(NO_3)_3 (\ell) \longrightarrow \)
\( \longrightarrow \underline w N_2 (g) + 3CO_2(g) + \underline z H_2O(g) + { \large 1 \over 4} O_2(g) \)
Nessa equação, os coeficientes estequiométricos w e z são, respectivamente,
Provas
Analise a tabela, que fornece informações sobre dois elementos químicos, X e Y, em seu estado fundamental de energia.

Com base nos dados fornecidos na tabela, a ligação existente e a fórmula mínima do composto formado entre os elementos X e Y são, respectivamente,
Provas
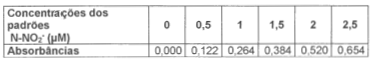
Foram preparados cinco padrões de nitrito dissolvido (N-NO2-) e uma prova em branco. Suas absorbâncias foram lidas utilizando uma cubeta com trajeto óptico (TO) de 50 mm, em um espectrofotômetro na faixa da luz visível, e apresentadas na tabela abaixo (curva de calibração). Ao analisar uma amostra de água da Área de Proteção Ambiental da Lagoa Verde, obteve-se uma absorbância de 0,284. Dessa forma, ao utilizar as fórmulas abaixo, a concentração em µM de N-NO2- na amostra da água analisada é:
Curva de calibração
Fórmulas
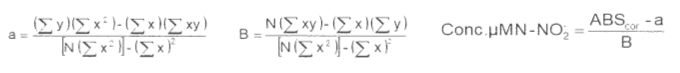
Em que:
x= concentração dos padrões.
y= absorbância dos padrões.
N= Número de padrões mais a prova em branco
Provas
Assinala a alternativa que apresenta um procedimento de quantificação por análise de volumetria complexométrica.
Provas
Deseja-se preparar 500 ml de solução estoque de dihidrogeno fosfato de potássio anidro (KH2PO4), com concentração de 5.000 µM de P-PO43-_ Quanto se deve pesar?
Dados: Massas atômicas (g moI1) K= 39, 10; H= 1,01; P= 30,97 e O= 16,00.
Provas
O "Plano de gerenciamento de resíduos químicos perigosos" é um instrumento de gestão elaborado a partir da Política Nacional de Resíduos Sólidos (PNRS), instituído pela Lei nº 12.305, de 2 de agosto de 201 O. Seu objetivo é realizar uma análise detalhada do gerenciamento dos resíduos, a fim de propor ações, metas e indicadores que garantam a conformidade com as normas vigentes e assegurem a destinação adequada dos resíduos gerados pelas atividades da Instituição. Segundo Jardim (1998), um programa desses, deve contemplar dois tipos de resíduos: o ativo e o passivo. A caracterização do passivo nem sempre é possível, além disso, o tempo e os esforços gastos com esta atividade inicial devem ser bem equacionados para que não haja um desestímulo logo no início. É importante lembrar que essa caracterização prioriza o reciclo e o reúso de tudo que for possível, bem como habilita o resíduo para a sua destinação final. A caracterização preliminar de resíduos químicos não-identificados pode ser realizada por meio de uma série de testes simples a seguir. Sendo assim, associa a segunda coluna (procedimento) de acordo com a primeira (teste).
Teste
(1) Resíduo redutor
(2) Presença de halogênios
(3) Presença de cianetos
(4) Presença de sulfetos
(5) Reatividade com água
Procedimento
( ) Adiciona-se uma gota de cloroamina-T e uma gota de ácido barbitúrico/piridina em três gotas de resíduo. A cor vermelha indica teste positivo.
( ) Observa-se a possível descoloração de um papel umedecido em 2,6- dicloro-indofenol ou azul de metileno.
( ) Na amostra acidificada com HCℓ, o papel embebido em acetato de chumbo fica enegrecido.
( ) Adiciona-se uma gota de água e observa-se a formação de chama, geração de gás ou qualquer outra reação violenta.
( ) Coloca-se um fio de cobre limpo e aquecido previamente ao rubro no resíduo e leva-se à chama. A cor verde indica teste positivo.
Assinala a alternativa que apresenta a sequência correta de preenchimento dos parênteses, quando lida de cima para baixo.
Provas
A determinação do oxigênio dissolvido (OD) em amostras de água pode ser realizada pelo método de Winkler, que envolve reações de oxirredução. Nessa técnica, uma solução de manganês II é adicionada à amostra e o oxigênio presente na água oxida o íon manganês para uma forma de manganês IV. Esse manganês IV então reage com íons iodeto (I-), liberando iodo molecular (I2), que é, posteriormente, titulado com uma solução padrão de tiossulfato de sódio (Na2S2O3).
As reações envolvidas são:
O2 + 2Mn2+ + 4OH \( ↔ \) 2MnO2 + 2H2O
MnO2 + 2I- + 4H+ \( ↔ \) Mn2+ + I2 + 2H2O
I2 + 2S2O32- \( ↔ \) 2I- + S4O62-
Com base nas informações acima, assinala a alternativa correta.
Provas
As substâncias ou os organismos manuseados em laboratório e os tipos de equipamentos operados podem resultar em acidentes, como intoxicações, envenenamentos, queimaduras térmicas e químicas, contaminação por agentes biológicos, incêndios, explosões. Esses acidentes podem ser evitados ou minimizados pelo uso de Equipamentos de Proteção Individual (EPI) e de Proteção Coletiva (EPC) de forma correta. Com relação aos EPI e EPCs, considera as afirmativas abaixo.
I. Os EPls são considerados dispositivos de uso individual destinados a proteger a integridade física e a saúde do trabalhador.
II. Os EPls são classificados de acordo com a parte do corpo que protegem: cabeça, tronco e membros superiores.
III. O funcionamento dos EPCs deve ser verificado periodicamente.
IV. Os EPCs são equipamentos de uso no laboratório que, quando bem especificados para as finalidades a que se destinam, permitem executar operações em condições de salubridade para o operador e as demais pessoas no laboratório.
Está(ão) CORRETA(S) a(s) afirmativa(s):
Provas
Caderno Container