Foram encontradas 36.279 questões.
Considere soluções aquosas independentes de dois sais solúveis em água: nitrato de chumbo (II) e cloreto de prata (I). Ao se misturar as duas soluções em um único recipiente, promove-se a formação de um produto insolúvel em água, que possui fórmula molecular
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Transformações Químicas e EnergiaTermoquímica
Calcule a variação da entalpia (ΔH) para a reação global de formação de 0,325 ton calcita a partir de seus elementos constituintes utilizando as reações e os dados termodinâmicos fornecidos a seguir.
Use: Massa molar O = 16 g.mol-1,
I) C(s) + O2(g) ➔ CO2(g) ∆ H = -393,5 kJ mol-1
II) CaO(s) ➔ Ca(s) + 1/2O2(g) ∆H = +635,0 kJ mol-1
III) CaO(s) + CO2(g) ➔ CaCO3(s) ∆H = -178,3 kJ mol-1
Provas
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
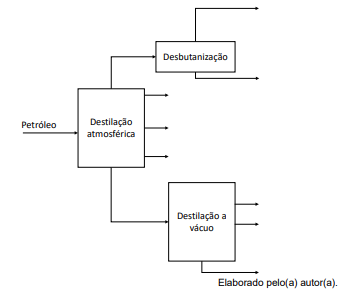
No processo descrito no fluxograma anterior, as destilações ocorrem produzindo
Provas
Provas
Um composto orgânico apresenta a seguinte fórmula molecular: C8H10O2. Sua estrutura revela a presença de um grupo carbonila e um grupo funcional que o caracteriza como um éster. Considere as seguintes informações:
• o composto apresenta isomeria geométrica;
• a hidrólise ácida do composto resulta na formação de ácido propanoico e um composto orgânico com fórmula
molecular C4H8O.
Com base nas informações fornecidas, a estrutura correta do composto orgânico é:
Provas
A entropia de um sistema é uma medida da sua desordem. A entropia do sistema aumenta quando há:
Provas
Das alternativas a seguir, aquela que representa a equação química balanceada para a combustão completa do etanol (C2H5OH) é:
Provas
Dentre as opções a seguir, o elemento que apresenta maior raio atômico, localizado no quarto período da Tabela Periódica e com número atômico 30, é o:
Provas
Considere a célula (pilha) representada na figura a seguir:
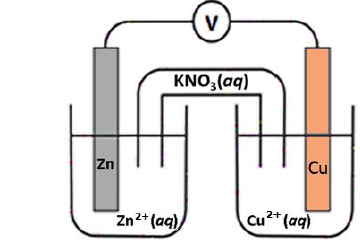
As semirreações são:
\( Zn^{2+}(aq) + 2e^– → Zn(s) Eº = –0,76 V \\ Cu^{2+}(aq) + 2e– → Cu(s) Eº = +0,34 V \)
Assinale a alternativa que corresponde à reação espontânea da célula (pilha):
Provas
Caderno Container