Foram encontradas 35.936 questões.
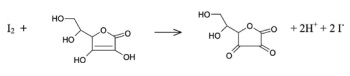
A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
O raio atômico do átomo de iodo elementar é menor do que o raio do íon iodeto (I⁻).
Provas

A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
A utilização de um catalisador provoca o aumento da entalpia de reação (ΔH), elevando a quantidade total de energia liberada ou absorvida.
Provas

A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
Na ausência do íon iodeto, que atua como catalisador, é esperado que a redução de H2O2 apresente uma energia de ativação menor do que a reação catalisada.
Provas

A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
Suponha-se que, em um dos experimentos, tenham sido usados 10 mL de iodeto de potássio 0,28 mol/L. Nesse caso, é correto afirmar que, considerando-se dissociação completa, o número de íons iodeto é superior a 2,0 × 1021.
Provas
Provas
Provas
Provas
Assinale a alternativa que descreve CORRETAMENTE a razão entre a acidez de uma solução com pH 3 e uma solução com pH 5.
Provas
(__)O espaço entre as partículas nos líquidos é bem menor que nos gases, por isso é mais difícil comprimir um líquido ou um sólido do que um gás.
(__)Nos líquidos, as partículas estão bem próximas umas das outras e não podem se movimentar, elas ficam apenas vibrando em uma posição fixa.
(__)Os líquidos têm a forma e o volume variáveis, conforme o recipiente.
Assinale a alternativa com a sequência CORRETA de cima para baixo.
Provas
Observe o exemplo abaixo:

Fonte: Mendonça, Vivian Lavander; Mendonça, Tereza Costa. Da escola para o mundo: Ciências: 5° ano. São Paulo: Scipione, 2021.
A figura representa na parte superior um prego e na parte inferior uma rolha, sobre a densidade desses materiais em relação a água, é possível afirmar que:
Provas
Caderno Container