Foram encontradas 36.167 questões.
Observação: Caso necessário, utilize a Tabela Periódica.
O hipoclorito de sódio (NaClO) possui propriedades bactericida e alvejante, fazendo com que seja utilizado no processo de cloração de águas de piscinas. Ele é produzido pela reação do gás cloro !$ \left(Cl_2\right) !$ com hidróxido de sódio (NaOH), como mostra a equação a seguir.
!$ Cl_{2(g)}+2NaOH_{(aq)}→NaCl_{(aq)}+NaClO_{(aq)}+H_2O_{(l)} !$
Em um processo de produção do hipoclorito de sódio, reagiram 5 kg de hidróxido de sódio com uma quantidade suficiente de gás cloro e foram obtidos 3,72 kg do hipoclorito de sódio. Nesse processo, o rendimento aproximado foi de
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
A pilha de iodo-lítio surgiu em 1967, nos Estados Unidos, e passou a ser utilizada como fonte de energia para aparelhos de marca-passo cardíaco, pois é capaz de funcionar continuamente por até dez anos. Ela é constituída, basicamente de lítio e iodo e pode ser representada por meio das semirreações 1 e 2, a seguir.
Semirreação 1: !$ Li_{(s)}→Li_{\ \ \ \ (aq)}^++1e^-\ Eº=+3,045V !$
Semirreação 2: !$ I_{2(s)}+2e^-→2I_{(aq)}^-\ Eº=+0,54V !$
Com base nos dados acima, tem-se o seguinte:
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
A análise elementar por combustão do glicerol, !$ C_3H_8O_3 !$, indicou a presença de 8,90 g de carbono. A massa da amostra de glicerol analisada é
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
A análise gravimétrica de cátions prata pode ser realizada por meio da precipitação desses cátions na forma de cloreto de prata. Se 215 mg de cloreto de magnésio forem adicionados em uma solução contendo nitrato de prata, sob agitação, a quantidade máxima de cloreto de prata que pode ser formada é
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
A epinefrina, ou adrenalina, tem fórmula molecular !$ C_9H_{13}NO_3 !$. A composição percentual em massa da epinefrina é
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
Ao se preparar uma solução aquosa de ácido clorídrico 0,100 molL-1 a partir da solução aquosa de ácido clorídrico concentrado, com teor de 37,5% em massa, deve-se considerar os seguintes procedimentos de segurança:
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
O acetoaminofenol, também conhecido como paracetamol, é um fármaco usado como analgésico e antipirético, cuja fórmula estrutural é apresentada a seguir.
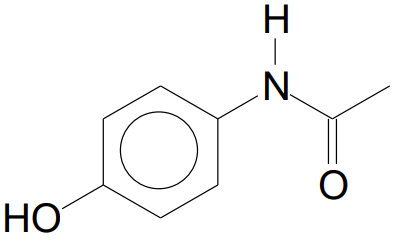
A fórmula molecular do acetoaminofenol é
Provas
Durante a pandemia do novo Coronavírus, o álcool foi amplamente utilizado na higienização da pele, superfícies e objetos. O álcool na concentração de 70% foi o mais utilizado, pois
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
O conceito de solubilidade ou coeficiente de solubilidade pode ser definido como a capacidade limite de dissolução de uma determinada substância (soluto) em outra (solvente) com a qual se misture de forma homogênea. A solubilidade de uma substância está diretamente ligada à quantidade de solvente disponível e à temperatura do sistema. A curva de solubilidade de um sal hipotético pode ser apresentada como mostrado na Figura 1.
Figura 1: Curva de solubilidade de um sal hipotético em água
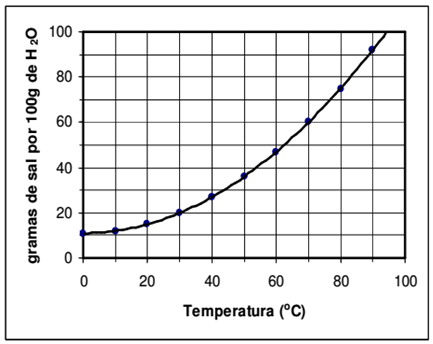
Disponível em: https://obqa.ufba.br Acesso em: 27 jan. 2022.
Considerando que, a 70°C, foram misturados 80g deste sal com 100 g de água, quando for atingido o equilíbrio
Provas
A estequiometria é a área da química que relaciona as quantidades de reagentes e produtos envolvidos em uma operação química e se baseia no princípio de que a soma das massas das substâncias reagentes em um recipiente fechado é igual à soma das massas dos produtos dessa reação.
Para se representar uma reação química, essa área utiliza equações, fórmulas, coeficientes estequiométricos adequados, além de relações intrínsecas a esse tema. Os cálculos estequiométricos podem relacionar as substâncias em quantidade de matéria (ou mol), número de partículas (moléculas, íons, átomos), massa ou volume, por exemplo.
Considere que de um determinado cilindro contendo 6,4 kg de gás metano foram removidas 18,06.1023 moléculas desse gás. Verifica se que (Dados: C = 12 g.mol-1; H = 1 g.mol-1):
Provas
Caderno Container