Foram encontradas 36.142 questões.
Uma mistura gasosa ideal de 4,0 kg de oxigênio e 1,3 kg de acetileno está contida em um vaso fechado de volume invariante, a 200 ºC e 300 kPa. Essa mistura entra em combustão e reage completamente, produzindo CO2 e H2O. Depois, deixa-se o meio resfriar por um certo tempo, de forma que os produtos continuam gasosos, e a pressão final medida é de 600 kPa.
É correto afirmar que:
Provas
Em uma célula voltaica a energia de Gibbs padrão de reação é determinada pela expressão:
!$ Δ !$G!$ \underset{r}{º} !$= - nFE!$ \underset{cel}{º} !$
em que n é um número adimensional que representa a quantidade de mols de elétrons transferidos nas semirreações de oxidação e de redução combinadas, F é a constante de Faraday e E!$ \underset{cel}{º} !$ é o potencial-padrão da célula.
Considere F = 96500 C/mol e os potenciais-padrão de redução do ferro e do alumínio, a 298 K, indicados abaixo.
| Fe2+(aq) + 2 e– !$ → !$ Fe(s) | Eº = −0,44 V |
| Al3+(aq) + 3 e– !$ → !$ Al(s) | Eº = −1,66 V |
Para uma célula voltaica formada pelo contato de dois metais quando uma peça de ferro é fixada com parafusos de alumínio, a 298 K, avalie as asserções a seguir.
I. O valor numérico de n é 5.
II. Com o passar do tempo, a peça fixada irá cair devido à corrosão do ferro.
III. Com o passar do tempo, a peça fixada irá cair devido à corrosão do alumínio.
IV. A energia de Gibbs padrão de reação da célula é igual a −706 kJ/mol.
V. Na célula voltaica formada, a oxidação do ferro é um processo espontâneo.
Assinale a opção que apresenta APENAS as afirmativas verdadeiras.
Provas
O peróxido de hidrogênio, H2O2, quando em contato com um ferimento na pele, é decomposto pela enzima catalase, liberando água e gás oxigênio, conforme reação a seguir.
!$ 2\,H_2O_2(I)→2\,H_2O(I)+O_2(g) !$
Considerando que 1,3 L de H2O2 (densidade = 1,00 g/mL) se decompõe a 40 °C e pressão de 1,0 atm, assinale a alternativa que apresenta o volume aproximado de gás oxigênio produzido.
Dados:
MM (H2O2) = 34 g/mol.
C = K (Kelvin) – 273
R = 0,082 L.atm/mol.K
Provas
I. Catação e peneiração. II. Filtração e decantação. III. Destilação fracionada e evaporação.
Marque a alternativa que corresponde, somente aos métodos de separação de misturas heterogêneas:
Provas
Provas
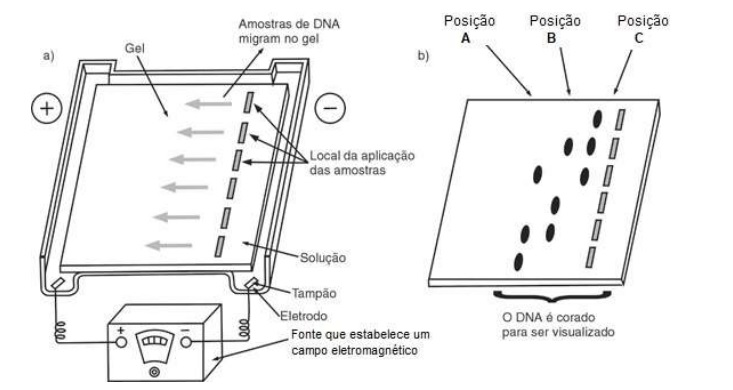
Disponível em: www.canal.cecierj.edu.br. Acesso em: 25 set. 2022 (adaptado).
As bandas formadas na posição A têm essa distribuição pois são constituídas por moléculas de menor
Provas
- Química OrgânicaGlicídios, Lipídios, Aminoácidos e Proteínas.
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
A utilização de soro de queijo na elaboração de bebidas lácteas constitui-se numa forma racional de aproveitamento deste produto secundário que apresenta excelente valor nutritivo. O gráfico a seguir apresenta os resultados de um experimento de preparação de bebidas lácteas com três concentrações de soro lácteo (30%, 40% e 50%) misturado ao leite.
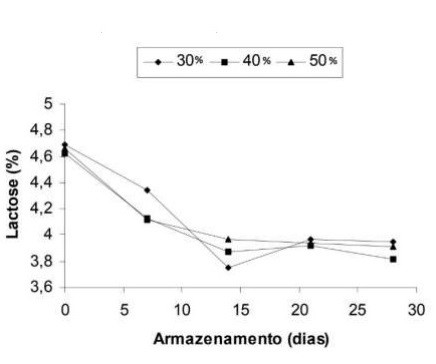
Disponível em: https://www.scielo.br. Acesso em: 29 set. 2022.
Ao longo do experimento, o pH dessas bebidas
Provas
Em Química, os índices inferiores à direita, representativos do número de átomos nas fórmulas das substâncias químicas, são:
Provas
O hidrogênio (H2) é considerado o combustível do futuro, porque sua queima gera grande quantidade de energia e o resíduo de combustão é água. A equação química que representa essa combustão é:
2 H2(g) + O2(g) !$ → !$ 2 H2O(g)
Nessa reação, o hidrogênio reage com o oxigênio em proporção 1:8 (em massa).
A esse respeito, analise as afirmativas a seguir.
I. A combustão completa de 5g de hidrogênio requer 40g de oxigênio.
II. A mistura de 4g de hidrogênio com 16g de oxigênio deverá gerar 20g de água.
III. A combustão de 2g de hidrogênio gera 2g de água.
Está correto o que se afirma em
Provas
O processo industrial de síntese de ureia ((NH2)2CO) passa por duas etapas principais:
2NH3 + CO2 !$ → !$ NH2C(O)ONH4 NH2C(O)ONH4 !$ → !$ (NH2)2CO + H2O
As etapas são, respectivamente, classificadas como reações de
Provas
Caderno Container